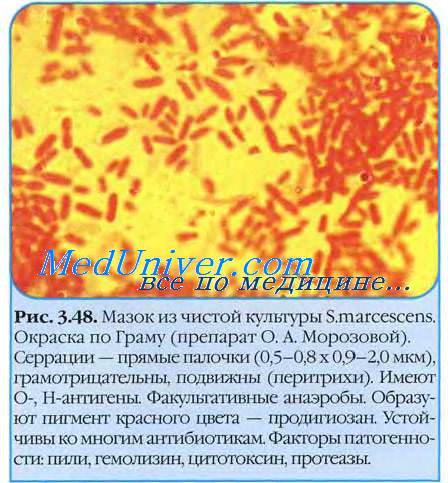
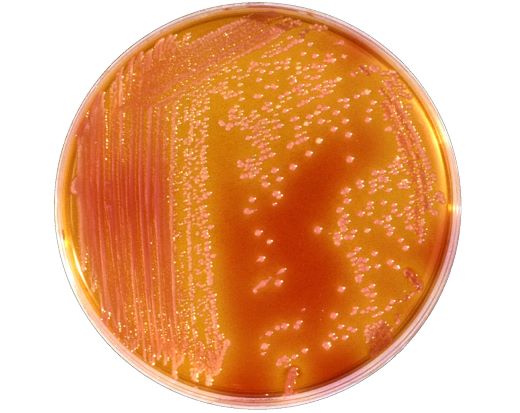
serratia marcescens в горле что это такое
Serratia marcescens в горле что это такое
Интерес к изучению серраций подтолкнула способность этих бактерий к образованию красного пигмента. В древние времена появление кровавых пятен на различных продуктах, особенно освящённой пище, считали дьявольским наваждением, что нередко становилось причиной народных волнений.
Серрации впервые выделил итальянский бактериолог Б. Бизио и назвал их Serratia marcescens (в честь лоцмана Серафино Серрати, проводившего суда по реке Арнб).
Род серраций образуют прямые подвижные (перитрихи) палочки размером 0,9-2,0×0,5-0,8 мкм, отдельные штаммы имеют капсулу. Серрации образуют розово-красный водорастворимый пигмент продигиозин.
Эпидемиология серраций. Распространенность серраций
Серрации распространены повсеместно в окружающей среде — их выделяют из почвы, воды, воздуха, с растений, различных предметов, а также из испражнений насекомых и грызунов.
Серрации, особенно serratia marcescens, ранее считали непатогенными и даже использовали при испытаниях аэрозолей или исследованиях циркуляции воздуха в помещениях из-за их ярко-красного пигмента. Экология S. marcescens аналогична таковой у синегнойной палочки.
В 60-х годах была установлена способность серраций вызывать бактериемию у стационарных пациентов и наркоманов. Позднее выяснилось, что у взрослых людей серрации наиболее часто колонизируют мочевыводящие и воздухоносные пути, а у детей — ЖКТ.
Serratia marcescens вызывает до 10% госпитальных бактериемии и пневмоний, 5% инфекций мочевыводнщих путей, хирургических ран и гнойничковых поражений кожи.
Важный момент — способность серраций к горизонтальной передаче (через руки медицинского персонала). Наиболее часто серрации проникают в организм через постоянные катетеры, интубационные устройства, а также препараты и растворы для внутривенных инфузий. У наркоманов, вводящих препараты внутривенно, часто возникают септические артриты, эндокардиты и остеомиелиты.
Топическая терапия при острых тонзиллофарингитах

Рассмотрены роль различных возбудителей в развитии воспалительных заболевания глотки и небных миндалин, а также подходы к лечению воспалительных заболеваний ротоглотки с использованием антисептиков местного действия.
Meaning of different agents in development of inflammatory diseases of pharynx and palatine tonsils was considered, as well as approaches to treatment of fauces inflammatory diseases using antiseptics with local effect.
Микробиота слизистых оболочек, которая представлена сообществами микроорганизмов в виде биопленок, гомеостатична и играет положительную роль в обменных процессах на слизистой оболочке и защите от внешних патогенов. В организме человека специфическое преимущество такой организации микроорганизмов заключается в обеспечении гомеостаза органов, функциональность которых зависит от населяющих их микробов. Здоровый вид кожи, нормальное пищеварение и, конечно, устойчивость к внешней инфекции (состояние иммунитета) человека во многом определяется стабильностью, можно сказать, «здоровьем», его микрофлоры [2].
Макроорганизм и его микрофлора в нормальных условиях находятся в состоянии эубиоза, сложившегося в процессе эволюции. При изменении баланса участия микроорганизмов в физиологических процессах на слизистых оболочках или коже организма-хозяина нарушается гомеостаз метаболических процессов, стабильность иммунной системы. Если возмущение превосходит компенсаторные ресурсы организма, происходит неконтролируемый каскад различных физиологических, биохимических и иммунных процессов с клиническими проявлениями в виде симптомокомплексов. Кишечные, кожные, кардиоваскулярные, мочеполовые и другие заболевания причинно-следственно связаны с изменением микрофлоры местной локализации и кишечной, как депо микроорганизмов в теле человека [22].
_250.gif)
Эти современные знания о биопленках важны и для понимания роли микрофлоры верхних дыхательных путей в здоровье организма, и принципах лечения острых респираторных вирусных заболеваний. Микрофлора глотки многочисленна и вариабельна и в норме сходна с микрофлорой пищеварительного и респираторного трактов. В ее составе у здоровых людей постоянно обнаруживают β-гемолитические и негемолитические стрептококки, микрококки, эпидермальный стафилококк, нейссерии, дифтероиды, псевдодифтерийные бактерии, вейлонеллы, бактероиды, актиномицеты, сапрофитические трепонемы, микоплазмы. Факультативными для глотки являются: золотистый стафилококк, β-гемолитический стрептококк, клебсиелла, пневмонии и др. энтеробактерии, кандиды, нокардии, а также гемофильная палочка [13].
Постоянные микроорганизмы относятся к комменсалам, и их спектр сформировался благодаря эволюционно сложившимся отношениям симбиоза и антагонизма между самими микроорганизмами и их взаимоотношениями с макроорганизмом. В разнообразии видов здесь доминируют бактерии. Простейшие и вирусы представлены значительно меньшим числом видов. В норме от микроорганизмов свободны кровь, ликвор, синовиальная жидкость, костный мозг, брюшная полость, плевральная полость, матка [22].
В полости рта находится больше различных видов бактерий, чем в остальных отделах желудочно-кишечного тракта, и это количество, по данным разных авторов, составляет от 160 до 300 видов. Бактерии попадают в полость рта с воздухом, водой, пищей — так называемые транзитные микроорганизмы, время пребывания которых ограничено. А постоянная (резидентная) микрофлора, образующая сложную и стабильную экосистему полости рта и глотки, — это 30 видов микроорганизмов, которые выполняют ряд функций: с одной стороны, они участвуют в переваривании пищи, оказывают большое позитивное влияние на иммунную систему, являясь мощными антагонистами патогенной флоры; с другой стороны, они служат возбудителями и главными виновниками основных стоматологических и оториноларингологических заболеваний [5].
В развитии воспалительных заболевания глотки и небных миндалин ведущую роль занимают микроорганизмы, вегетирующие на слизистых ротовой полости и глотки. Следует отметить их разнообразие, среди которого аэробные, а также факультативные и облигатные анаэробные микроорганизмы, представленные грамотрицательными и грамположительными микроорганизмами. Значение микроорганизмов в возникновении воспалительных заболеваний тонзилло-фарингеальной зоны очень велико. Ключевыми факторами в развитии гнойного воспаления являются нарушение симбиоза между макро- и микроорганизмами, приобретение патогенных свойств микроорганизмами. Увеличение критического числа микробных тел, возрастание их инвазивности, выработка экзо- и эндоферментов, продуктов метаболизма способствуют формированию патологического очага и его распространению [1, 6].
Важно то, что это разнообразие микроорганизмов представляет собой оптимальные возможности для передачи детерминант резистентности, а в качестве резервуара будет в этом случае выступать нормальная микрофлора человека. Использование как системных, так и топических антибиотиков в случаях, когда они не показаны, вносит значительный вклад в этот процесс и способствует распространению в популяции микроорганизмов, устойчивых к антибиотикам [6, 9].
Инфекционные заболевания глотки — тонзиллиты и тонзиллофарингиты — большая группа заболеваний, различных по этиологиям, клиническим проявлениям, а также морфологическим и патоморфологическим признакам. Объединяющим фактором здесь служат микроорганизмы [2, 10].
Имеется прямая взаимосвязь между состоянием иммунной системы и активацией непатогенной флоры и/или оппортунистической микрофлоры полости рта (орроrtonus — удобный). Оппортунистические микроорганизмы активируются в условиях, удобных для них, — это иммунодефицитные состояния. Когда местные или системные механизмы нарушены, развивается оральный кандидоз, обусловленный дрожжеподобными грибами, присутствующими во рту у здоровых людей.
Самую большую группу постоянно обитающих в полости рта бактерий представляют кокки — 85–90% от всех видов. Они обладают значительной биохимической активностью, разлагают углеводы, расщепляют белки с образованием сероводорода.
Стрептококки являются основными обитателями полости рта: S. mutans, S. mitis, S. sanguis. Большинство из них — факультативные анаэробы, но встречаются и облигатные анаэробы (пептококки). Кислоты, продуцируемые стрептококками, подавляют рост некоторых гнилостных микроорганизмов, попадающих в полость рта из внешней среды. В зубном налете и на деснах здоровых людей присутствуют также стафилококки — St. epidermidis, иногда St. aureus [2].
Верхние отделы дыхательных путей несут особенно высокую микробную нагрузку, так как они анатомически приспособлены для осаждения бактерий из вдыхаемого воздуха. Помимо обычных негемолитических и зеленящих стрептококков, непатогенных нейссерий, стафилококков и энтеробактерий, в носоглотке можно обнаружить менингококки, пиогенные стрептококки, пневмококки и бордетеллы. Следует отметить, что указанные отделы у новорожденных обычно стерильны и колонизируются в течение 2–3 сут. По мере совершенствования защитных механизмов вероятность носительства патогенных бактерий снижается, и их сравнительно редко выделяют уже у подростков.
На состав микробных сообществ различных полостей организма влияют самые разнообразные факторы: чистота вдыхаемого воздуха, наличие пыли, химических и бактериальных загрязнений. Однако наибольшее воздействие оказывают заболевания, патогенез которых включает изменения физико-химических свойств эпителиальных поверхностей и прием антимикробных препаратов.
Стрептококки группы A (Str. pyogenes) — обычно вызывают фарингит, инфекцию кожи и мягких тканей, реже пневмонию и послеродовой сепсис, постинфекционные осложнения ревматизма и острый гломерулонефрит (ОГН). Они имеют много вирулентных факторов, включая антифагоцитарный М-протеин и тонкую капсулу из гиалуроновой кислоты, а также группу внеклеточных токсинов и ферментов, в том числе пирогенный токсин, стрептолизин, стрептокиназу и ДНКазы.
Тонзиллофарингит — рутинная инфекция среди взрослых и детей старше 3 лет, она дает 20–40% всех случаев острых фарингитов, передается от человека к человеку респираторным путем, а в ряде случаев и с пищей. Инкубационный период составляет в среднем 14 сут, после чего появляются боль в горле, лихорадка, озноб, плохое самочувствие, иногда тошнота, рвота и боль в животе. Симптомы весьма разнообразны, варьируя от минимальных до ярко выраженных с увеличением миндалин, гнойный налет отмечается на миндалинах и задней стенке глотки, шейные лимфатические узлы увеличены и болезненны. Обычно неосложненный стафилококковый фарингит длится 3–5 дней. Гнойные осложнения, нечастые из-за широкого применения антибиотиков, включают острый средний отит, синусит, перитонзиллярный или заглоточный абсцесс, менингит, воспаление легких, бактериемию, эндокардит [1, 2, 10].
В этиологии острого тонзиллофарингита участвуют как вирусы (риновирусы, ротавирусы, вирусы парагриппа, вирусы Коксаки), так и бактерии (стрептококки групп А, C, G, стафилококки, нейссерии, коринебактерии, спирохеты, листерии). Среди возбудителей бактериальной природы наибольшее значение принадлежит β-гемолитическому стрептококку группы А (БГСА, Streptococcus pyogenes), встречающемуся в 5–30% случаев острого тонзиллофарингита и обострения хронического тонзиллофарингита [12, 13].
Наиболее значимым бактериальным возбудителем острого тонзиллита является БГСА. Реже острый тонзиллит вызывают вирусы, стрептококки групп C и G, Arcanobacterium haemolyticum, Neisseria gonorrhoeae, Corynebacterium diphtheria (дифтерия), анаэробы и спирохеты (ангина Симановского–Плаута–Венсана), крайне редко — микоплазмы и хламидии [32]. В соответствии с Международной классификацией болезней 10-го пересмотра выделяют стрептококковый фарингит (J02.0), стрептококковый тонзиллит (J03.0). В зарубежной литературе широко используются взаимозаменяемые термины «тонзиллофарингит» и «фарингит». В России используется термин «стрептококковый тонзиллит», под которым понимается тонзиллит (ангина) или фарингит, вызванный БГСА.
БГСА передается воздушно-капельным путем. Источниками инфекции являются больные и, реже, бессимптомные носители. Инкубационный период при остром БГСА-тонзиллите составляет от нескольких часов до 2–4 дней. Хотя острый тонзиллит считается инфекционным заболеванием, стрептококковую ангину можно рассматривать как обострение хронического тонзиллита.
Золотым стандартом определения БГСА в полости рта, а значит, для назначения антибактериальной терапии, является Стрептатест. Чувствительность данного теста составляет по данным многоцентровых клинических исследования [19] 97,3%, а специфичность 95,3%. Современные тестовые системы позволяют получать результат через 15–20 минут с высокой специфичностью (95–100%), но меньшей, чем при культуральном исследовании, чувствительностью (60–95%). Экспресс-методы дополняют, но не заменяют культуральный метод. Кроме того, только при выделении возбудителя можно определить его чувствительность к антибиотикам [2, 19].
В России проблема нерационального использования антибиотиков при инфекциях верхних дыхательных путей осложняется и возможностью их безрецептурного приобретения пациентами и использования для самолечения. Польза от применения антибиотиков при фарингите весьма незначительна. Согласно результатам метаанализа, у 90% больных симптомы исчезают в течение недели независимо от приема антибиотиков. Антибиотики могут сокращать продолжительность симптомов менее чем на сутки. Более того, вероятность повторного обращения в медицинское учреждение по поводу фарингита у лиц, получавших антибиотики, выше, чем у пациентов, не принимавших их. При этом следует помнить, что антибактериальные препараты являются потенциально токсичной фармакологической группой и обусловливают до 25–30% всех побочных эффектов лекарственных средств [4, 7, 9, 11].
Согласно данным исследователей, системная антибактериальная терапия показана только при подтвержденной бактериальной этиологии фарингита. Согласно международным рекомендациям (Mac Isaac, 1994) [20], клинические критерии бактериальной этиологии фарингита следующие: воспаление миндалин, увеличение шейных лимфатических узлов, лихорадка и отсутствие кашля. Если у пациента присутствуют все 4 критерия, то антибактериальная терапия может назначаться эмпирически. Наличие двух или трех из перечисленных критериев + положительный тест на стрептококк группы А являются показанием к назначению антибиотиков. Пациентам, у которых отмечен один из указанных критериев или не было ни одного, не требуются постановка теста на стрептококковый антиген и проведение антибактериальной терапии.
Известно, что примерно 70% фарингитов вызываются вирусами, среди которых отмечают риновирусы, коронавирусы, среди бактериальных возбудителей острого фарингита ведущая роль принадлежит БГСА: 15–30% случаев заболевания у детей и 5–17% случаев у взрослых, относительно редко (
ФГБУ НКЦО ФМБА России, Москва
Семейство Enterobacteriaceae. Часть 2
Автор: врач – клинический фармаколог Трубачева Е.С.

Автор: врач – клинический фармаколог Трубачева Е.С.
Сегодня мы закончим разговор о микроорганизмах из семейства Enterobacteriaceae, которое, как мы помним, является одним из самых проблематичных источников внутрибольничных инфекций, потому что возбудители умеют делиться и передавать в рамках почти всего семейства свои механизмы резистентности, и это при том, что изначально почти каждый представитель имеет природную устойчивость к целым классам антибиотиков.
Героями сегодняшнего разговора станут энтеробактеры, серрации, морганеллы. Конечно, есть и другие представители и, возможно, в постковид они начнут встречаться намного чаще, но пока нам в рамках Азбуки достаточно вышеперечисленных плюс кишечные палки и клебсиеллы, о которых мы говорили ранее.
Enterobacter spp.
Микробиологические аспекты
Род энтеробактера включает несколько видов, но наиболее клинически значимыми из них являются:
Очень важно помнить, что энтеробактеры проявляют природную устойчивость к большому спектру антибиотиков, таким как бета-лактамы, к которым они продуцируют хромосомные AmpC бета-лактамазы, плазмидные бета-лактамазы расширенного спектра, а также карбапенемазы. Так как клинически значимые представители Enterobacter spp. обитают в желудочно-кишечном тракте человека, то основным источником инфицирования для пациента становится медицинский персонал, который просто по факту своей ежедневной работы в больнице с антибиотиками является резервуаром всевозможных антибиотикорезистентностей.
Клинически значимые аспекты
Enterobacter spp. является причиной:
Инфекций мочевыводящих путей: катетер— или инструментально-ассоциированных (как результат эндоскопических манипуляций контаминированным инструментарием).
Внутрибольничных пневмоний, в том числе вентилятор-ассоциированных.
Инфекций кожи и мягких тканей, таких как раневые инфекции, инфицирование пролежней, ожоговые инфекции и послеоперационные инфекции. Кроме того в случае полимикробного характера инфицирования пролежней возможно развитие сепсиса как исхода раневой инфекции.
Инфекций кровотока — катетер— и инструмент-ассоциированные.
Инфекций центральной нервной системы — менингиты, чаще всего внутрибольничные, как следствие нейрохирургических вмешательств.
Неонатальных инфекций, таких как некротический энтероколит, сепсис и менингит.
Чем лечить?
Ответ будет традиционным — лучше вообще не инфицировать, тогда не придется ломать голову, чем все это лечить. В основе терапии лежит обязательное микробиологическое исследование с определением антибиотикочувствительности.
В случае выявления представителей Enterobacter spp. при лечении тяжелых инфекций предпочтение следует отдавать комбинированной терапии, и самыми подходящими будут пиперациллин-тазобактам в комбинации с аминогликозидами или фторхинолонами. А для преодоления резистентности, вызванной бета-лактамазами расширенного спектра, можно использовать карбопенемы.
Для лечения инфекций мочевыводящих путей самым первым и наиважнейшим является удаление мочевого катетера до момента прекращения пиурии. Далее лечим либо исходя из профиля антибиотикограммы, либо ципрофлоксацином в правильно подобранной дозе, либо, как было указано выше, рассматриваем назначение нитрофуранов и фосфомицина.
Serratia spp.
Серрации по своей сути являются родными сестрами клебсиелл, но в отличие от последних только S.marcescens вызывает клинически значимые заболевания у людей, а остальные виды — S.liquefaciens и S.rubidaea — делают это значительно реже, и в обычной, доковидной жизни, ими можно было пренебречь.
Клинические аспекты
Что вызывает?
Катетер-ассоциированные инфекции и как их исход — сепсис.
Инфекции мочевыводящих путей как следствие медицинских манипуляций необработанным инструментом.
Раневые инфекции в послеоперационном периоде.
Нозокомиальные пневмонии как следствие интубации.
Конъюнктивиты и кератиты.
И редко вызывали остеомиелиты и эндокардиты
Терапевтические аспекты
В первую очередь про серрацию надо узнать, а значит, необходимо микробиологическое исследование. Во-вторую, вспомнить о природной устойчивости. В-третью, держать в уме то, что очень часто цефалоспорины третьего и четвертого поколения тоже не будут работать, так как посредством плазмид получают устойчивость от родственников по семейству Enterobacteriaceae, например, от родной сестры — клебсиеллы. Точно таким же образом серрация может оказаться устойчивой и к карбопенемам. К фторхинолонам резистентность так же уже давно описана.
Так чем лечить?
Лучше вообще не заражать — потому что если бак. лаборатория дает серрацию, то ниоткуда кроме как с наших рук она появиться не может, так как ни ходить, ни летать сия зверюшка до сих пор не научилась.
В случае развития тяжелых инфекций — сепсиса, вентилятор-ассоциированной пневмонии и т. п., и только при документированной чувствительности, препаратами выбора могут быть цефепим или меропенем, или ципрофлоксацин в вену в стандартных дозировках. Если чувствительность утеряна, то зовем клинического фармаколога, а если такового нет, то смотрим в сторону амикацина, пиперациллина-тазобактама и азтреонама, только помним об их побочных эффектах. Курс лечения соблюдать жизненно необходимо, чтобы зверюшка еще куда-нибудь не мутировала и новыми механизмами защиты не обзавелась. Обычно речь идет о 10–14 днях (но так как польза превышает вред, то нефротоксичность аминогликозидов со временем отступит, а ототоксичность — тут уж как повезет).
Инфекции мочеполового тракта лечим так же с учетом чувствительности, и если таковая располагает, то препаратом выбора становятся фторхинолоны, либо комбинация двух антибиотиков, например фторхинолон с карбапенемом или бета-лактам с аминогликозидом.
Эндокардиты с остеомиелитами бывают хоть и редко, но крайне метко, а потому снова сначала исследуем чувствительность, потом индивидуально в каждом случае подбираем антибиотики (а лучше зовем клинического фармаколога, пусть он мучается). И снова крайне важно соблюдение сроков лечения, для эндокардита это порядка четырех, а то и шести недель внутривенной антибактериальной терапии, а для остеомиелита не менее двух недель. Почему нельзя меньше? Потому что последует мутация и новый рецидив, а антибиотиков просто может не хватить, ибо, как и сестра-клебсиелла, серрация тоже умеет в панрезистентность.
В заключении хочется повторить, что и в этом случае проще помыть руки, чем разгребать последствия инфицирования серрацией. Мытье рук и проще, и дешевле, и, что самое главное, спокойнее.
Morganella spp.
Морганеллы будут последними представителями семейства Enterobacteriaceae, которых мы обсуждаем в рамках нашей Азбуки. Если кому-то станет интересно покопаться дальше, то к их услугам всегда будет четырехтомник по медицинской микробиологии под редакцией Лабинской, конкретно второй и третий том, в которых все очень подробно расписано, правда, чтение это для неподготовленного человека будет довольно сложным. Но вернемся к нашей морганелле.
Микробиологические аспекты
Морганелла существует только одна — M.morganii, но имеет два подвида — M.morganii и M.sibonii, которые отличаются только по ферментации треалозы, и никакого клинического значения данное отличие не имеет.
Конечно, и морганелла умеет в природную устойчивость к антибиотикам, а именно к пенициллинам, цефалоспоринам первого и второго поколения, макролидам и ко-тримоксазолу. При этом сохраняет высочайшую чувствительность к аминогликозидам, пиперациллину, цефалоспоринам третьего и четвертого поколения, фторхинолонам и карбопенемам. То есть данную зверюшку есть чем победить.
Клинические аспекты
Морганелла является представителем нормальной микрофлоры человека и самостоятельно крайне редко что-то вызывает. Этим крайне редким являются инфекции мочевыводящих путей, чему способствуют крайне пожилой возраст, длительная госпитализация, мочевой катетер и иммунодефицит любой этиологии.
В плане приобретенной антибиотикорезистентности морганелла обзавелась факторами устойчивости к фторхинолонам, что и понятно, учитывая какие именно заболевания она вызывает и чем их чаще всего лечат.
Что еще может вызывать?
Крайне редко — сепсис, как исход инфекции мочевыводящих путей.
Раневую хирургическую инфекцию.
Неонатальный сепсис и хореоамнионит.
Но стоит иметь в виду, что данные ситуации крайне редки, и стоит изначально подумать не об этом возбудителе, а о том, какой за ним может прятаться в виду контаминации материала, и лучше бы все еще раз пересеять и перепроверить.
Терапевтические аспекты
Если результат микробиологического исследования сомнений не вызывает и вы убеждены, что имеете дело с морганеллами, то препаратами выбора становятся карбопенемы, и только в случае их недоступности и документированной бактериологом чувствительности, можно посмотреть в сторону цефалоспоринов, например, цефтазидима (для которого нужна отдельная цефалоспориназа, чтобы он был инактивирован), а лучше цефтазидим-авибактама. Хотя если недоступны карбопенемы, то и Завицефте, скорее всего, взяться будет неоткуда.
Какие препараты могут быть использованы в качестве резервных? Решать этот вопрос также необходимо только после получения результата микробиологии и чувствительности в идеале по МПК, и только после этого рассматривать назначение цефепима или ципрофлоксацина, или аминогликозидов (они, к слову, в случае морганеллы могут обоснованно выступать в качестве монотерапии инфекций мочевыводящих путей).
На этом автор заканчивает обзор семейства Enterobacteriaceae и в сотый раз призывает: «Коллеги, мойте руки! Это намного проще, дешевле и быстрее, чем лечить то, что с немытых рук может упасть в пациента».