Что выделяется при горении топлива
Продукты горения (сгорания)
Продукты горения – это вещества (газообразные, жидкие или твердые вещества) и соединения, образующиеся в результате сложного физико-химического процесса горения веществ (материалов).
Под продуктами горения чаще всего понимают дым, токсичные продукты горения, сажу и другие.
Продукты горения сухой травы
Состав
Состав их зависит от состава горящего вещества и условий его горения. В условиях пожара чаще всего горят органические вещества (древесина, ткани, бензин, керосин, резина и др.), в состав которых входят главным образом углерод, водород, кислород и азот. При горении их в достаточном количестве воздуха и при высокой температуре образуются продукты полного сгорания: СО2, Н2О, N2. При горении в недостаточном количестве воздуха или при низкой температуре кроме продуктов полного сгорания образуются продукты неполного сгорания: СО, С (сажа).
Продукты сгорания называют влажными, если при расчете их состава учитывают содержание паров воды, и сухими, если содержание паров воды не входит в расчетные формулы.
Реже во время пожара горят неорганические вещества, такие как сера, фосфор, натрий, калий, кальций, алюминий, титан, магний и др. Продуктами сгорания их в большинстве случаев являются твердые вещества, например Р2О5, Na2O2, CaO, MgO. Образуются они в дисперсном состоянии, поэтому поднимаются в воздух в виде плотного дыма. Продукты сгорания алюминия, титана и других металлов в процессе горения находятся в расплавленном состоянии.
При неполном сгорании органических веществ в условиях низких температур и недостатка воздуха образуются более разнообразные продукты – окись углерода, спирты, кетоны, альдегиды, кислоты и другие сложные химические соединения. Они получаются при частичном окислении как самого горючего, так и продуктов его сухой перегонки (пиролиза). Эти продукты образуют едкий и ядовитый дым. Кроме того, продукты неполного горения сами способны гореть и образовывать с воздухом взрывчатые смеси. Такие взрывы бывают при тушении пожаров в подвалах, сушилках и в закрытых помещениях с большим количеством горючего материала. Рассмотрим кратко свойства основных продуктов горения.
Углекислый газ
Углекислый газ или двуокись углерода (СО2) – продукт полного горения углерода. Не имеет запаха и цвета. Плотность его по отношению к воздуху равна 1,52. Плотность углекислого газа при температуре Т = 0 ° С и при нормальном давлении р = 760 миллиметров ртутного столба (мм Hg) равна 1,96 кг/м 3 (плотность воздуха при этих же условиях равна ρ = 1,29 кг/м 3 ). Углекислый газ хорошо растворим в воде (при Т = 15 °С в одном литре воды растворяется один литр газа). Углекислый газ не поддерживает горение веществ, за исключением щелочных и щелочно-земельных металлов. Горение магния, например, происходит в атмосфере углекислого газа по уравнению:
Токсичность углекислого газа незначительна. Концентрация углекислого газа в воздухе 1,5 % безвредна для человека длительное время. При концентрации углекислого газа в воздухе, превышающей 3-4,5 %, нахождение в помещении и вдыхание газа в течение получаса опасно для жизни. При температуре Т = 0 °С и давлении р = 3,6 МПа углекислый газ переходит в жидкое состояние. Температура кипения жидкой углекислоты составляет Т = –78 °С. При быстром испарении жидкой углекислоты газ охлаждается и переходит в твердое состояние. Как в жидком, так и твердом состоянии, капли и порошки углекислоты применяются для тушения пожаров.
Оксид углерода
Всем известная вода – Н2О – также выделяется во время горения виде газа – как пар. Вода является продуктом горения газа метана – СН4. Вообще, вода и углекислота в основном выделяются при полном сгорании всех органических веществ.
Цианистый водород
Акролеин
Пропеналь, акролеин, акрилальдегид – все это названия одного вещества, ненасыщенного альдегида акриловой кислоты: СН2=СН-СНО. Этот альдегид тоже является сильно летучей жидкостью. Акролеин бесцветен, с резким запахом, очень ядовит. При попадании жидкости или ее паров на слизистые, особенно в глаза, вызывает сильное раздражение. Пропеналь является высокореакционным соединением, и это объясняет его высокую токсичность.
Формальдегид
Подобно акролеину, формальдегид принадлежит к классу альдегидов и является альдегидом муравьиной кислоты. Также это соединение известно как метаналь. Это токсичный, бесцветный газ с резким запахом.
Азотсодержащие вещества
Чаще всего во время горения веществ, содержащих азот, выделяется чистый азот – N2. Этот газ и так содержится в атмосфере в большом количестве. Азот может быть примером продукта горения аминов. Но при термическом разложении, к примеру, солей аммония, а в некоторых случаях и при самом горении, в атмосферу выбрасываются и его оксиды, со степенью окисления азота в них плюс один, два, три, четыре, пять. Оксиды – газы, имеют бурый цвет и чрезвычайно токсичны.
Сернистый газ
При горении многих веществ, кроме рассмотренных выше продуктов сгорания выделяется дым – дисперсная система, состоящая из мельчайших твердых частиц, находящихся во взвешенном состоянии в каком-либо газе. Диаметр частиц дыма составляет от 10 −4 до 10 −6 см (от 1 до 0,01 мкм). Отметим, что 1 мкм (микрон) равен 10 −6 м или 10 −4 см. Более крупные твердые частицы, образующиеся при горении, быстро оседают в виде копоти и сажи. При горении органических веществ дым содержит твердые частицы сажи, взвешенные в CO2, CO, N2, SO2 и других газах. В зависимости от состава и условий горения вещества получаются различные по составу и по цвету дымы. При горении дерева, например, образуется серовато-черный дым, ткани – бурый дым, нефтепродуктов – черный дым, фосфора – белый дым, бумаги, соломы – беловато-желтый дым.
В составе дыма, образующегося на пожарах при горении органических веществ, кроме продуктов полного и неполного сгорания, содержатся продукты термоокислительного разложения горючих веществ. Образуются они при нагреве еще негорящих горючих веществ, находящихся в среде воздуха или дыма, содержащего кислород. Обычно это происходит перед факелом пламени или в верхних частях помещений, где находятся нагретые продукты сгорания.
Состав продуктов термоокислительного разложения зависит от природы горючих веществ, температуры и условий контакта с окислителем. Так, исследования показывают, что при термоокислительном разложении горючих веществ, в молекулах которых содержатся гидроксильные группы, всегда образуется вода. Если в составе горючих веществ находятся углерод, водород и кислород, продуктами термоокислительного разложения чаще всего являются углеводороды, спирты, альдегиды, кетоны и органические кислоты. Если в составе горючих веществ, кроме перечисленных элементов, есть хлор или азот, то в дыме находятся также хлористый и цианистый водород, оксиды азота и другие соединения. Так, в дыме при горении капрона содержится цианистый водород, при горении линолеума «Релин» – сероводород, диоксид серы, при горении органического стекла – оксиды азота. Продукты неполного сгорания и термоокислительного разложения в большинстве случаев являются токсичными веществами, поэтому тушение пожаров в помещениях производят только в кислородных изолирующих противогазах.
Пепел, зола, копоть, сажа, уголь
Копоть, или сажа – остатки углерода, который не вступил в реакцию, по разным причинам. Сажу называют также амфотерным углеродом. Зола, или пепел – мелкие частицы неорганических солей, не сгоревших или не разложившихся при температуре горения. При выгорании топлива эти микросоединения переходят во взвешенное состояние или скапливаются внизу. А уголь – это продукт неполного сгорания дерева, то есть не сгоревшие его остатки, но при этом еще способные гореть. Конечно, это далеко не все соединения, которые выделятся при сгорании тех или иных веществ. Перечислить их всех нереально, да и не нужно, потому что другие вещества выделяются в ничтожно малых количествах, и только при окислении определенных соединений.
Классификация
Большинство продуктов горения являются отравляющими веществами. Поэтому, говоря об их классификации, будет правильным ознакомить вас со следующим термином:
Классификация опасности веществ по степени воздействия на организм – это установление (ранжирование) уровней опасности веществ по их поражающему и повреждающему воздействию на организм человека и (или) животного. Более подробно о данной классификации читайте в материале по ссылке >>
Также ознакомьтесь с познавательным материалом по теме:
Формулы для расчета объема
Вид формулы для расчета объема продуктов полного сгорания при теоретически необходимом количестве воздуха зависит от состава горючего вещества.
Индивидуальное химическое соединение
В этом случае расчет ведут, исходя из уравнения реакции горения. Объем влажных продуктов сгорания единицы массы (кг) горючего вещества при нормальных условиях рассчитывают по формуле:
Vп.с. – объем влажных продуктов сгорания, м 3 /кг; 
Например, чтобы определить объем сухих продуктов сгорания 1 кг ацетона при нормальных условиях, составляем уравнение реакции горения ацетона в воздухе:
Определяем объем сухих продуктов сгорания ацетона:
Объем влажных продуктов сгорания 1 м 3 горючего вещества (газа) можно рассчитать по формуле:
Vп.с. – объем влажных продуктов сгорания 1 м 3 горючего газа, м 3 /м 3 ; 
Сложная смесь химических соединений
Если известен элементный состав сложного горючего вещества, то состав и количество продуктов сгорания 1 кг вещества можно определить по уравнению реакции горения отдельных элементов. Для этого составляют уравнения реакции горения углерода, водорода, серы и определяют объем продуктов сгорания, приходящийся на 1 кг горючего вещества. Уравнение реакции горения имеет вид:
С + О 2 + 3,76N 2 = СО 2 + 3,76N 2
При сгорании 1 кг углерода получается 22,4 / 12 = 1,86 м 3 СО 2 и 22,4 × 3,76/12 = 7,0 м 3 N 2.
Аналогично определяют объем (в м 3 ) продуктов сгорания 1 кг серы и водорода. Полученные данные приведены ниже:
| СО2 | N2 | Н2О | SO2 | |
| Углерод | 1,86 | 7,00 | – | – |
| Водород | – | 21,00 | 11,2 | – |
| Сера | – | 2,63 | – | 0,7 |
При горении углерода, водорода и серы кислород поступает из воздуха. Однако в состав горючего вещества может входить кислород, который также принимает участие в горении. В этом случае воздуха на горение вещества расходуется соответственно меньше.
В составе горючего вещества могут находиться азот и влага, которые в процессе горения переходят в продукты сгорания. Для их учета необходимо знать объем 1 кг азота и паров воды при нормальных условиях.
На основании приведенных данных определяют состав и объем продуктов сгорания 1 кг горючего вещества.
Например, чтобы определить объем и состав влажных продуктов сгорания 1 кг каменного угля, состоящего из 75,8 % С, 3,8 % Н, 2,8 % О, 1,1 % N, 2,5 % S, W = 3,8 %, A = 11,0 %.
Объем продуктов сгорания будет следующий, м 3 :
| Состав продуктов сгорания | СО2 | Н2О | N2 | SO2 |
| Углерод | 1,86 × 0,758 = 1,4 | – | 7 × 0,758 = 5,306 | – |
| Водород | – | 11,2 × 0,038 = 0,425 | 21 × 0,038 = 0,798 | – |
| Сера | – | – | 2,63 × 0,025 = 0,658 | 0,7 × 0,025 = 0,017 |
| Азот в горючем веществе | – | – | 0,8 × 0,011 = 0,0088 | – |
| Влага в горючем веществе | – | 1,24 × 0,03 = 0,037 | – | – |
| Сумма | 1,4 | 0,462 | 6,7708 – 0,0736 = 6,6972 | 0,017 |
Vп.с. = 1,4 + 0,462 + 6,6972 + 0,017 = 8,576 м 3 /кг.
Смесь газов
Количество и состав продуктов сгорания для смеси газов определяют по уравнению реакции горения компонентов, составляющих смесь. Например, горение метана протекает по следующему уравнению:
СН 4 + 2О 2 + 2 × 3,76N 2 = СО 2 + 2Н 2О + 7,52N 2
Согласно этому уравнению, при сгорании 1 м 3 метана получается 1 м 3 диоксида углерода, 2 м 3 паров воды и 7,52 м 3 азота. Аналогично определяют объем (в м 3 ) продуктов сгорания 1 м 3 различных газов:
| СО2 | Н2О | N2 | SO2 | |
| Водород | – | 1,0 | 1,88 | – |
| Окись углерода | 1,0 | – | 1,88 | – |
| Сероводород | – | 1,0 | 5,64 | 1,0 |
| Метан | 1,0 | 2,0 | 7,52 | – |
| Ацетилен | 2,0 | 1,0 | 9,54 | – |
| Этилен | 2,0 | 2,0 | 11,28 | – |
На основании приведенных цифр определяют состав и количество продуктов сгорания смеси газов.
Анализ продуктов сгорания, взятых на пожарах в различных помещениях, показывает, что в них всегда содержится значительное количество кислорода. Если пожар возникает в помещении с закрытыми оконными и дверными проемами, то пожар при наличии горючего может продолжаться до тех пор, пока содержание кислорода в смеси воздуха с продуктами сгорания в помещении не снизится до 14-16 % (об.). Следовательно, на пожарах в закрытых помещениях содержание кислорода в продуктах сгорания может быть в пределах от 21 до 14 % (об.). Состав продуктов сгорания во время пожаров в помещениях с открытыми проемами (подвал, чердак) показывает, что содержание в них кислорода может быть ниже 14 % (об.):
| СО | СО2 | О2 | |
| В подвалах | 0,15-0,5 | 0,8-8,5 | 10,6-19 |
| На чердаках | 0,1-0,6 | 0,3-4,0 | 16,0-20,2 |
По содержанию кислорода в продуктах сгорания на пожарах можно судить о коэффициенте избытка воздуха, при котором происходило горение.
Действие на организм человека
Степень токсичности веществ связана с их физической и химической природой. Взаимодействуя с организмом, продукты горения вызывают патологические синдромы.
Международная классификация болезней десятого пересмотра МКБ-10 определяет отравление продуктами горения кодом Т59 – «Токсическое действие других газов, дымов и паров».
По механизму действия на человека отравляющие компоненты в составе дыма делятся на пять групп.
Многие токсины, образующие в продуктах горения «универсальны», так как вызывают поражение сразу нескольких систем организма.
Первая помощь при отравлении
Симптомы интоксикации разными веществами могут отличаться, но принципы оказания первой помощи всегда одинаковые.
Большинство ядов поступает через дыхательные пути. Первое, что необходимо сделать при отравлении – прекратить поступление продуктов горения в организм. Для этого необходимо:
Острая интоксикация требуют оказания экстренной помощи. Действия при отравлении продуктами горения, следующие:
Некоторые ингаляционные отравления продуктами горения имеют период мнимого благополучия. Даже при отсутствии патологических симптомов, стоит внимательно следить за состоянием тех, кто может быть отравлен. При первых же признаках неблагополучия необходимо вызывать соответствующих специалистов.
Отравление продуктами горения у детей развивается быстрее, чем у взрослых. Это объясняется более высоким уровнем кислородного обмена. У малышей появляются жалобы на головную боль, сонливость, слезотечение, тошноту. При осмотре заметны изменения цвета кожи, учащение и затруднение дыхания, нарушения координации. Принципы оказания первой помощи для детей те же, что и для взрослых. При отсутствии специализированной медицинской помощи, пострадавшему ребенку угрожают необратимые изменения центральной нервной системы.
Источник: Пожаровзрывобезопасность веществ и материалов и средства их тушения: Справочник. Баратов А.Н., Корольченко А.Я. –М., 1990.
Гори-гори ясно: 10 вещей, которые нужно знать о том, как горит бензин
В двигателе внутреннего сгорания и вне его. Мы все что-то слышали про компрессию, богатую смесь, искру, лямбда-зонд и октановое число. Но «что-то слышать» и понимать, как это устроено — разные вещи. А есть ещё масса хитрых вопросов. Например, можно ли в бензине потушить окурок или рванёт? Правда ли, что от выстрела в бензобак начинается пожар? Как объяснить, что бензин легко загорается от малейшей искры, а дизельное топливо и зажигалкой не поджечь? И почему бензин портит дизельный движок, а дизель — бензиновый? Мы постараемся максимально ответственно и вдумчиво ответить на эти вопросы и развеять кое-какие мифы. Не зря же специализируемся на свечах зажигания.
1. Горит бензин или его пары?
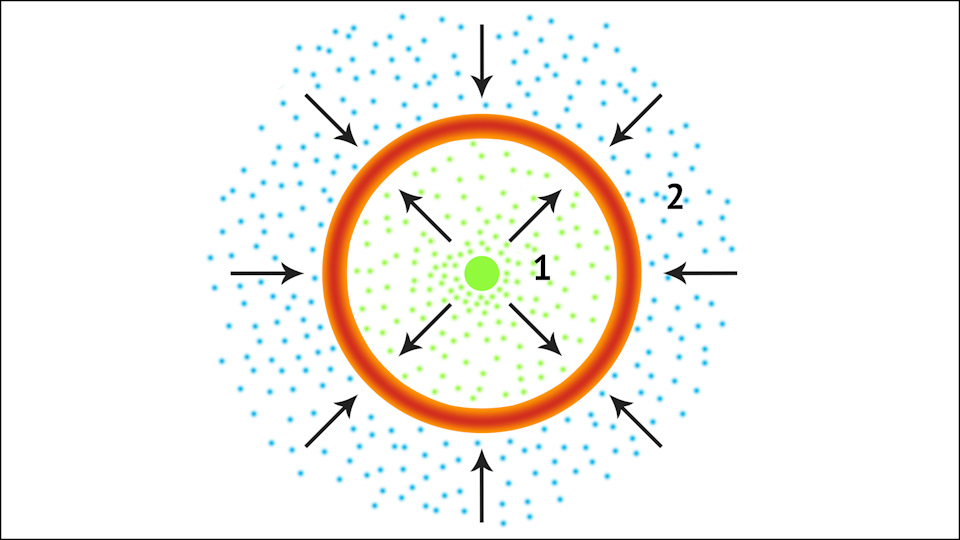
Горит смесь паров бензина и кислорода, содержащегося в воздухе. Поэтому если вы слышали байку о том, как кто-то тушил в полной канистре бензина сигаретные бычки — это не байка, а вполне себе правда. Хотя это очень опасно и делать так мы не советуем. Опасно потому, что горючие пары у поверхности бензина есть всегда, если только он не охлажден до температуры ниже –40°C.
Концентрация бензина в воздухе, при которой смесь становится пожароопасной, имеет четкое минимальное и максимальное значение: от 0,8% до 8,0%. Если бензина в воздухе меньше, то смесь не загорится из-за нехватки топлива. Если больше, то тоже не загорится, но уже из-за нехватки достаточного для поддержания реакции количества кислорода.
Важно не путать пары и ничтожно малые капли бензина. Капля — это тоже жидкость, просто с точки зрения человека в крохотном объеме. Если пшикнуть из баллончика на пламя чем-нибудь горючим, то гореть будет не аэрозоль из мельчайших капель вещества, а испарения, которые окружают каждую каплю.
Красное кольцо — это и есть место горения, где пары бензина (1) соединяются с кислородом (2). А сама капля бензина (зеленый круг) не горит, а лишь испускает пары. Источник (здесь и далее, если не указано иное): NGK Spark Plugs
Горение паров бензина — это сложный окислительный процесс, при котором молекулы бензина распадаются, углерод и водород из топлива соединяются с кислородом из воздуха под действием высокой температуры, происходит выделение энергии. При полном сгорании бензин разлагается на воду (H2O) и монооксид углерода (CO). Это в теории, на деле всё сложнее, а сопутствующих соединений образуется больше из-за того, что воздух состоит из целого коктейля элементов, а не одного кислорода.
К сожалению, таких видео в интернете масса. А всё из-за непонимания того, что горят именно пары бензина, которые при заправке буквально струёй вырываются из горловины бака.
Всё описанное, заметим, справедливо для горения бензина на открытом воздухе. В двигателе внутреннего сгорание дело происходит иначе.
2. Что происходит с бензином в двигателе внутреннего сгорания
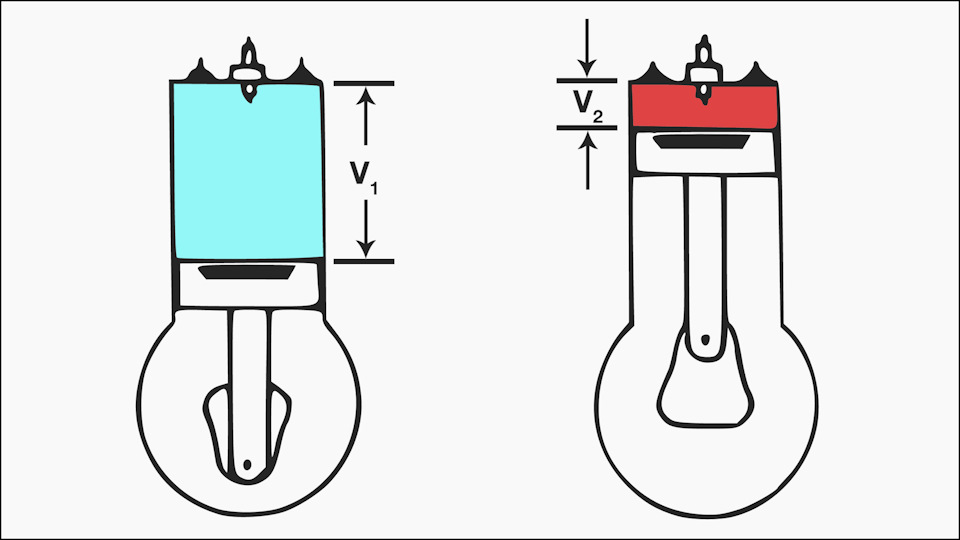
Сам по себе бензин горит очень медленно — это можно увидеть, поджигая маленькую лужицу топлива на улице. Чтобы ускорить его горение и, соответственно, выработку энергии, необходимо увеличить давление смеси. Двигатель внутреннего сгорания в начале каждого такта открывает клапан, в цилиндр впрыскивается смесь бензина и воздуха в нужной пропорции, а затем поршень, поднимаясь вверх, сжимает смесь, увеличивая её давление. Разницу в объеме при поднятом и опущенном поршне называют степенью сжатия, и в бензиновых ДВС она составляет 8–14:1. То есть поршень сжимает объем топливо-воздушной смеси в 8–14 раз.
Отношение между максимальным объёмом V1 и минимальным объёмом V2 зовётся степенью сжатия
Когда поршень находится в крайнем положении и смесь сжата максимально, свеча зажигания производит искру с температурой 10 000 °C. Если компрессия (давление) ниже необходимой, упадет мощность двигателя. Если выше, начнется детонация (об этом дальше).
От искры зажигания топливовоздушная смесь загорается, пламя распространяется от свечи зажигания по всему объёму цилиндра. Дальше происходят химические реакции, выделение газов и движение поршня вниз — с этим процессом автомобилисты хорошо знакомы.
Итак, для горения бензина необходим воздух. Сколько? Идеальное соотношение составляет 1:14,7, т. е. для полного сжигания 1 кг бензина необходимо 14,7 кг воздуха. Бензино-воздушная смесь с таким идеальным соотношением называется стехиометрической. В двигателях внутреннего сгорания это соотношение может быть чуточку больше или меньше. В таких случаях топливо-воздушную смесь называют богатой или бедной в зависимости от количества паров бензина в ней. Богатая смесь даст большую мощность двигателю, зато бедная обеспечит экономичность. За регулировку обогащения смеси топливом отвечает лямбда-зонд, анализирующий количество кислорода в выхлопных газах.
3. Что может быть не так с горением бензина в двигателе
Давление в цилиндре и высокая температура искры — это еще не гарантия, что бензин в двигателе будет загораться в нужный момент и сгорать с нужной скоростью. Огромную роль в этом процессе играют свечи и катушка зажигания.
Первая ситуация, когда ДВС работает неправильно, — детонация. Детонация есть самопроизвольное возгорание топливовоздушной смеси взрывного характера вследствие превышения некоего порога сжатия и температуры, происходящее после возникновения искры зажигания (это важный момент). В этом случае, пока топливовоздушная смесь начинает плавно гореть от свечи, где-то в другой точке объема самопроизвольно возникает еще один очаг возгорания. Фронт пламени при детонации в цилиндре распространяется со скоростью в 100 раз выше, чем при нормальной работе двигателя. Взрывная волна оказывает сильнейшую ударную нагрузку на цилиндр и буквально выгрызает в поршне каверны. Хуже того, микровзрывы разрушают свечу и стенки цилиндра и гнут шатуны. Как это происходит, можно посмотреть в нашем видео.
Детонация, помимо прочего, возникает из-за использования бензина с октановым числом ниже допустимого в конкретном двигателе — в таком топливе стойкость к детонации ниже, чем у выскооктанового бензина (об этом ниже). Также бывает виноват перегретый двигатель или высокая нагрузка при низких оборотах.
Есть ещё одно неприятное явление, по последствиям похожее на детонацию, — калильное зажигание. Во время него смесь в цилиндре воспламеняется ещё до появления искры свечи, например, от перегретого нагара на клапанах или поврежденной и тоже перегревшейся из-за неправильной установки свечи. Мы уже писали отдельный пост о калильном зажигании — обратите внимание. В лучшем случае оно приведет к сгоранию электрода свечи или повреждению её изолятора, а в худшем — к прогоранию поршней, поршневых колец и маслосъёмных колпачков, то есть к серьёзному ремонту двигателя.
Результат длительной езды с детонацией — расплавление поршня и колец. Источник: MrAliev / DRIVE2
Другая частая проблема, связанная с «убитыми» или некачественными свечами, — пропуски зажигания. Свеча либо вовсе не вырабатывает искру, либо зазор между электродами уменьшается из-за нагара и искра получается слабой, либо изношенная катушка зажигания уже не может выдавать необходимое напряжение. Пропуски дают о себе знать сильной вибрацией двигателя на холостом ходу и падением мощности авто. Остатки несгоревшего из-за отсутствия искры топлива попадают в нейтрализатор, воспламеняются там и сжигают его, закупоривая соты.
Расплавленный нейтрализатор. Это ещё ничего, в особо тяжелых случаях расплав закупоривает почти все соты. Источник: HelpAutoKiev / DRIVE2
Тут повторим мысль, уже однажды звучавшую в этом представительстве: иридиевые и платиновые свечи зажигания — это не очередной способ вытянуть побольше денег из автолюбителей, а физика. Тонкий стержень из тугоплавкого иридия в центральном электроде значительно лучше самоочищается от нагара в сравнении с толстым никелевым сердечником. Простая свеча с толстым электродом может быстро покрыться нагаром из-за некачественного бензина, расход топлива увеличится, начнутся пропуски зажигания. Кроме того, чем тоньше электрод, тем проще вызвать искру — снижается нагрузка на катушку зажигания. Иридиевая свеча хоть и стоит дороже обычной, но в течение срока службы демонстрирует меньший расход топлива и вредных выбросов. Нет, это не методичка из PR-отдела, а исследование журнала «За рулём».
Свеча с иридиевым сердечником (слева; Laser Iridium) и с никелевым (справа) — обе NGK Spark Plugs
Платиновые напайки на электродах создают стойкость к коррозии и эрозии. То есть зазор между электродами практически не будет меняться в течение срока службы свечи, а значит, значительно снижается шанс возникновения пропусков зажигания. Платиновые и иридиевые свечи не вечные, но проходят они в среднем в 3-4 раза больше обычных (порядка 100 тыс. км), после чего требуют замены. При небольших ежегодных пробегах есть шанс, что после покупки нового автомобиля с иридиевыми свечами вы вообще их никогда не поменяете, а скорее продадите машину.
Свеча NGK с едва заметными светлыми платиновыми напайками на концах электродов — такого количества драгметалла вполне достаточно. Источник: mikelz / DRIVE2
4. Почему важно октановое число и можно ли на нём экономить
Есть много мифов, появившихся вследствие непонимания смысла октанового числа бензина. Мы постараемся последовательно их развеять. Октановое число характеризует стойкость топлива к детонации — и ничто другое. Ни качество и чистоту, ни температуру горения, ни абстрактную «эффективность» — только стойкость к детонации.
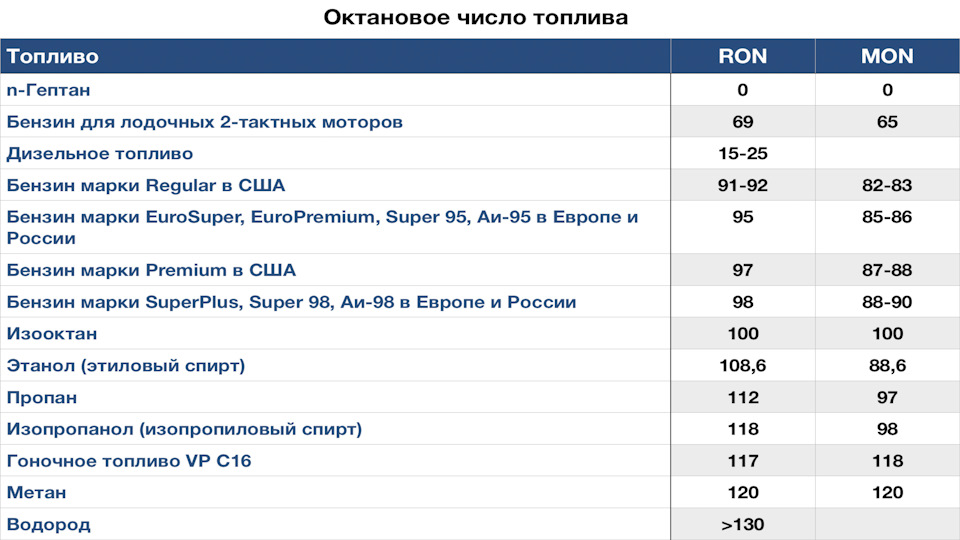
Что фактически значит число 95 в марке автомобильного бензина? Оно значит, что топливовоздушная смесь конкретного бензина имеет стойкость к детонации такую же, как смесь из 95% изооктана и 5% гептана. Изооктан — углеводород, принятый за образец стойкости к детонации (октановое число 100), а гептан, наоборот — образец склонности к детонации (октановое число 0). На их комбинировании и построена октановая шкала.
Тогда что такое бензин с октановым числом выше 100, если 100-процентный изооктан является эталоном? Это бензин, который с помощью присадок сделали более стойким к детонации, чем чистый изооктан; такой используется в гоночных автомобилях (у авиационных бензинов октановое число тоже может быть выше 100, но у них своя шкала детонационной стойкости). Главным образом этого позволяет достичь добавление тетраэтилсвинца, однако применяются также эфиры МТБЭ и ЭТБЭ, толуол и проч. Интересно, что они во-первых, делают топливо дороже, а во-вторых, в большинстве своём вредны для окружающей среды и человека. Так, тетраэтилсвинец до конца XX века добавляли в весь автомобильный бензин для повышения его октанового числа, но затем присадка попала под запрет из-за токсичности (а бензин стал неэтилированным).
Повторим же: чем выше октановое число, тем более бензин стоек к детонации. В форсированных двигателях с высокой степенью сжатия низкооктановый бензин начинает детонировать во время зажигания со всеми описанными выше последствиями для двигателя. Проще говоря, если у вас современный немецкий турбомотор и к нему приложена рекомендация заправляться Аи-98 (а в случае острой необходимости Аи-95), то заправка Аи-92 очень скоро приведёт к детонации и порче очень дорогого двигателя.
RON — исследовательский метод, согласно которому в России и обозначается марка бензина, по условиям вычисления похож на езду по трассе (буква «И» в маркировке бензина как раз от слова «исследовательский», а «А» означает «автомобильный»). MON — моторный метод, похожий на эксплуатацию в городе
А что насчёт заправки высокооктановым топливом атмосферного движка, настроенного под Аи-92 или даже ниже? Никакой детонации, естественно, не будет — будет другая проблема. Высокооктановое топливо горит медленнее, чем низкооктановое. Какой-нибудь Аи-98 просто не успеет полностью сгореть в цилиндре, и огонь пройдёт сквозь выпускной клапан в коллектор, пожжёт катализатор, а на высоких оборотах доберется и до глушителя.
5. Безнин невозможно поджечь сигаретой
А теперь немного о несерёзном. Трюк с гашением в ведре бензина работает только с сигаретой, провернуть тот же фокус с горящей спичкой не получится. Вернее, фокус получится, но совсем другой. Если оставить сигарету в покое и не затягиваться, она будет не гореть, а тлеть без образования газофазного пламени (то есть огня), необходимого для воспламенения бензина. Чисто теоретически, неудачно брошенная в лужу бензина сигара может испустить достаточно искр, чтобы поджечь пары топлива, — это единственное оправдание популярному киноходу с поджиганием бензина таким образом.
А вот с негаснущей на ветру зажигалкой типа Zippo такой трюк сработает почти наверняка (как в конце «Крепкого орешка 2»). Поэтому курение рядом с заправляющимся автомобилем опасно, но не фатально (всё равно не делайте этого), а попытка подсветить бензобак зажигалкой абсолютно гарантированно закончится пожаром.
Коротко и наглядно — бензин сигаретным бычком не зажечь. Но не повторяйте это дома!
6. Бензобак в автомобиле так просто не взрывается
Автомобиль, как на этом фото, может загореться даже во время стоянки — например, из-за короткого замыкания или даже поджога, — и со временем взорваться, но сначала он порядочно прогорит. Источник: Les Chatfield / Flickr
Демонстрация того, что как в канистру с бензином не стреляй, а взрыва не выйдет:
Но хватит о кино и мифах — возвращаемся к серьёзному разговору.
7. Бензин при аварии может загореться
Если не считать автомобили с некачественным ГБО, по-настоящему эффектно взрываются только… электромобили :
Тем не менее, пожар может начаться просто от того, что бензин попал на какой-то узел, куда он попадать не должен. Искра не нужна, достаточно очень высокой температуры поверхности, чтобы началось самовоспламенение бензина. Физика безжалостна: температура, при нагревании до которой пары бензина загораются сами, начинается с 250°C. Если бензин попадет в выпускной коллектор или в катализатор, который разогревается до 500-600°C (если крутить движок), топливо мгновенно вспыхнет. То же самое произойдет при соприкосновении топлива с тормозными дисками (300-400°C при торможении «в пол»).
В тяжелых ДТП, когда автомобиль буквально разрывает на части, нарушается целостность топливной системы, а то и самого бензобака, бензин быстро вытекает наружу и попадает на раскаленные узлы автомобиля. Далее происходит самовоспламенение испаряющегося топлива и начинается сильный пожар. А уж если после аварии и разлития горючего что-то под капотом заискрит…
8. Дизельное топливо при аварии горит гораздо хуже
При аварии дизельное топливо точно так же может растечься по раскаленным деталям автомобиля и по дороге, но воспламениться даже от искр ему не позволит химия. Дизель относится к тяжелым видам топлива с низкой летучестью, он имеет длинную углеродную цепочку, потому испаряется очень неохотно. Бензин, напротив, очень летуч — уже при температуре –40°C он начинается испаряться достаточно для того, чтобы загореться. Этот порог называется температурой вспышки. Даже в мороз достаточно любой искры, чтобы бензин заполыхал огнем. А вот температура вспышки у дизеля составляет аж +62°C. Случайные искры не смогут разогреть дизельную лужу до такой степени, чтобы та начала испаряться и гореть. Чтобы солярка загорелась на воздухе, ее нужно нагреть до температуры вспышки, например, газовой горелкой, усилив испарение. В зависимости от силы огня и количества дизеля в ёмкости топливо прогреется через 15-20 секунд и тогда наконец загорится.
9. Что будет, если дизельный автомобиль заправить бензином
Из-за свойств дизельного топлива дизельвоздушная смесь в цилиндрах воспламеняется сама, без участия свечи зажигания, при увеличении давления и сопутствующего ему увеличения температуры. С бензовоздушной смесью, как мы сказали выше, такое тоже возможно, хотя и с негативными последствиями. Тогда почему бы не залить бензин в дизельный ДВС? Тут основная проблема заключается в параметрах топлива, под которые спроектирован двигатель. Действительно, дизельный движок, в зависимости от степени технологичности (чем старше и проще, тем лучше) даже сможет немного поработать на бензине. Но из-за разницы в скорости воспламенения и горения бензина и дизеля двигатель будет подвергаться огромным разрушительным нагрузкам.
В современных движках на тяжелом топливе дизель впрыскивается в цилиндр не один, а несколько раз за один ход поршня. Сначала происходит предвпрыск небольшого количества топлива, которое загорается еще до того, как поршень достиг вершины хода. Затем, когда поршень достиг верхней мёртвой точки, и достигнуто максимальное сжатие воздуха в камере сгорания, впрыскивается оставшаяся часть дизеля. Двойной впрыск обеспечивает надежное возгорание и равномерное выделение газов, необходимых для толкания поршня вниз. Этапов впрыска в рамках одного такта двигателя может быть два, а может и все десять, тут уж как будет спроектирован двигатель.
Случайный залив бензина в дизельный авто на крупных сетевых заправках часто кончается относительно благополучно: приезжает сотрудник топливной компании и сливает бензин из бака и топливной системы. Источник: priZrak495 / DRIVE2
А вот с бензином ситуация другая. Во время предвпрыска бензин, смешанный с остатками дизеля из топливного бака, не загорится. Он понизит цетановое число солярки. Чем ниже цетановое число, тем медленней воспламеняется топливо и тем интенсивней сгорает. Когда поршень достигнет высшей точки и произойдет впрыск оставшейся части «бензинодизеля», смесь наконец загорится от высокого давления и температуры. При огромной степени сжатия бензин не будет плавно гореть, пока поршень будет двигаться вниз — он буквально сдетонирует, вызвав сильнейшую ударную нагрузку на цилиндр. Со стороны детонация бензина в дизельном ДВС звучит как удары маленькими молоточками по металлическим деталям двигателя. На самом деле это приглушенные взрывы бензина. От постоянных взрывов и ударных нагрузок портятся поршни, в цилиндре образуются микротрещины, сильно изнашивается цепь/ремень ГРМ. Чем меньше в топливной смеси осталось дизеля и чем больше в ней бензина, тем сильнее детонанция.
10. Что будет, если в бензиновый двигатель залить дизель
Если же залить дизель в бензиновый автомобиль, то практически сразу начнутся пропуски зажигания — дизелю не хватит давления и температуры в цилиндрах, чтобы стабильно самовоспламеняться, а искрой от свечи его не поджечь. Так как солярка тяжелее бензина, она сразу опустится на дно и попадёт в топливную систему.
Цилиндры наполнятся несгоревшим дизелем, топливо пойдёт в выпускной коллектор, из выхлопной трубы повалит дымок. Мотор «закашляет», потеряет мощность и вскоре заглохнет. Скорее всего, отделаетесь «малой кровью» — чисткой топливной системы и фильтров, забитых содержащимся в дизеле парафином.
Коротко о главном
Рекомендации по использованию бензинового автомобиля простые: заправляйтесь на проверенных заправках топливом с рекомендованным октановым числом, следите за свечами и, пожалуйста, никогда не пытайтесь подсветить бензобак зажигалкой!
Остались вопросы? Задавайте — постараемся ответить.