Укажите с чем связаны полиморфные превращения железа ответ
Полиморфизм железа
Дата добавления: 2015-07-09 ; просмотров: 10047 ; Нарушение авторских прав
Полиморфизм. Некоторые металлы в зависимости от температуры могут существовать в различных кристаллических формах. Это явление называется полиморфизм или аллотропия, а различные кристаллические формы одного вещества называются полиморфными модификациями. Процесс перехода от одной кристаллической формы к другой называется полиморфным превращением. Полиморфные превращения протекают при определенной температуре.
Полиморфные модификации обозначают строчными греческими буквами α, β, γ, δ и т. д., причем α соответствует модификации, существующей при наиболее низкой температуре. Полиморфизм характерен для железа, олова, кобальта, марганца, титана и некоторых других металлов.
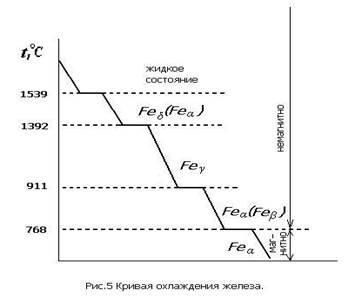
Важное значение имеет полиморфизм железа. На рис. 5 изображена кривая охлаждения железа.
Полиморфные превращения характеризуются горизонтальными участками на кривой охлаждения, так как при них происходит полная перекристаллизация металла. До 911°С устойчиво Feα, имеющее кубическую объемноцептрированную решетку. В интервале 911…1392 °С существует Feγ с кубической гранецентрированной кристаллической решеткой.
При 1392…1539 °С вновь устойчиво Feα. Часто высокотемпературную модификацию Feα обозначают Feδ. Остановка на кривой охлаждения при 768 °С связана не с полиморфным превращением, а с изменением магнитных свойств. До 768 °С железо магнитно, а выше — немагнитно.
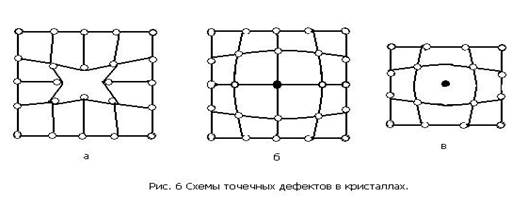
Дефекты кристаллического строения. Реальный металлический кристалл всегда имеет дефекты кристаллического строения. Они подразделяются на точечные, линейные и поверхностные (рис. 6).
Точечные дефекты малы во всех трех измерениях. К точечным дефектам относятся вакансии, представляющие собой узлы кристаллической решетки в которых отсутствуют атомы (рис. 6, а), а также замещенные атомы примеси (рис. 6, б) и внедренные атомы (рис. 6, в) которые могут быть как примесными, так и атомами основного металла.
Точечные дефекты вызывают местные искажения кристаллической решетки, которые затухают достаточно быстро по мере удаления от дефекта.
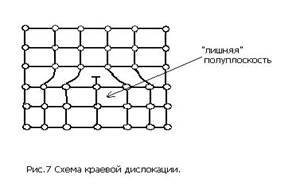
Линейные дефекты имеют малые размеры в двух измерениях и большую протяженность в третьем. Эти дефекты называют дислокациями. Краевая дислокация (рис. 7) представляет собой искажение кристаллической решетки, вызванное наличием «лишней» атомной полуплоскости.
Поверхностные дефекты малы только в одном измерении. К ним относятся, например, границы между отдельными зернами или группами зерен.
Железо, его совйства, полиморфные превращения чистого железа
Желе́зо — элемент побочной подгруппы восьмой группы четвёртого периода периодической системы химических элементов Д. И. Менделеева с атомным номером 26. Обозначается символом Fe (лат. Ferrum). Один из самых распространённых в земной коре металлов (второе место после алюминия).Простое вещество железо (CAS-номер: 7439-89-6) — ковкий металл серебристо-белого цвета с высокой химической реакционной способностью: железо быстро корродирует при высоких температурах или при высокой влажности на воздухе. В чистом кислороде железо горит, а в мелкодисперсном состоянии самовозгорается и на воздухе.Собственно, железом обычно называют его сплавы с малым содержанием примесей (до 0,8 %), которые сохраняют мягкость и пластичность чистого металла. Но на практике чаще применяются сплавы железа с углеродом: сталь (до 2,14 вес. % углерода) и чугун (более 2,14 вес. % углерода), а также нержавеющая (легированная) сталь с добавками легирующих металлов (хром, марганец, никель и др.). Совокупность специфических свойств железа и его сплавов делают его «металлом № 1» по важности для человека.В природе железо редко встречается в чистом виде, чаще всего оно встречается в составе железо-никелевых метеоритов. Распространённость железа в земной коре — 4,65 % (4-е место после O, Si, Al[2]). Считается также, что железо составляет бо́льшую часть земного ядра.
Свойства: Оно пластично, легко куется как в холодном, так и нагретом состоянии, поддается прокатке, штамповке и волочению. Способность растворять углерод и других элементы служит основой для получения разнообразных железных сплавов. Железо может существовать в виде двух кристаллических решеток: α- и γ-объемноцентрированной кубической (ОЦК) и гранецентрированной кубической (ГЦК). Ниже 910°С устойчиво α-Fe с ОЦК-решеткой (а = 2,86645Å при 20 °С). Между 910 °С и 1400°С устойчива γ-модификация с ГЦК-решеткой (а = 3,64Å). Выше 1400°С вновь образуется ОЦК-решетка δ-Fe (a = 2,94Å), устойчивая до температуры плавления (1539 °С). α-Fe ферромагнитно вплоть до 769 °С (точка Кюри). Модификации γ-Fe и δ-Fe парамагнитны.
Некоторые металлы (железо, титан, кобальт, цирконий и др.) при разных температурах имеют различные кристаллические решетки. Такое явление называется полиморфизмом или аллотропией. Процесс перехода из одного кристаллического строения в другое называется полиморфным (аллотропическим) превращением.
Строение, получающееся в результате полиморфного превращения, называется аллотропической формой. Аллотропическая форма, устойчивая при более низкой температуре, обозначается индексом a, при более высокой – b, g и т. д.
Температура, при которой происходит переход решетки из одного вида в другой, называется температурой полиморфного превращения или температурой перекристаллизации. При этом изменяются свойства металла (плотность, теплопроводность, теплоемкость и др.).
Аллотропические превращения при нагревании происходят с поглощением тепла, а при охлаждении – с его выделением. Как при нагревании, так и при охлаждении аллотропические превращения происходят с некоторым запаздыванием. Так, температура превращения a-модификации в b-модификацию, происходящего при нагревании, будет всегда выше температуры превращения b в a, происходящего при охлаждении. Такое явление называется гистерезисом.
До температуры 1539 °С происходит охлаждение жидкого железа. При 1539 °С на кривой охлаждения появляется площадка. При этой температуре железо затвердевает, и выделяется скрытая теплота кристаллизации. По окончании кристаллизации и до температуры 1392 °С железо имеет объемно-центрированную кубическую решетку (Fea ).При 1392 °С на кривой появляется вторая площадка, связанная с аллотропическим превращением a-железа (Fea) в g-железо (Feg), имеющее гранецентрированную кубическую решетку.При аллотропическом превращении исчезают старые зерна и появляются новые. Такое превращение аналогично процессу кристаллизации: вначале образуются зародыши, а затем идет рост зерен новой модификации. Такое превращение является перекристаллизацией. Следующая площадка наблюдается на кривой охлаждения при температуре 911 °С по причине превращения Feg в Fea. Кристаллическая решетка превращается из гранецентрированной опять в объемно-центрированную кубическую, которая сохраняется до самых низких температур.Площадка на кривой охлаждения, соответствующая температуре 768 °С, связана не с перестройкой кристаллической решетки, а с перестройкой электронных оболочек атомов и изменением магнитных свойств. Ниже 768 °С железо магнитно, а выше – немагнитно.Иногда немагнитное железо Fea называют Feβ, а высокотемпературную модификацию Fea (в интервале 1392…1539 °С) – Fed. Полиморфные превращения протекают как в чистых металлах, так и в сплавах.
Fe-Fe3C
Первичная кристаллизация сплавов системы железо-углерод начинается по достижении температур, соответствующих линии ABCD (линии ликвидус), и заканчивается при температурах, образующих линию AHJECF (линию солидус).При кристаллизации сплавов по линии АВ из жидкого раствора выделяются кристаллы твердого раствора углерода в α-железе (δ-раствор). Процесс кристаллизации сплавов с содержанием углерода до 0,1 % заканчивается по линии АН с образованием α (δ)-твердого раствора. На линии HJB протекает перитектическое превращение, в результате которого образуется твердый раствор углерода в γ-железе, т. е. аустенит. Процесс первичной кристаллизации сталей заканчивается по линии AHJE.При температурах, соответствующих линии ВС, из жидкого раствора кристаллизуется аустенит. В сплавах, содержащих от 4,3 % до 6,67 % углерода, при температурах, соответствующих линии CD, начинают выделяться кристаллы цементита первичного. Цементит, кристаллизующийся из жидкой фазы, называется первичным. B точке С при температуре 1147°С и концентрации углерода в жидком растворе 4,3 % образуется эвтектика, которая называется ледебуритом. Эвтектическое превращение с образованием ледебурита можно записать формулой ЖР4,3Л[А2,14+Ц6,67]. Процесс первичной кристаллизации чугунов заканчивается по линии ECF образованием ледебурита.Таким образом, структура чугунов ниже 1147°С будет: доэвтектических – аустенит+ледебурит, эвтектических – ледебурит и заэвтектических – цементит (первичный)+ледебурит. Превращения, происходящие в твердом состоянии, называются вторичной кристаллизацией. Они связаны с переходом при охлаждении γ-железа в α-железо и распадом аустенита.Линия GS соответствует температурам начала превращения аустенита в феррит. Ниже линии GS сплавы состоят из феррита и аустенита.Линия ЕS показывает температуры начала выделения цементита из аустенита вследствие уменьшения растворимости углерода в аустените с понижением температуры. Цементит, выделяющийся из аустенита, называется вторичным цементитом. В точке S при температуре 727°С и концентрации углерода в аустените 0,8 % образуется эвтектоидная смесь состоящая из феррита и цементита, которая называется перлитом. Перлит получается в результате одновременного выпадения из аустенита частиц феррита и цементита. Процесс превращения аустенита в перлит можно записать формулой А0,8П[Ф0,03+Ц6,67].Линия PQ показывает на уменьшение растворимости углерода в феррите при охлаждении и выделении цементита, который называется третичным цементитом. Следовательно, сплавы, содержащие менее 0,008% углерода (точкаQ), являются однофазными и имеют структуру чистого феррита, а сплавы, содержащие углерод от 0,008 до 0,03% – структуру феррит+цементит третичный и называются техническим железом.Доэвтектоидные стали при температуре ниже 727ºС имеют структуру феррит+перлит и заэвтектоидные – перлит+цементит вторичный в виде сетки по границам зерен. В доэвтектических чугунах в интервале температур 1147–727ºС при охлаждении из аустенита выделяется цементит вторичный, вследствие уменьшения растворимости углерода(линия ES). По достижении температуры 727ºС (линия PSK) аустенит, обедненный углеродом до 0,8% (точка S), превращаясь в перлит. Таким образом, после окончательного охлаждения структура доэвтектических чугунов состоит из перлита, цементита вторичного и ледебурита превращенного (перлит+цементит).Структура эвтектических чугунов при температурах ниже 727ºС состоит из ледебурита превращенного. Заэвтектический чугун при температурах ниже 727ºС состоит из ледебурита превращенного и цементита первичного.
Полиморфное превращение в железе.
Во многих металлах при изменении температуры происходит перегруппировка атомов, кристаллическая решетка одного вида переходит в другой. Это явление называется аллотропией или полиморфизмом, а различные кристаллические формы одного вещества называют полиморфными модификациями.
Полиморфные модификации обозначаются греческими буквами α, β, γ, δ и т.д., причем α соответствует модификации, существующей при наиболее низкой температуре.
Суть полиморфного превращения заключается в том, что при нагревании в твердом металле возникают новые центры кристаллизации, что приводит к образованию новой решетки. При формировании кристаллической решетки температура остается постоянной, так как при нагревании формирование происходит с поглощением тепла, а при охлаждении – с выделением тепла. Полиморфное превращение – это кристаллизационный процесс и на кривой нагревания (охлаждения) изображается горизонтальной линией.
В результате полиморфного превращения образуются зерна, имеющие другой размер и форму по сравнению с исходными зернами. При переходе из одной полиморфной модификации в другую меняются все свойства металлов.
Важнейшее значение в технике имеют полиморфные превращения в железе (Рис. 5). Железо может существовать в нескольких модификациях.
Рисунок 5. Кривая охлаждения чистого железа.
До температуры 1539ºС железо остается жидким. При температуре 1539ºС начинается кристаллизация и образуется δ-железо, имеющее кубическую объемно-центрированную решетку. Между температурами 1400 и 910ºС происходит перестройка этой решетки в новую модификацию – γ-железо с образованием кубической гранецентрированной решетки. Ниже температуры 910ºС железо переходит в новую форму – α-железо с кубической объемно-центрированной решеткой. При температуре 768ºС происходит последняя температурная остановка с образованием магнитной формы α-железа, в которой сохраняется объемно-центрированная решетка.
Подобные полиморфные превращения происходят и с другими металлами, но при иных критических температурах.
Контрольная работа 1 Вариант 7
Опишите явление полиморфизма в приложении к железу. Какое практическое значение оно имеет?
Многие металлы в зависимости от температуры могут существовать в разных кристаллических формах или, как их называют, в разных полиморфных модификациях. В результате полиморфного превращения атомы кристаллического тела, имеющие решетку одного типа, перестраиваются таким образом, что образуется кристаллическая решетка другого типа. Полиморфную модификацию, устойчивую при более низкой температуре, для большинства металлов принято обозначать α, а при более высокой – β, затем γ и т. д.
При полиморфном превращении кристаллы (зерна) новой полиморфной формы растут в результате неупорядоченных, взаимно связанных переходов атомов через границу фаз. Отрываясь от решетки исходной фазы (например, β), атомы по одиночке или группами присоединяются к решетке новой фазы (α), и, как следствие этого, граница зерна α-модификации передвигается в сторону зерна β-модификации, «поедая» исходную фазу. Зародыши новой модификации наиболее часто возникают на границах зерен исходных кристаллитов. Вновь образующиеся кристаллы закономерно ориентированы по отношению к кристаллам исходной модификации.
Используя явление полиморфизма, можно упрочнять и разупрочнять сплавы при помощи термической обработки.
Железо имеет две полиморфные модификации α и γ. Модификация α-железа существует при температурах ниже 910 °С и выше 1392 °С. В интервале температур 1392–1539 °С α-железо нередко обозначают как δ-железо.
Кристаллическая решетка α-железа – объемно центрированный куб с периодом решетки 0,28606 нм. До температуры 768 °С α-железо магнитно (ферромагнитно).
γ-железо существует при температуре 910–1392 °С; оно парамагнитно. Кристаллическая решетка γ-железа гранецентрированная кубческая (а = 0,3645 нм при 910 °С).
Как изменяются свойства деформированного металла при нагреве, какие процессы происходят при этом?
Деформированный металл по сравнению с недеформированным имеет повышенный запас энергии и находится в неравновесном, термодинамически неустойчивом состоянии. В таком металле даже при комнатной температуре могут самопроизвольно протекать процессы, приводящие его в более устойчивое состояние. Однако, если деформированный металл нагреть, то скорость этих процессов возрастает. Небольшой нагрев (для железа 300-400°С) ведет к снятию искажений кристаллической решетки, но микроструктура остается без изменений, зерна по-прежнему вытянуты. Прочность при этом несколько; снижается, а пластичность повышается. Такая обработка называется возвратом или отдыхом.
При дальнейшем повышении температуры подвижность атомов возрастает и среди вытянутых зерен идет интенсивное зарождение и рост новых равноосных свободных от напряжений зерен. Зародыши новых зерен возникают в участках с наиболее искаженной кристаллической решеткой, с повышенным уровнем свободной энергии, термодинамически наименее устойчивых. Новые зерна растут за счет старых, вытянутых, до их столкновения друг с другом и до полного исчезновения вытянутых зерен. Это явление называется рекристаллизацией (первичной).
Рекристаллизация является диффузионным процессом и протекает неравномерно, одни зерна зарождаются и растут раньше, другие позднее. После рекристаллизации металл состоит из новых равноосных зерен. Более высокий нагрев приводит к развитию собирательной рекристаллизации, т. е. к росту одних рекристаллизованных зерен за счет других, более мелких. Чем выше температура нагрева, тем интенсивнее идет собирательная рекристаллизация, так как с повышением температуры диффузионные процессы протекают быстрее и создают условия для образования крупнозернистого металла.
Вычертите диаграмму состояния железо – карбид железа, укажите структурные составляющие во всех областях диаграммы, опишите превращения и постройте кривую охлаждения (с применением правила фаз) для сплава, содержащего 0,7% С. Какова структура этого сплава при комнатной температуре и как такой сплав называется?
Первичная кристаллизация сплавов системы железо-углерод начинается по достижении температур, соответствующих линии ABCD (линии ликвидус), и заканчивается при температурах, образующих линию AHJECF (линию солидус).
При кристаллизации сплавов по линии АВ из жидкого раствора выделяются кристаллы твердого раствора углерода в α-железе (δ-раствор). Процесс кристаллизации сплавов с содержанием углерода до 0,1 % заканчивается по линии АН с образованием α (δ)-твердого раствора. На линии HJB протекает перитектическое превращение, в результате которого образуется твердый раствор углерода в γ-железе, т. е. аустенит. Процесс первичной кристаллизации сталей заканчивается по линии AHJE.
При температурах, соответствующих линии ВС, из жидкого раствора кристаллизуется аустенит. В сплавах, содержащих от 4,3 % до 6,67 % углерода, при температурах, соответствующих линии CD, начинают выделяться кристаллы цементита первичного. Цементит, кристаллизующийся из жидкой фазы, называется первичным. B точке С при температуре 1147°С и концентрации углерода в жидком растворе 4,3 % образуется эвтектика, которая называется ледебуритом. Эвтектическое превращение с образованием ледебурита можно записать формулой ЖР4,3Л[А2,14+Ц6,67]. Процесс первичной кристаллизации чугунов заканчивается по линии ECF образованием ледебурита.
Таким образом, структура чугунов ниже 1147°С будет: доэвтектических – аустенит+ледебурит, эвтектических – ледебурит и заэвтектических – цементит (первичный)+ледебурит.
Превращения, происходящие в твердом состоянии, называются вторичной кристаллизацией. Они связаны с переходом при охлаждении γ-железа в α-железо и распадом аустенита.
Линия GS соответствует температурам начала превращения аустенита в феррит. Ниже линии GS сплавы состоят из феррита и аустенита.
Линия ЕS показывает температуры начала выделения цементита из аустенита вследствие уменьшения растворимости углерода в аустените с понижением температуры. Цементит, выделяющийся из аустенита, называется вторичным цементитом.
В точке S при температуре 727°С и концентрации углерода в аустените 0,8 % образуется эвтектоидная смесь состоящая из феррита и цементита, которая называется перлитом. Перлит получается в результате одновременного выпадения из аустенита частиц феррита и цементита. Процесс превращения аустенита в перлит можно записать формулой А0,8П[Ф0,03+Ц6,67].
Линия PQ показывает на уменьшение растворимости углерода в феррите при охлаждении и выделении цементита, который называется третичным цементитом.
Следовательно, сплавы, содержащие менее 0,008% углерода (точкаQ), являются однофазными и имеют структуру чистого феррита, а сплавы, содержащие углерод от 0,008 до 0,03% – структуру феррит+цементит третичный и называются техническим железом.
Доэвтектоидные стали при температуре ниже 727ºС имеют структуру феррит+перлит и заэвтектоидные – перлит+цементит вторичный в виде сетки по границам зерен.
В доэвтектических чугунах в интервале температур 1147–727ºС при охлаждении из аустенита выделяется цементит вторичный, вследствие уменьшения растворимости углерода (линия ES). По достижении температуры 727ºС (линия PSK) аустенит, обедненный углеродом до 0,8% (точка S), превращаясь в перлит. Таким образом, после окончательного охлаждения структура доэвтектических чугунов состоит из перлита, цементита вторичного и ледебурита превращенного (перлит+цементит).
Структура эвтектических чугунов при температурах ниже 727ºС состоит из ледебурита превращенного. Заэвтектический чугун при температурах ниже 727ºС состоит из ледебурита превращенного и цементита первичного.
Правило фаз устанавливает зависимость между числом степеней свободы, числом компонентов и числом фаз и выражается уравнением:
C = K + 1 – Ф,
где С – число степеней свободы системы;
К – число компонентов, образующих систему;
1 – число внешних факторов (внешним фактором считаем только температуру, так как давление за исключением очень высокого мало влияет на фазовое равновесие сплавов в твердом и жидком состояниях);
Ф – число фаз, находящихся в равновесии.
Сплав железа с углеродом, содержащий 0,7 %С, называется доэвтектоидной сталью. Его структура при комнатной температуре – перлит + феррит. 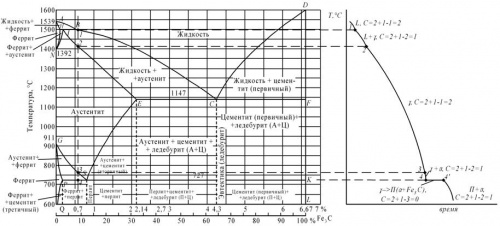
Рисунок 1: а-диаграмма железо-цементит, б-кривая охлаждения для сплава, содержащего 0,7% углерода
Вычертите диаграмму изотермического превращения аустенита стали У8. Нанесите на нее кривую режима изотермической обработки, обеспечивающей твердость 20. 25 HRC. Укажите, как этот режим называется и какая структура образуется в данном случае. 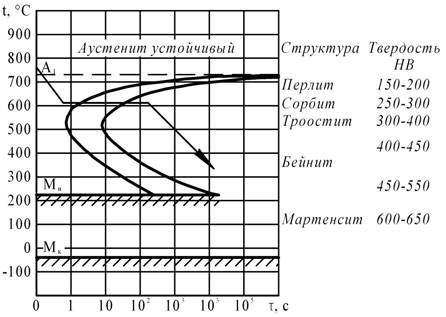
Диаграмма изотермического превращения аустенита стали У8
Изотермической обработкой, необходимой для получения твердости 20 – 25 HRC, является изотермический отжиг. При изотермическом отжиге сталь У8 нагревают до температуры на 30 – 50°С выше точки Ас1 и после выдержки охлаждают до температуры несколько ниже точки Аr1. При этой температуре сталь подвергают изотермической выдержке до полного превращения аустенита, затем охлаждают до комнатной температуры. Для получения структуры пластинчатого перлита заданной твердости (20 – 25HRC) устанавливается температура изотермической выдержки 640 – 660 °С.
Чем ниже температура распада аустенита, тем дисперснее продукты распада аустенита и тем выше получаемая твердость.
Изотермический отжиг по сравнению с обычным отжигом имеет два преимущества. Прежде всего, он может дать выигрыш во времени, если суммарное время ускоренного охлаждения, изотермической выдержки и последующего ускоренного охлаждения меньше времени медленного непрерывного охлаждения изделия вместе с печью. Другое преимущество изотермического отжига – получение более однородной структуры, т.к. при изотермической выдержке температура по сечению изделия выравнивается и превращение во всем объеме стали происходит при одинаковой степени переохлаждения. Структура стали У8 после изотермического отжига – перлит.
Плашки из стали У11А закалены: первая – от 760ºС, вторая – от температуры 850ºС. Используя диаграмму состояния железо-цементит, укажите температуры закалки, объясните, какая из этих плашек закалена правильно, имеет более высокие режущие свойства и почему.
Исходная структура высокоуглеродистой инструментальной стали У11А до нагрева под закалку – перлит + карбиды.
Критические точки для стали У11А: Аc1=730ºС, Аcm=810ºС.
При нагреве до 700ºС в стали У12 не происходят аллотропические превращения и мы имеем ту же структуру – перлит + карбиды, быстро охлаждая (т.к. закалка), имеем также после охлаждения перлит + карбиды с теми же механическими свойствами (примерно), что и в исходном состоянии до нагрева под закалку.
Оптимальный режим нагрева под закалку для заэвтектоидных сталей (%С>0,8%) составляет АС1+(30÷50º), т.е. для У11А – 760–780ºС. При этом после закалки имеем мелкое зерно, обеспечивающее наилучшие механические свойства стали У11А.
Нагрев и выдержка стали У11А при температуре 850ºС перед закалкой приводит к росту зерна и ухудшению механических свойств стали после термической обработки. Крупнозернистая структура вызывает повышенную хрупкость стали, иногда приводит к трещинам.
Таким образом, первая плашка закалена правильно и имеет высокие механические свойства.