Тромбо асс при эко для чего
Секреты хороших результатов в программах ЭКО+ИКСИ
Многие считают, что положительный исход ЭКО полностью зависит от репродуктолога. Но успех программы ЭКО+ИКСИ заключается в слаженной работе всех специалистов клиники, а также и от самих пациентов. Врач консультирует пациента, назначает анализы и готовит к программе. После осуществляется пункция яйцеклеток и подсаживается эмбрион. Врач контактирует с пациентом все время: при обследовании, во время участия в протоколе ЭКО, в период после процедур. Потому вполне логично, что при выборе клиники пациенты обращают внимание на репродуктолога, отношения, которые устанавливаются между ними и врачом. Но только ли от этого зависит итог участия в программе?
После пункции полученные ооциты передаются в лабораторию. И с данного момента будущее ребенка переходит в руки состава врачей-эмбриологов. Какой расходный материал, какие среды используются в лаборатории, насколько они стабильны, соблюдается ли температурный режим это все очень важно и для правильного оплодотворения, и для последующего культивирование эмбрионов. Клиника OXY-center при прохождении программ ЭКО+ИКСИ предоставляет только высококачественные расходные материалы, используются сертифицированные среды для культивирования. Здесь важна каждая деталь, и мы обращаем пристальное внимание на все мелочи процесса.
Рассмотрим кратко описание функционирования эмбриологической лаборатории, а также те работы, которые выполняет врач-эмбриолог.
Важность температурных режимов (термостабилизация) для всех эмбриологических процедур
Организм способен поддерживать постоянную температуру, причем этот процесс происходит с высокой точностью. При естественном зачатии яйцеклетка движется к матке при 37 градусах по Цельсию. Очень важно и при оплодотворении «в пробирке» (и других способах ВРТ) обеспечивать клеткам нужный температурный режим. Поэтому одна из целей эмбриолога приблизить условия проведения процедур в рамках протокола ЭКО к естественным и обеспечить ооцитам нужную температуру. Это же относится и к условиям созревания эмбрионов. Для этого в клинике «Oxy center» практикуют обеспечение термостабилизации.
Термостабилизация подразумевает прогрев всех инструментов, используемых при работе с эмбрионами и ооцитами: иглы для пункции, катетеры, пробирки для фолликулярной жидкости. Поддержание нужной температуры возможно благодаря специальным термостоликам, которыми оборудована эмбриологическая лаборатория.
Контроль уровня углекислого газа и температуры в инкубаторе
При манипуляциях, направленных на оплодотворение яйцеклетки, а также культивирование эмбриона, важно сохранять не только определенную температуру, но и уровень кислорода, влажности, углекислого газа. Используемые нашей клиникой инкубаторы имеют интегрированные термометры и сенсоры, которые регулируют и измеряют данные показатели. Однако для дополнительного контроля их необходимо снимать и вручную. Измерения проводятся нашими эмбриологами с помощью независимых приборов. Полученные показания сравнивают с теми, что высвечиваются на дисплее инкубатора.
Как проходит процедура
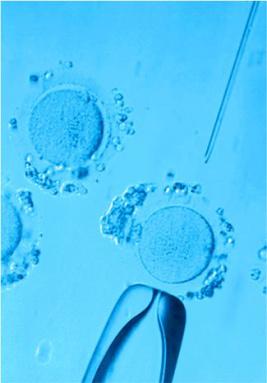
В день пункции эмбриолог в лабораторных условиях изучает сперму. Прежде, чем добавить сперму в среду с ооцитами, ее обрабатывают средствами для удаления семенной плазмы, очищают, центрифугируют, затем микроскопируют, определяют качество спермы и отправляют в инкубатор. Это проводится для получения полноценных и подвижных сперматозоидов. Полученные яйцеклетки врач-эмбриолог совместно с врачом-репродуктологом просматривает под микроскопом и отбирает лучшие, способные к оплодотворению, которые затем переносят в инкубатор с пониженным содержанием кислорода и соблюдением оптимальных условий для культивирования. Они воссоздают натуральную среду в организме будущей матери. Эмбрионы восприимичивы к загрязнению на молекулярном уровне, поэтому в лаборатории строго контролируется чистота и качество воздуха. Для этого применяется уникальная система фильтрации из нескольких стадий. За ее счет достигается стерильная для эмбрионов атмосфера.
Оплодотворение клеток производят по истечению нескольких часов после проведения пункции. Начальные стадии ИКСИ проводятся, как и стандартный цикл ЭКО. При ИКСИ врач-эмбриолог находит сперматозоиды (выбираются подвижные сперматозоиды с лучшей морфологией), обездвиживает их, «всасывает» и вводит в саму яйцеклетку с помощью микроиглы. Ооцит при этом закрепляется в определенном положении посредством микропипетки (холдинга) с противоположной стороны. Эта процедура требует аккуратности и внимательности, а для ее проведения необходим специальный микроманипулятор.
Этот алгоритм действий повторяется отдельно для каждого полученного ооцита. Яйцеклеточная мембрана обладает эластичностью, и минимальное отверстие от микроиглы быстро затягивается благодаря этому свойству мембраны. Далее эмбрионы в индивидуальных каплях специальной среды растут в инкубаторе. Проводится обязательный ежедневный мониторинг их развития. Есть еще три важных вопроса, решаемые репродуктолого и эмбриологом сообща: когда, сколько и какие эмбрионы подсаживать.
Когда и сколько переносить эмбрионов в маточную полость?
В нашей клинике этот вопрос решается индивидуально для каждой супружеской пары. На основании оценки качества эмбрионов, они могут быть перенесены на 3 или 5 сутки после пункции. Так же возможен двойной перенос (на 3 и 5 сутки). Перед началом переноса репродуктолог обсуждает с супругами эмбриологическую ситуацию: сколько имеется эмбрионов, какого они качества, сколько будет перенесено, сколько может быть подвергнуто криоконсервации витрификационным методом, то есть заморозкой, минуя стадию льда. Пациенткам OXY-center мы переносим в маточную полость не более 2-х эмбрионов, по международным стандартам, для понижения риска возникновения многоплодной беременности.
Какие эмбрионы отбираются для переноса?
Это очень важное решение. Принимает его врач-эмбриолог, оценивая эмбрионы непосредственно перед переносом. Лучшая стадия развития утро третьего дня, примерно через 65 часов после ЭКО+ИКСИ. Это 8-клеточный этап. До этого развитие эмбриона идет за счет запасов «материнских» ресурсов, которые накапливает за время роста и созревания яйцеклетка. Дальнейшее его развитие зависит от того, какой геном был сформирован и как своевременно произойдет переход развития на новый этап, зависит и дальнейший рост эмбриона. Как раз на этот период (стадия 4-8 бластомеров) и наступает замирание в развитии многих эмбрионов в результате ошибок в геноме, которые либо перешли от клеток родителей, либо возникли при их слиянии.
К 5 дню внутри эмбриона формируется полость, заполненная жидкостью, увеличивающаяся в размерах, а затем образуется бластоциста. При этом в самой бластоцисте, клетки подразделяются на два типа: те, из которых далее формируется плод (эмбриобласт), и те, из которых формируется плацента (трофобласт). Трофобласты отвечают за имплантацию эмбриона, то есть его крепление в эндометрий. Плацента даст начало внезародышевым оболочкам плода.
В чем заключается процедура переноса?
Большая часть женщин переживает эмбриональный перенос безболезненно: он осуществляется быстро и пациентка может не заметить окончания процедуры. Иногда, эмоционально лабильным женщинам может потребоваться поддержка психолога. При переносе в качестве инструмента применяется гибкий мягкий катетер, заполняемый питательной средой с содержанием одного или нескольких эмбрионов. Перенос происходит под контролем УЗИ, чтобы отслеживать движение среды с эмбрионами в маточной полости. Мы приглашаем приходить на перенос супруга, для психологической поддержки пациентки.
Шанс забеременеть после ИКСИ выше, чем при стандартном ЭКО, до 30%, поэтому мы используем в нашей клинике ЭКО+ИКСИ. После микроинъекции число оплодотворённых ооцитов 60%, а вероятность формирования эмбриона 95%. При необходимости, в ходе подготовки к ВРТ, врач-генетик обследует и консультирует супружескую пару. При знаичтельной вероятности проявления у будущего ребенка различных генетических патологий врач проводит кариотипирование обоих представителей пары, преимплантационная генетическая диагностика (ПГД) эмбрионов. ПГД позволяет отобрать здоровые эмбрионы, которые затем перенесут в маточную полость, а также отсеять эмбрионы с риском отклонений. Данная процедура повышает возможность появления на свет генетически здорового ребенка, а также общую вероятность возникновения беременности при ЭКО+ИКСИ. Задача специалистов «Oxy center» заключается не только в преодолении бесплодия и сохранении ожидаемой беременности, но и при минимальном воздействии на организм матери помочь ей выносить и родить здорового и крепкого малыша.
Как сохранить беременность после ЭКО
Беременность после ЭКО часто протекает с осложнениями. Это происходит потому, что к экстракорпоральному оплодотворению прибегают женщины, имеющие заболевания эндокринной системы и половой сферы. У них часто наблюдаются невынашивание, токсикозы и прочие проблемы, ставящие беременность под угрозу. Чтобы этого не допустить и сохранить беременность после ЭКО, нужно наблюдаться в клинике, имеющей необходимое оборудование и квалифицированных специалистов, работающих с ЭКО-мамами.
Гормональные нарушения при беременности после ЭКО
Эти проблемы вызываются введением больших доз гормонов на этапе подготовки к ЭКО, если проводилась гормональная стимуляция яичников. Для многих женщин — это необходимость и единственная возможность забеременеть, так как стимуляция работы яичников приводит к созреванию сразу нескольких фолликулов. При этом резко повышается концентрация эстрогенов в крови. Гормональный сбой может вызвать нарушения сосудистой проницаемости и скопление жидкости в области легких и брюшной полости. Лишняя влага мешает женщине дышать, вызывает тошноту, рвоту и снижение аппетита.
Ещё одно возможное последствие ГС — замедленное нарастание показателей ХГЧ (хорионического гонадотропина), который называют «гормоном беременности». Этот гормон должен:
При нехватке ХГЧ рост плода замедляется, что приводит к выкидышу и замиранию беременности.
Поддержка беременности после ЭКО в этом случае просто необходима. При наблюдении в специализированной клинике врачи вовремя смогут скорректировать гормональный фон, убрать отечность и устранить угрозу выкидыша.
Инфекционно-воспалительные процессы
Женщины, забеременевшие после ЭКО, часто страдают хроническими воспалениями органов половой сферы, которые и приводят к невозможности естественного зачатия. Хотя в период подготовки к беременности женщин максимально пролечивают, болезни часто обостряются снова. Все это сказывается на работе иммунной системы и снижению выработки гормонов, ответственных за нормальное протекание беременности.
У женщины возникает кровянистая «мазня», указывающая на угрозу прерывания. Плоду в этих условиях нелегко удержаться в матке, поэтому требуется медицинская поддержка беременности после ЭКО. Врачебное наблюдение помогает устранить опасные воспалительные процессы, сохранив беременность после ЭКО.
Материнские проблемы
К ЭКО в основном прибегают женщины в возрасте 30 лет и старше. Большой процент из них имеют различные болезни внутренних органов (почек, сердца, печени, желчного пузыря) и нарушения обмена веществ. Все эти «болячки» склонны к обострениям во время беременности, что негативно влияет на внутриутробное развитие ребенка.
У женщин, уже имеющих проблемы со здоровьем, может возникнуть сахарный диабет беременных, вызванный неправильной работой поджелудочной железы. Уровень глюкозы в крови повышается, что вызывает кислородное голодание плода. Это осложнение чаще возникает, если женщина вынашивает близнецов, что нередко бывает после искусственного оплодотворения. Если вовремя не пролечить возникшие нарушения, беременность можно потерять. Для этого женщины, наблюдаясь в клинике после ЭКО, регулярно сдают кровь на биохимию и сахар.
Фетоплацентарная недостаточность
Это состояние возникает в результате неправильного формирования и или недостаточности плаценты. Поскольку женщины, забеременевшие после ЭКО, часто имеют проблемы в половой сфере, фетоплацентрарные нарушения у них нередки.
В результате страдает плод, которому достается мало питательных веществ и кислорода что может привести к выкидышу или рождению больного ребенка. Помочь при этом состоянии может периодическое назначение допплерометрии, показывающей состояние плодо-плацентарного кровотока. При подозрении на патологию поддержка беременности после ЭКО подразумевает назначение препаратов, улучшающих кровообращение в плаценте и помогающих правильному протеканию беременности.
Многоплодие
Во время ЭКО женщине часто подсаживают сразу несколько эмбрионов. Если все они приживаются, возникает многоплодная беременность. Иногда двойня развивается из одной яйцеклетки, как при обычной беременности, у женщины рождаются однояйцевые близнецы. Многие считают двойню или тройню отличным результатом после ЭКО, забывая, что несколько малышей тяжелее вынашивать и легче потерять.
Иногда природа сама регулирует процесс, и лишние эмбрионы перестают развиваться, но зачастую все подсаженные яйцеклетки растут одинаково. Можно, конечно, провести редукцию (удаление) сверхплановых зародышей, но родители редко соглашаются на это.
У женщин, беременных двойней, токсикоз возникает чаще и протекает тяжелее. Матка, растущая гораздо быстрее, давит на ноги, вызывая их отек. Давление на диафрагму в последние месяцы, мешает полноценному дыханию мамы. На поздних сроках при беременности двойней или тройней, чаще наблюдается повышение давления, которое может привести к судорожному синдрому (эклампсии) и преждевременным родам. Поскольку близнецы и так появляются на свет с небольшим весом, это может привести глубокой недоношенности и гибели новорожденных.
Перерастяжение матки и повышенная нагрузка на организм вызывают:
Женщине, у которой в результате ЭКО сформировалась многоплодная беременность, нужно особое наблюдение и строгий контроль, поэтому ей чаще делают УЗИ, чтобы узнать, как развиваются детки.
Состояние малышей, вынашиваемых ЭКО-мамами, контролируют с помощью УЗИ и допплерометрии. Грамотные врачи, работающие в клинике «Линия жизни», окажут полноценную поддержку беременности после ЭКО и помогут успешно выносить многоплодную беременность и родить здоровых деток. Сознательное отношение женщины и наблюдение опытных специалистов позволяет сохранить большинство беременностей, наступивших после ЭКО.
Как снизить риск венозной тромбоэмболии при приеме КОК
Поделиться:
В предыдущей статье я рассказала вам о главных рисках приема оральных контрацептивов — тромбозе глубоких венвенозной и тромбоэмболии легочной артерии. Это угрожающее жизни состояние, до которого, конечно, лучше не доводить. Сегодня мы по порядку обсудим основные факторы риска и посмотрим, как их следует учитывать.
1. Нельзя — это нельзя
Во-первых, не разрешать принимать КОК женщинам, имеющим противопоказания в соответствии с « Национальными медицинскими критериями методов контрацепции » и с критериями ВОЗ (5-й пересмотр, 2015 г.). 1
2. Учитывать сочетания различных факторов, требующих осторожности
Тщательнейшим образом оценивают соотношение польза/риск у пациенток, имеющих несколько состояний/заболеваний, при которых КОК не противопоказаны, но требуют осторожности (2-й класс приемлемости).
Например, возраст старше 40 лет и ожирение с ИМТ = 30 кг/м2 не являются противопоказаниями, однако сочетание этих двух факторов вполне взрывоопасно. Крупномасштабное когортное исследование European Active Surveillance Study on Oral Contraceptives (EURAS-OC), проведенное в 2000–2005 гг., продемонстрировало связь риска венозных тромбоэмболий с возрастом и весом: чем старше пациентка и чем выше ее вес, тем выше вероятность развития венозного тромбоза.
3. Не делать бессмысленных анализов
В большинстве случаев до начала приема КОК вероятность венозной тромбоэмболии невозможно предсказать с помощью анализов. Никакая коагулограмма и D-димер не позволят оценить, как поведет себя свертывающая система крови.
Сейчас стало очень модно перед назначением КОК всем подряд проводить генетические исследования для выявления мутаций в генах системы гемостаза. Это, конечно, очень любопытно и захватывающе, но нужно только тем, у кого среди близких родственников были ранние инсульты, инфаркты или тромбоэмболии. На самом деле мутации встречаются довольно редко и не являются 100%-ным показателем того, что беда обязательно произойдет.
К слову, о «генетическом риске». В последние годы в научной литературе появился ряд публикаций о том, что у носителей групп крови II, III и IV шансы получить венозный тромбоз в 2 раза выше, чем у носителей первой группы. Этот феномен даже получил название «ненулевая группа крови». Так вот, ненулевая группа крови является более сильным фактором риска тромбоза, чем гетерозиготные полиморфизмы генов II и V факторов. Но мы же не отказываем в возможности принимать КОК всем носителям II (А) группы крови (а их большинство в нашей популяции)!
4. Учитывать «синдром путешествий» (или «синдром эконом-класса»)
5. Если предстоит операция
6. Избегать неоправданных «перерывов»
Совершенно не является тайной, что риск тромбоэмболических осложнений максимально высок в первые месяцы приема КОК — в период адаптации к препарату. Уже через 3 месяца риск существенно снижается и концу первого года становится даже ниже среднепопуляционного.
Как снижается риск венозных тромбозов 5
Частота венозной тромбоэмболии vs продолжительность приема КОК. Исследование EURAS.
Прим. Повышенный риск в основном сконцентрирован в первый год (точнее, в первые 3 месяца) после начала применения.
«Отдых» от контрацептивов для женщины, нуждающейся в контрацепции, чреват не только наступлением нежелательной беременности, но и вполне серьезными осложнениями. В конце концов, решительно непонятно, от чего именно так «устал» организм, находящийся в монотонном дремлющем состоянии на фоне регулярного приема КОК.
Для подавляющего большинства здоровых женщин репродуктивного возраста достоверно установленные полезные свойства КОК перевешивают очень низкий абсолютный риск развития венозной тромбоэмболии, но знать об этом и применять соответсвующие меры предосторожности, безусловно, необходимо.
Восстановление легких после коронавируса
Восстанавливаются ли легкие после COVID-19? Да. Но нужно не пропустить сроки реабилитации и серьёзно отнестись к рекомендациям врача.
Новая коронавирусная инфекция, вызванная SARS-CoV-2, недостаточно изучена, однако ясно, что она наносит вред всем органам и тканям человека. Вирус проникает в организм через слизистые оболочки носа, глаз, глотки. Первые симптомы появляются на 2-14 день. Обычно это повышение температуры выше 37.5 градусов Цельсия, насморк, потеря обоняния, сухой кашель, послабление стула, слабость и головная боль. На 6–10 сутки от момента появления первых симптомов могут начать беспокоить одышка, боль в груди, усиление кашля. Это тревожные симптомы, говорящие о поражении легких и требующие проведения дополнительного обследования: компьютерной томографии легких, измерения насыщения крови кислородом (сатурации).
Легкие после COVID-19
Попадая в организм человека через слизистые оболочки дыхательных путей SARS-CoV-2 вызывает мощнейшую воспалительную реакцию. Активируются иммунные клетки, вырабатывается колоссальное количество воспалительных веществ (воспалительных цитокинов). Интенсивность этой реакции скорее всего обусловлена генетически. Именно интенсивностью воспалительной реакции и определяется тяжесть поражения легочной ткани по данным исследований. В легочной ткани поражение при COVID-19 обусловлено как поражением самих альвеол (в которых происходит газообмен и кровь насыщается кислородом из воздуха) нашими собственными иммунными клетками так и поражением легочных сосудов, оплетающих альвеолы. Степень поражения легких можно определить при помощи КТ (компьютерной томографии).
Таблица 1. Поражение лёгких при COVID-19
Процент поражения легочной ткани
Поражена часть лёгкого. Небольшое затруднение дыхания.
Обследование и ведение беременных пациенток с наследственной предрасположенностью к тромбофилическим осложнениям и тромбофилиями различного генеза
Тромбофилия не является заболеванием, ее стоит рассматривать скорее как патологическое состояние или синдром, возникающие под воздействием комбинации постоянных или временных факторов риска, вызывающих тромбозы [3].
Показанием к обследованию пациенток является возникновение идиопатических тромбозов, инсультов, инфарктов, наличие выкидышей, тяжелого гестоза, преждевременной отслойки нормально расположенной плаценты, преждевременных родов на сроках до 34 недель, синдрома задержки роста плода при предыдущих беременностях, тромбозов, возникших на фоне приема контрацептивных препаратов или заместительной гормональной терапии (ЗГТ) [2]. Показаниями к лабораторной диагностике тромбофилии у пациентки является наличие следующих общих признаков патологии:
первая манифестация тромбоза в возрасте 13–20–30 лет;
артериальные и венозные тромбозы (от тромбоза поверхностных вен до ТЭЛА);
тромбоз на фоне применения непрямых антикоа- гулянтов (варфарин – снижение витамина К);
у новорожденных: неонатальная коагулопатия, фульминантная пурпура как причина смерти. Сведения о патологических состояниях получают прежде всего из анамнеза.
КОМПЛЕКСНОЕ ОБСЛЕДОВАНИЕ
Таким образом, обследование беременной в I триместре при постановке на учет либо пациентки, планирующей беременность, начинают именно со сбора подробного анамнеза, который включает в себя семейный анамнез: семейный акушерский, семейный тромботический (в том числе сведения о заболеваниях матери и отца в трудоспособном возрасте, такие как гипертония (ГБ), ишемическая болезнь сердца (ИБС), острое нарушение мозгового кровообращения (ОНМК) и др. Также важны анамнез экстрагенитальных заболеваний пациентки, диагностированных до или во время беременности (ГБ, СД, СКВ и др.), и оценка репродуктивной функции пациентки.
При привычном невынашивании беременности рекомендуются дополнительные виды исследований, такие как Д-димер, растворимый фибрин-мономерный комплекс (РФМК), тромбоэластография, уровень ингибитора активатора плазминогена, исследование на антифосфолипидный синдром (АФС) с интервалом 6 недель:
IgM и IgG кардиолипину, фосфолипидам, гликопротеиду;
Высокоинформативным является анализ на полиморфизм генов тромбофилии. Причем приказом МЗ РФ № 572-Н предусмотрены исследования на определение уровня протромбина, протеинов С и S. Дополнительно к приказу рекомендуется назначить исследование на гомоцистеин.
Оценить вероятность предтромботического состояния и развития тромбоза, а также эффективность и безопасность терапии в тромбоцитарном звене позволит определение количества тромбоцитов (PLT). В норме PLT составляет 180 – 320 х 109 /л, при тромбоцитозе более 350 х 109 /л и тромбоцитопении менее 100 х 109 /л.
СРЕДНИЙ ОБЪЕМ ТРОМБОЦИТОВ (MPV) СОСТАВЛЯЕТ 3,6–9,4 МКМ. ОТ РАЗМЕРА ТРОМБОЦИТА ЗАВИСЯТ СОДЕРЖАНИЕ В НЕМ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ И ЕГО СКЛОННОСТЬ КЛЕТОК К АДГЕЗИИ. СЛЕДУЕТ ПОМНИТЬ, ЧТО ОБЪЕМ ТРОМБОЦИТОВ ИЗМЕНЯЕТСЯ ПЕРЕД АГРЕГАЦИЕЙ, И ЧЕМ БОЛЬШЕ ОБЪЕМ ТРОМБОЦИТОВ, ТЕМ ОНИ «МОЛОЖЕ» [1]. ПРЕОБЛАДАНИЕ В КРОВИ МОЛОДЫХ ФОРМ ТРОМБОЦИТОВ НАБЛЮДАЕТСЯ ПРИ КРОВОПОТЕРЕ И СВИДЕТЕЛЬСТВУЕТ ОБ УСИЛЕННОЙ РЕГЕНЕРАЦИИ. УВЕЛИЧЕНИЕ УРОВНЯ СТАРЫХ И УМЕНЬШЕНИЕ СОДЕРЖАНИЯ ЗРЕЛЫХ ТРОМБОЦИТОВ ХАРАКТЕРНЫ ДЛЯ РАЗЛИЧНЫХ ВОСПАЛИТЕЛЬНЫХ ПРОЦЕССОВ, ИНТОКСИКАЦИЙ, ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ.
ОЦЕНКА ФУНКЦИОНИРОВАНИЯ СИСТЕМЫ КОАГУЛЯЦИИ
Агрегация тромбоцитов. Для определения исходной функции тромбоцитов, эффективности антиагрегантной терапии назначается исследование спонтанной агрегации тромбоцитов или исследование с применением индукторов: аденозиндифосфатом (АДФ), адреналином, коллагеном ристоцетином.
ОПРЕДЕЛЕНИЕ ДЛИТЕЛЬНОСТИ КРОВОТЕЧЕНИЯ – ВАЖНЫЙ И ИНФОРМАТИВНЫЙ ТЕСТ, КОТОРЫЙ ПОЗВОЛЯЕТ ОДНОВРЕМЕННО КАЧЕСТВЕННО ОЦЕНИТЬ КОЛИЧЕСТВО ТРОМБОЦИТОВ В КРОВИ, ИХ АДГЕЗИВНЫЕ И АГРЕГАЦИОННЫЕ СВОЙСТВА, ФУНКЦИОНАЛЬНЫЕ ХАРАКТЕРИСТИКИ СТЕНКИ КРОВЕНОСНЫХ СОСУДОВ, А ТАКЖЕ ВЫРАЖЕННЫЙ ДЕФИЦИТ ПЛАЗМЕННЫХ ФАКТОРОВ СВЕРТЫВАНИЯ. В НОРМЕ ДЛИТЕЛЬНОСТЬ КРОВОТЕЧЕНИЯ СОСТАВЛЯЕТ 4–8 МИНУТ.
Агрегация тромбоцитов с АДФ показывает количество высвобождающихся собственных агонистов, содержащихся в гранулах тромбоцитов. Определение агрегации тромбоцитов с ристоцетином показано для диагностики болезни фон Виллебранда (увеличение времени кровотечения при нормальном количестве тромбоцитов и отсутствие явных причин для дисфункции тромбоцитов).
Удлинение времени кровотечения отражает на- рушение гемостаза вследствие тромбоцитопений, тромбоцитопатий врожденного и приобретенного генеза (нарушения функций тромбоцитов – адгезии и агрегации), нарушений сосудистой стенки или сочетания этих факторов. Время кровотечения мо- жет увеличиться при применении антиагрегантной терапии, синдроме диссеминированного внутрисосудистого свертывания (ДВС), синдроме «массивных» трансфузий. Увеличение длительности кровотечения при нормальном количестве тромбоцитов в крови позволяет предположить нарушение их функций.
Укорочение времени кровотечения характерно для гиперагрегации тромбоцитов.
Информативным для лечащего врача является также определение активированного частичного тромбопластинового времени (АЧТВ), которое при беременности в норме колеблется от 25 до 40 секунд. Удлинение АЧТВ свидетельствует о дефиците плазменных факторов коагуляции ниже 10–25 %, применении антикоагулянтов. Укорочение АЧТВ говорит о гиперкоагуляции, характерной для ДВС, а значит, необходимо решить вопрос о назначении антикоагулянтной терапии. При проведении терапии гепаринами осуществляется обязательный контроль АЧТВ: удлинение АЧТВ более чем в 2,5 раза от нормы перед очередным введением гепарина свидетельствует о высокой чувствительности к гепаринотерапии и требует снижения дозы.
ПРОТРОМБИНОВОЕ ВРЕМЯ (ПТВ) ПОЗВОЛЯЕТ ПРОИЗВЕСТИ ОЦЕНКУ ВНЕШНЕГО ПУТИ СВЕРТЫВАНИЯ КРОВИ 1 ФАЗЫ. В НОРМЕ ПТВ СОСТАВЛЯЕТ 12–16 СЕК. ЕГО УКОРОЧЕНИЕ ПОКАЗЫВАЕТ АКТИВАЦИЮ ВНЕШНЕГО ПУТИ КОАГУЛЯЦИОННОГО ГЕМОСТАЗА, А УДЛИНЕНИЕ – ДЕФИЦИТ, ЧТО ОЗНАЧАЕТ НЕОБХОДИМОСТЬ НАЗНАЧЕНИЯ ЛЕЧЕНИЯ ФАКТОРАМИ ПРОТРОМБИНОВОГО КОМПЛЕКСА (ПРОТРОМПЛЕКС, НОВОСЕВЕН И ДР).
Удлинение ПТВ наблюдается при заболеваниях печени и желчного пузыря, нарушениях эвакуации желчи, циркуляции ВА, дефиците или аномалии факторов протромбинового комплекса [5].
В процессе коагуляции важна концентрация фибриногена, которая в норме составляет 2–4 г/л. Ее повышение может наблюдаться в последние месяцы беременности, после родов и хирургических операций, в период воспалительных и неопластических заболеваний, при легких формах гепатитов, в I-й фазе ДВС.
СНИЖЕНИЕ КОНЦЕНТРАЦИИ ФИБРИНОГЕНА ХАРАКТЕРНО ДЛЯ ТЯЖЕЛЫХ ЗАБОЛЕВАНИЙ ПЕЧЕНИ, НАСЛЕДСТВЕННЫХ ГИПО-, АФИБРИНОГЕНЕМЙ, ПЕРВИЧНОГО ФИБРИНОЛИЗА, II И III СТАДИЙ ДВС, ПРИЧЕМ В ПОСЛЕДНЕМ СЛУЧАЕ ВАЖНЫ НЕ СТОЛЬКО ПОКАЗАТЕЛИ, СКОЛЬКО ДИНАМИКА, СКОРОСТЬ ИЗМЕНЕНИЯ КОНЦЕНТРАЦИИ.
При активации системы фибринолиза (взаимо- действие плазмина с фибриногеном и фибрином) образуются растворимые комплексы мономеров фибрина (РФМК), которые не должны превышать 10 мг/л. РФМК расценивается как ранний признак ДВС. О хроническом ДВС свидетельствует постоянная циркуляция мономерных комплексов в крови.
Исследование на Д-димеры используется для диагностики ДВС. При добавлении специфической сыворотки определяется количество Д-димеров, по которым судят о фибринолизе. Д-димер не повышается у пациентов с дефицитом тканевого активатора плазминогена или высокой активностью ингибитора активатора плазминогена часто даже при тромбозе глубоких вен (ТГВ) и тромбозе легочной артерии (ТЭЛА).
Информативно исследование на определение процента активности белка-антикоагулянта антитромбина III, нормальный показатель – 80–120 %. Любое изменение концентрации (как снижение, так и повышение) может указывать на наличие генетических мутаций в гене антитромбина III. Уменьшение характеризует заболевания печени, причем в этом случае снижение концентрации АТ III пропорционально тяжести заболевания. Кроме того, более низкие значения возможны при введении пациенту нефракционированного гепарина (НФГ), который при низкой концентрации АТ III не дает ожидаемого эффекта. Снижение концентрации также может наблюдаться при шоковых состояниях (например, при острой почечной недостаточности (ОПН) и активации ингибиторов АТ III в крови).
Следует помнить, что показатели содержания АТ III снижаются в середине менструального цикла, в послеоперационном периоде, при синдроме ДВС, приеме оральных контрацептивов, эстрогенов.
Повышение концентрации АТ III характерно для вирусного гепатита, холестаза, может наблюдаться при дефиците витамина К, приеме антикоагулянтов непрямого действия (например, варфарина) или во время менструации.
ЗАКЛЮЧЕНИЕ
Для получения точной информации о состоянии пациентки лабораторные методы исследований дополняются инструментальными: УЗИ, ЭКГ и УЗДГ сосудов нижних конечностей. В соответствии с приказом Министерства здравоохранения Российской федерации УЗИ рекомендуется проводить:
при постановке на учет;
на сроке 11–14 недель;
на сроке 18–21 неделя;
на сроке 30–34 недели;
планово с 33 недель КТГ;
Желательно получить информацию максимально рано, чтобы принять решение для назначения лечения: при пренатальном обследовании, обследовании в I триместре беременности, при возникновении осложнений во время настоящей беременности.
1. Агаркова Т. А., Трифонова Е. А., Габитова Н. А. Анализ генетических маркеров наследственной тромбофилии и эндотелиальной дисфункции при осложненном течении беременности. Всероссийский научный форум «Мать и дитя», 11-й. Материалы. М 2010; 6–7.
2.Баркаган З. С. Руководство по гематологии. М: Ньюдиамед, 2005; 3: 416.
4. Ройтберг Г. Е., Струтынский А. В. Лабораторная и инструментальная диагностика заболеваний внутренних органов – М.: ЗАО «Издательство БИНОМ», 1999 г. – 622 с.
6.Clark P., Brennand J., Conkie J. at al. Activated protein C sensitivity, protein C, protein S and coagulation in normal pregnancy // Thromb Haemost.. – 1998. – Вып. 79. – С. 1166–1170.