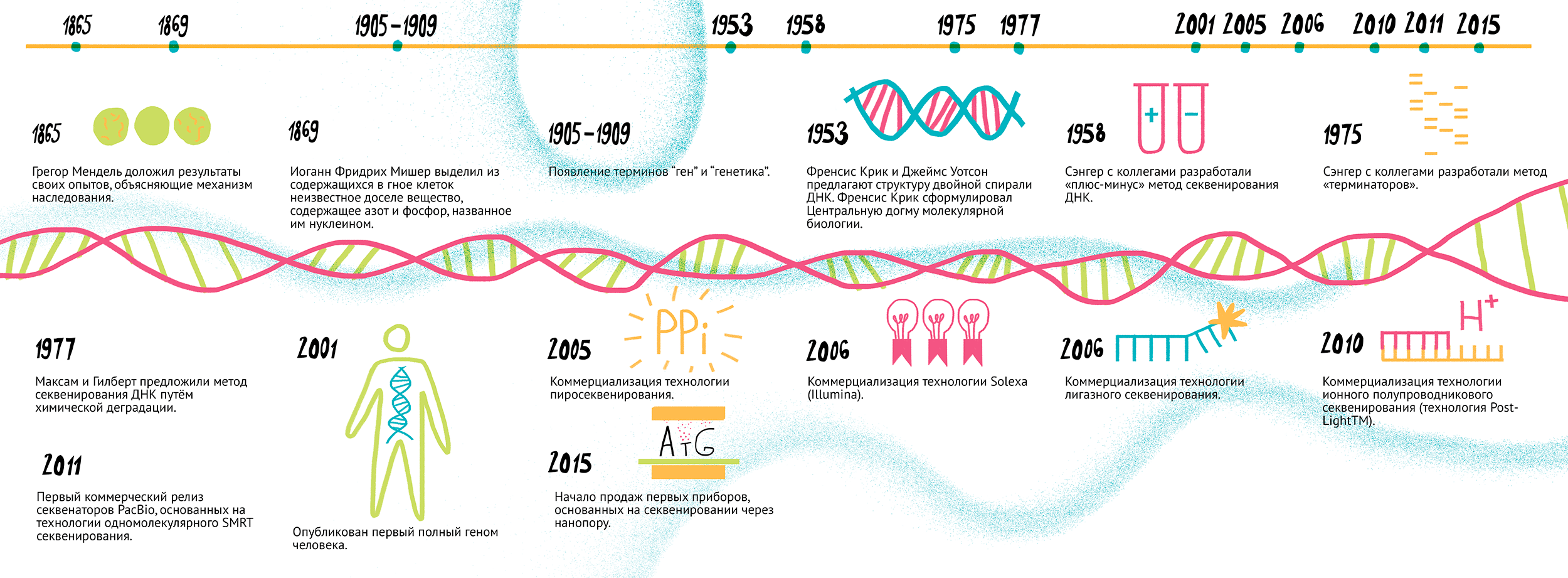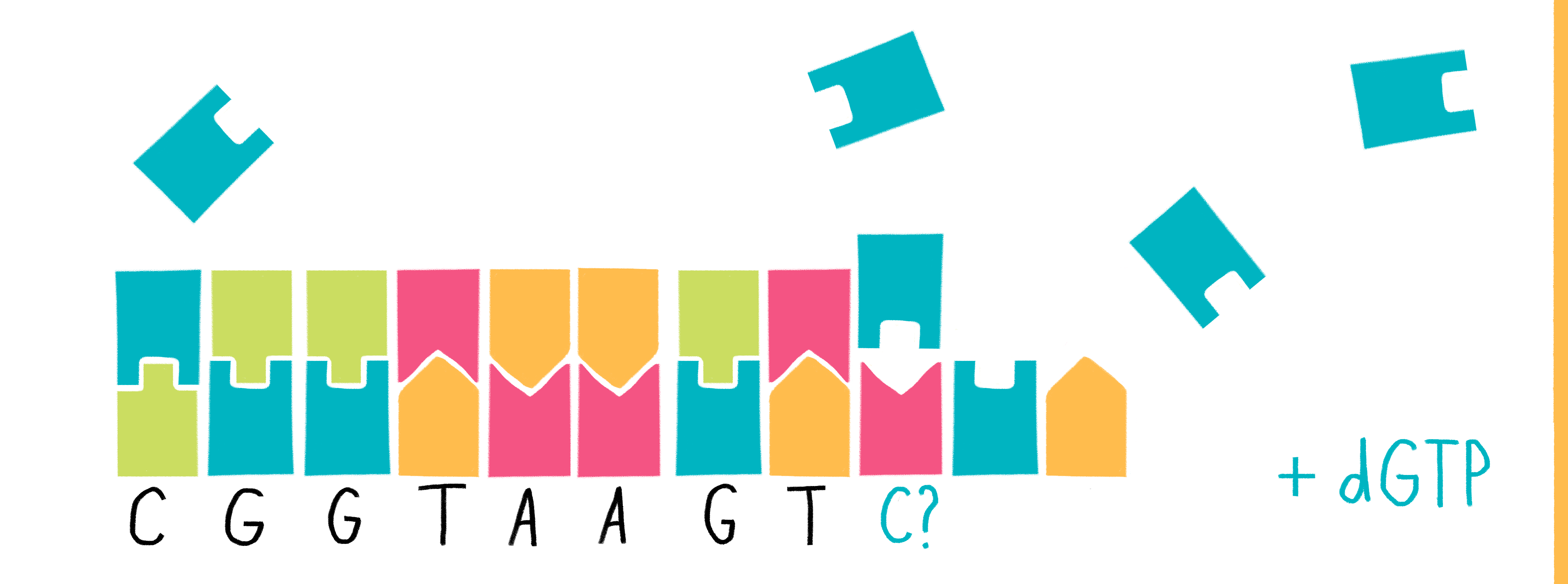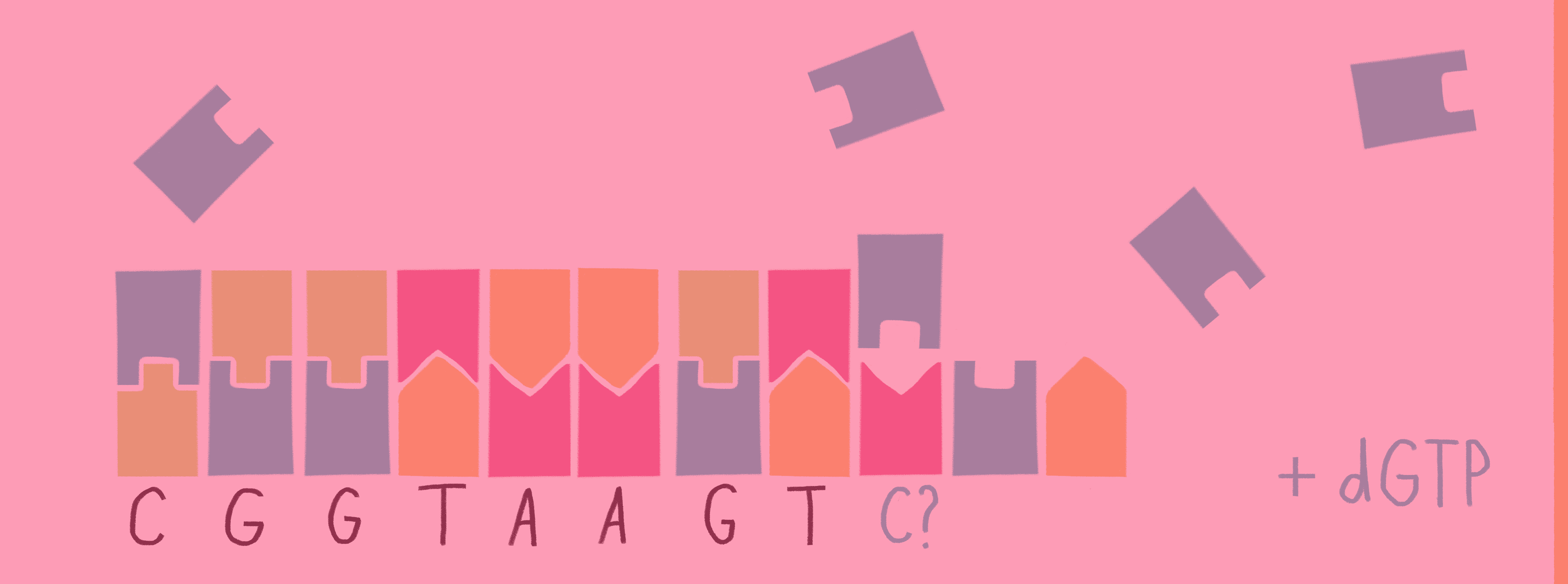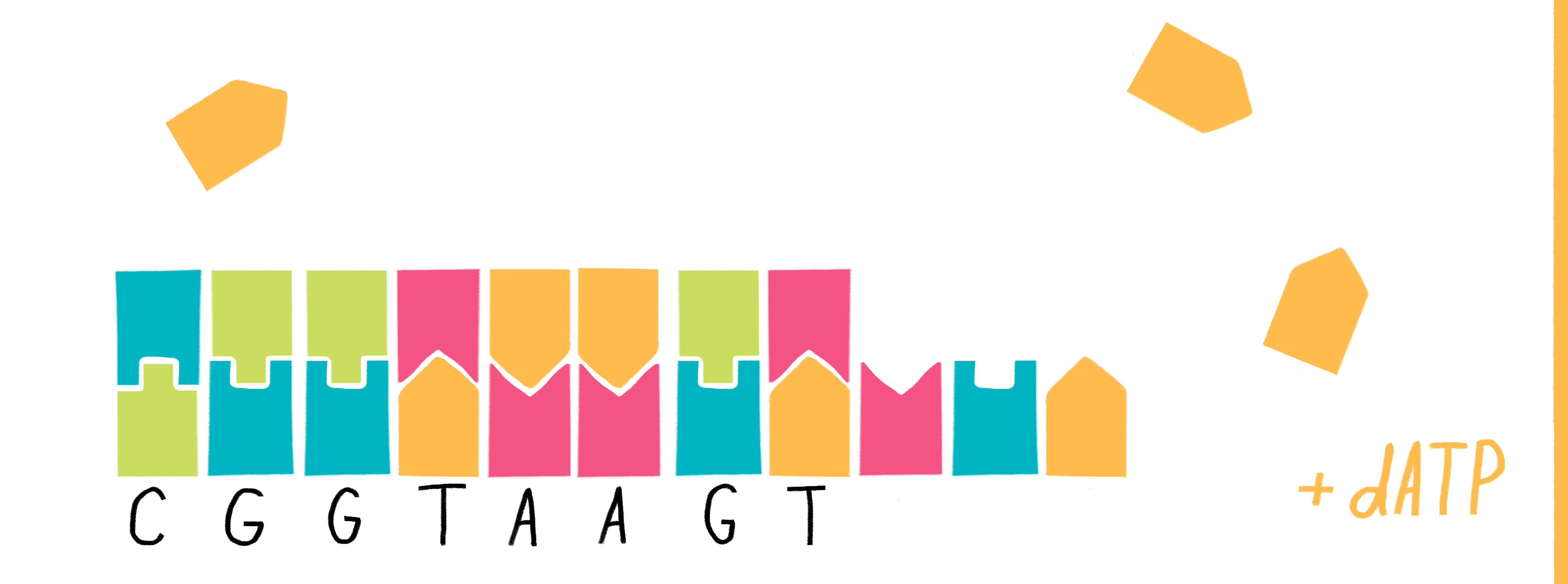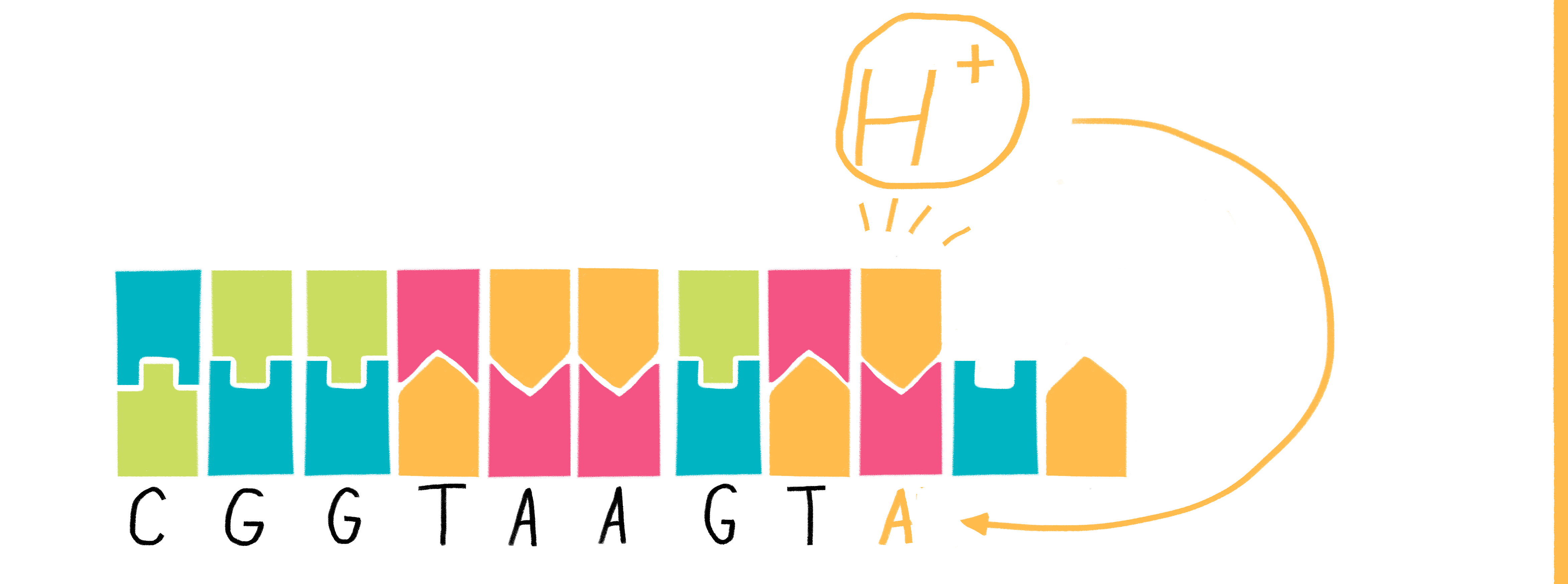rna dna что это
RNA/DNA ratio
Смотреть что такое «RNA/DNA ratio» в других словарях:
RNA/DNA ratio — RNA/DNA ratio. См. соотношение РНК/ДНК. (Источник: «Англо русский толковый словарь генетических терминов». Арефьев В.А., Лисовенко Л.А., Москва: Изд во ВНИРО, 1995 г.) … Молекулярная биология и генетика. Толковый словарь.
DNA replication — DNA replication. The double helix is unwound and each strand acts as a template for the next strand. Bases are matched to synthesize the new partner strands. DNA replication is a biological process that occurs in all living organisms and copies… … Wikipedia
DNA oxidation — is the process of oxidative damage on Deoxyribonucleic Acid. It occurs most readily at guanine residues due to the high oxidation potential of this base relative to cytosine, thymine, and adenine. It is widely believed to be linked to certain… … Wikipedia
DNA extraction — DNA isolation is a routine procedure to collect DNA for subsequent molecular or forensic analysis. There are three basic and two optional steps in a DNA extraction: Breaking the cells open, commonly referred to as cell disruption or cell lysis,… … Wikipedia
DNA microarray — A DNA microarray (also commonly known as gene chip, DNA chip, or biochip) is a collection of microscopic DNA spots attached to a solid surface. Scientists use DNA microarrays to measure the expression levels of large numbers of genes… … Wikipedia
DNA microarray experiment — steps involved in a microarray experiment (some steps omitted) For DNA microarrays in general, see DNA microarray. This is an example of a DNA microarray experiment, detailing a particular case to better explain DNA microarray experiments, while… … Wikipedia
соотношение РНК/ДНК — RNA/DNA ratio соотношение РНК/ДНК. Kоличественное отношение содержания РНК и ДНК в клетке (ткани), как правило, положительно коррелированное со скоростью роста организма; увеличение С.РНК/ДНК свидетельствует о возрастании транскрипционной… … Молекулярная биология и генетика. Толковый словарь.
Соотношение РНК/ДНК — * суадносіны РНК/ДНК * RNA/DNA ratio количественное отношение содержания РНК и ДНК в клетке (ткани), как правило, положительно коррелирует со скоростью роста организма. Увеличение соотношения свидетельствует о возрастании транскрипционной… … Генетика. Энциклопедический словарь
cell — cell1 cell like, adj. /sel/, n. 1. a small room, as in a convent or prison. 2. any of various small compartments or bounded areas forming part of a whole. 3. a small group acting as a unit within a larger organization: a local cell of the… … Universalium
Abiogenesis — Primordial soup redirects here. For the board game, see Primordial Soup (board game). Origin of life redirects here. For views on the origins of life outside the natural sciences, see Creation myth. Pre Cambrian stromatolites in the Siyeh… … Wikipedia
А не замахнуться ли нам на. изменение генома?
А не замахнуться ли нам на. изменение генома?
Ученые научились редактировать молекулу ДНК в интересующем месте
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Человек стремится покорить природу, и ключ для этого — ДНК. Но чтобы подобраться к молекуле ДНК и повлиять на нее, необходимо использовать точнейшие молекулярные инструменты — белки или РНК. В этой статье рассказывается о новейшем инструменте для внесения мутаций в геном in vivo — сиквенс-cпецифичных нуклеазах.
Конкурс «био/мол/текст»-2013
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2013 в номинации «Лучший обзор».
Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
История изучения ДНК непроста, как и любое значительное исследование. Открыта она была еще в 1868 году Иоганном Фридрихом Мишером, который выделил некое вещество, содержащее азот и фосфор, из остатков клеток в гное [1]. После того, как Мишер обнаружил, что оно обладает кислотными свойствами, вещество назвали нуклеиновой кислотой. Однако долгое время функция ДНК была неясной: ее считали всего лишь способом запасания фосфора в организме. Данная теория считалась правильной почти до середины XX века; в качестве косвенного доказательства ученые ссылались на однообразное, по их мнению, строение молекулы ДНК (состоящей исключительно из четырех различных видов нуклеотидов: дезоксиаденозина — А, дезоксигуанозина — G, дезокситимидина — Т, дезоксицитидина — С).
Функцию ДНК, естественно, открыли раньше, чем ее вторичную структуру, которая оставалась неизвестной вплоть до 1953 года. Соответственно, из-за этого не могли установить, как проходят такие процессы как передача наследственной информации, как белки распознают определенные последовательности в ДНК и т.п.
В 1949–1951 годах Эрвин Чаргафф сформулировал свои знаменитые правила, которые говорят о строгом соотношении количества азотистых оснований внутри каждой молекулы ДНК [4] (в частности, что количество аденина равняется количеству тимина, а количество цитозина — количеству гуанина); затем Морисом Уилкинсом и Розалиндой Франклин были получены рентгеноструктурные данные, несущие структурную информацию о ДНК. На основании этих двух фактов Френсис Крик и Джеймс Уотсон предложили структуру двойной спирали ДНК [5], которая была доказана позднее в опытах Мэтью Мезельсона и Франклина Сталя [6].
Как только была открыта вторичная структура ДНК, стало легче предсказывать, а затем доказывать экспериментами механизмы различных процессов, происходящих с ДНК. Репликация (удвоение молекулы ДНК), транскрипция (перенос генетической информации с ДНК на РНК), различная регуляция экспрессии генов стали главными проблемами, интересующими молекулярных биологов.
Очевидно, что для осуществления этих процессов необходимы определенные белки, которые, в свою очередь, взаимодействуют как друг с другом, так и с ДНК. И если некоторые стадии протекают неспецифично (например, у эукариот репликация ДНК может начаться во множестве участков ДНК [7]), то, например, регуляция экспрессии генов происходит с помощью взаимодействия белков с довольно консервативными, т.е. строгими последовательностями ДНК.
Эндонуклеазы рестрикции: «Режем ДНК в нужном вам месте!»
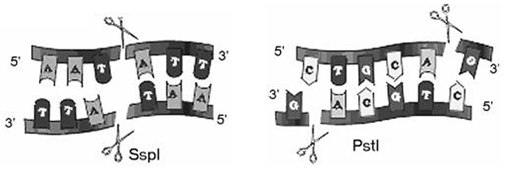
Одними из первых открытых белков, специфически связывающих ДНК, являются эндонуклеазы рестрикции. Это ферменты, которые разрезают ДНК по специфическим нуклеотидным последовательностям, называемым сайтами рестрикции (рис. 1) [8].
Рисунок 1. Рестрикция с образованием а) «тупых» концов; б) «липких» концов
Сам термин «рестрикция» появился благодаря исследованиям фага λ и феномена контролируемой рестрикции и модификации бактериальных вирусов клетками-хозяевами. Этот процесс был впервые обнаружен в результате работ Сальвадора Лурии [9] и Джузеппе Бертани [10] в 1950-х годах. Ученые обнаружили, что если фаг λ хорошо растет в одном штамме Escherichia coli, то в другом штамме его рост падает на несколько порядков, т.е. клетка-хозяин может снижать его биологическую активность. Оказалось, что запрет роста — «рестрикция» — вызывается ферментативным расщеплением ДНК фага. Соответственно, и фермент, отвечающий за этот процесс, назвали ферментом рестрикции.
Сами ферменты были обнаружены в лабораториях Вернера Арбера и Мэттью Мезельсона [11]; причем эндонуклеазы, которые исследовались в их работах, принадлежали, как определили позже, к I классу эндонуклеаз рестрикции. Они разрезают ДНК в случайном месте снаружи от места распознавания, причем как минимум на расстоянии 1000 нуклеотидов.
В 1970-х годах Гамильтон Смит, Томас Келли и Кент Велкокс выделили и охарактеризовали первую эндонуклеазу рестрикции II класса. Этот тип ферментов рестрикции более удобен для лабораторного использования, поскольку расщепляет ДНК внутри своего сайта распознавания, который, как правило, представляет собой палиндром из 4–8 нуклеотидов. Кроме того, эндонуклеазы этого класса не нуждаются в энергетической молекуле АТФ для активности, — только в ионах магния в качестве кофактора.
В 1990-х и ранних 2000-х годах были открыты другие представители данного семейства, которые не соответствовали всем критериям этого класса ферментов [12]. На данный момент уже открыты эндонуклеазы типов IIB, IIE, IIF, IIG, IIM, IIS, IIT. Возможно, в будущем этот список еще значительно расширится.
Существует также III класс эндонуклеаз рестрикции. Они были также открыты как компоненты прокариотической защитной системы против чужеродной ДНК. Эндонуклеазы III типа распознают две отдельных последовательности ДНК длиной 5–6 нуклеотидов и разрезают её примерно через 20–30 пар после сайта распознавания. Для их работы необходимы молекулы АТФ.
Эндонуклеазы рестрикции используют для обработки ДНК в различных лабораторных экспериментах. Обычно их применяют для вставки генов в процессах генного клонирования и экспериментах по исследованию белков.
Кроме того, эндонуклеазы могут быть использованы для выявления различий в аллелях гена [13]. Это возможно только в случае, если мутация произойдет в сайте узнавания, содержащемся внутри аллеля. Таким образом, отпадает нужда в дорогостоящем секвенировании гена; в частности, до изобретения секвенирования обработка эндонуклеазами рестрикции использовалась для картирования геномов.
Одно из новейших применений нуклеаз — внесение с помощью них различных изменений в геном клетки, таких как мутации уже имеющихся генов, вставка новых генов или вырезание исходных. Это очень перспективное направление генной инженерии с широчайшими возможностями практического применения! О нем будет рассказано в следующем разделе.
Эндонуклеазы — это эффекторы, т.е. белки действия. Если они окажутся у цели, то точно ее разрежут. Но природные белки распознают лишь небольшое число последовательностей ДНК, что накладывает огромные ограничения на использование этого уникального инструмента. Ах, если бы можно было доставить эндонуклеазу к любой желаемой последовательности ДНК.
Революция в области ДНК-связывающих белков: «Доставим ваш белок по любому адресу ДНК, используя TAL-эффекторы или CRISPR/Cas9-систему»
Одной из наиболее заманчивых идей для ученых является возможность напрямую точечно влиять на работу клетки. Для этого необходимо прицельно воздействовать на ДНК именно в области интересующего гена. Воздействие может быть разного характера: включение/выключение гена, внесение мутации и др. Для этого потребовалось уметь синтезировать белки, узнающие конкретную последовательность ДНК («следопыты»), к которым можно было бы пришить белки «действия».
Недавно открытые белки TAL-эффекторы и система Cas9 произвели настоящую революцию в нацеливании различных эффекторов на специфическую последовательность ДНК!
TAL-эффекторы: «Используем паразитов во благо»
TAL-эффекторы (Transcription Activator Like Effectors) — белки, синтезируемые многочисленным видами бактерий рода Xanthomonas — паразитами растений. Они были открыты в 2009 году практически одновременно несколькими группами ученых. TAL-эффекторы активируют считывание нужных паразитам генов в растениях-хозяевах (крайне специфично связываясь с хозяйской ДНК), что облегчает бактериальную колонизацию этого растения и выживание бактерий внутри него [14].
TAL-эффектор можно мысленно поделить на три части (рис. 2); наибольший интерес представляет средняя, крайне консервативная центральная область белка, состоящая из повторяющихся блоков размером 34 аминокислоты. В 2009 же году была показана простая и однозначная связь между повторами и узнаваемыми нуклеотидами. Блоки отличаются друг от друга лишь аминокислотами № 12 и № 13, которые и определяют вид нуклеотида, распознаваемый данным мономером. На каждый из четырех нуклеотидов ДНК приходится определенное сочетание этих аминокислот TAL-эффектора [15]; т.е. можно представить себе этот белок как паровозик, состоящий из одинаковых вагонов, центральное окошко которых покрашено в один из четырех цветов.
Рисунок 2. Строение TAL-эффектора на примере avrBs3
Простота «TALE-кода» открывает многочисленные возможности для биологического применения этих белков. Недавние исследования показали, что можно специально подобрать «вагоны» для искусственного «паровозика» и синтезировать ранее не существовавшие в природе белки для узнавания конкретных последовательностей ДНК в различных типах клеток — как растений, так и млекопитающих. Многие группы ученых уже используют искусственные TAL-эффекторы, узнающие новые последовательности ДНК, например, в томатах, Arabidopsis thaliana [16] и клетках человека [17].
Синтезированные TAL-эффекторы также сшивают с каталитическим доменом нуклеазы (см. раздел «Эндонуклеазы рестрикции») для создания TAL-эффекторных нуклеаз. Эти нуклеазы могут быть полезны для генной инженерии и генной терапии [18].
TAL-нуклеазы используют для создания двуцепочечных разрывов в строго определенном месте ДНК. Известно, что нарушенные таким образом гены клетка может чинить двумя путями: либо просто соединением концов (что может привести к случайным мутациям), либо заново синтезируя поврежденную цепь по комплементарной ей цепи ДНК (т.н. гомологичная рекомбинация).
Во втором случае вырезается значительный по длине участок ДНК, а вместо него по комплементарной (на краях разрыва) матрице синтезируется вставка, закрывающая брешь [19]. Если в клетку поместить ДНК специально мутированного гена, то он будет использован в качестве донорной матрицы, и в геном встроится желаемая мутация. Можно таким методом даже вырезать отдельные гены — или вставлять новые! Таким образом, благодаря разработанной технике сборки ДНК-узнающих повторов, TAL-эффекторы в составе гибридных белков предоставляют возможность направить желаемый эффектор к любой специфической последовательности ДНК — и добиться самых разных воздействий на ДНК: от регуляции транскрипции до внесений мутаций.
CRISPR/Cas9 система: «Неожиданное альтернативное применение защитного комплекса бактерий»
В нашем организме, после того, как мы переболели какой-то болезнью, остаются клетки памяти иммунной системы, которые при повторном попадании в организм вредителей активизируются и помогают ускоренно справиться с ними.
Бактерии справляются со своими патогенами с помощью аналогичной «системы памяти»: CRISPR/Cas-системы обеспечивают иммунитет бактерий и архей против вирусов и плазмид. Этот защитный комплекс состоит из:
Этот комплекс был открыт в 2012 году при совместной работе ученых из США, Швейцарии, Австрии и Швеции [20], [21].
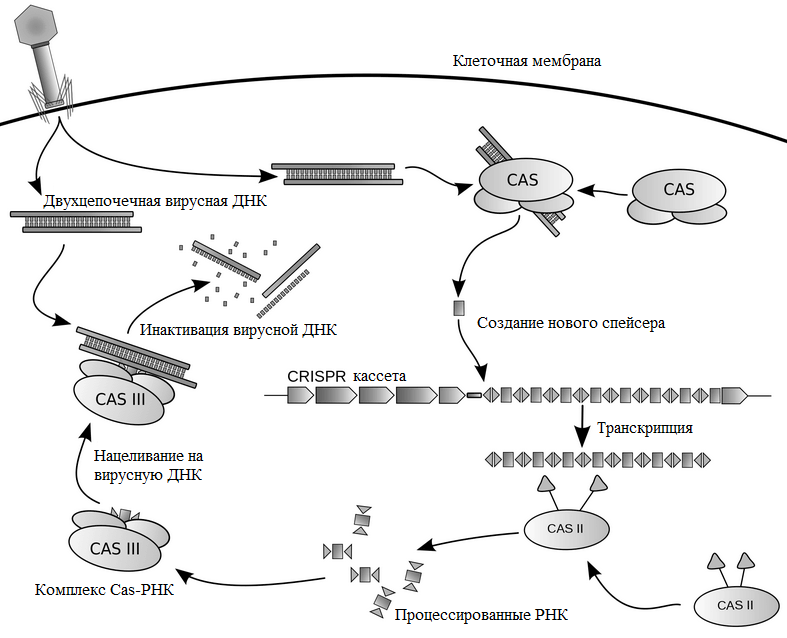
Иммунитет, обусловленный CRISPR/Cas, возникает за три стадии (рис. 3). В первой фазе бактерии или археи, у которых в геноме есть «блокнотик для записи» — CRISPR-кассета, — отвечают на появление вируса включением в конец кассеты коротких фрагментов чужеродной ДНК. На следующей стадии происходит транскрипция — считывание этой свежевключенной последовательности (образование описанных выше двух РНК) и обработка их нуклеазами. Теперь эти РНК могут специфично связаться с вирусной ДНК, и это взаимодействие через цепь событий приводит к ее расщеплению и «смерти» вредителя.
Рисунок 3. Схема работы комплекса Cas—РНК и CRISPR-кассеты
Грубо говоря, ситуация напоминает сказку про репку: первая РНК связывается с «репкой» — чужеродной ДНК — и «зовёт» вторую, вторая — специальный белок Cas9, который уже осуществляет двухцепочечный разрыв цепи чужой ДНК [22].
Несмотря на то, что в природе две РНК системы Cas9 разделены, учёные показали, что химерная РНК, представляющая собой сшитые в одну цепь вышеуказанные РНК, так же способна направлять Cas9 к ДНК-мишени. Более того, при соблюдении ряда условий можно менять последовательность первой внутри химерной РНК так, чтобы нацеливать Cas9 на желаемые гены.
Эта система даже проще TAL-эффекторов, поскольку для распознавания одного дезоксирибонуклеотида ДНК не нужен громоздкий «вагон» белка: один рибонуклеотид РНК легко и точно узнаёт комплементарный ему дезоксирибонуклеотид ДНК мишени! Экономия как в размере инструмента, так и в легкости его синтеза.
К настоящему времени показано, что эта система работает не только в археях и бактериях, но и в организмах рыб (Danio rerio), а также в клетках млекопитающих [23]. Уже установлено, что, как и в случае TAL-эффекторных нуклеаз, обработка ДНК Cas9-системой приводит к эффективному (10–30% случаев) возникновению мутаций.
Человек стремится покорить природу, и ключ для этого — ДНК. Но чтобы подобраться к ДНК и повлиять на нее, необходимо спуститься на молекулярный уровень и использовать белки или РНК. Сейчас развитие данных направлений идет стремительно, каждый месяц случаются значительные прорывы в этой области. Кто знает, какие чудеса ожидают нас через год? Возможно, будет найдена новая система, максимально упрощающая исходно сложный и кропотливый процесс вмешательства человека в работу природы.
12 методов в картинках: секвенирование нуклеиновых кислот
12 методов в картинках: секвенирование нуклеиновых кислот
Авторы
Редакторы
Секвенирование ДНК и РНК — это рутинный процесс, позволяющий, тем не менее, вникнуть в суть всего живого. Первоначально расшифровка генома была «развлечением» для избранных, а сегодня заказать эту услугу может каждая вторая научно-исследовательская лаборатория. С каждым годом проникнуть в дебри геномной, транскриптомной и эпигеномной информации становится все проще. Этот обзор посвящен основным принципам секвенирования нуклеиновых кислот и может послужить превосходным путеводителем как для любителя, изучающего основы молекулярной биологии, так и для специалиста, который планирует эксперимент и грезит научными прорывами.
12 биологических методов в картинках
Генеральный партнер цикла — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Партнер этой статьи — «СкайДжин»
Пять причин выбрать SkyGen:
Одна из главных миссий «Биомолекулы» — докопаться до самых корней. Мы не просто рассказываем, какие новые факты обнаружили исследователи — мы говорим о том, как они их обнаружили, стараемся объяснить принципы биологических методик. Как вытащить ген из одного организма и вставить в другой? Как проследить в огромной клетке за судьбой нескольких крошечных молекул? Как возбудить одну крохотную группу нейронов в огромном мозге?
И вот мы решили рассказать о лабораторных методах более системно, собрать воедино в одной рубрике самые главные, самые современные биологические методики. Чтоб было интереснее и нагляднее, мы густо проиллюстрировали статьи и даже кое-где добавили анимации. Мы хотим, чтобы статьи новой рубрики были интересны и понятны даже случайному прохожему. И с другой стороны — чтобы они были так подробны, что даже профессионал мог бы обнаружить в них что-то новое. Мы собрали методики в 12 больших групп и собираемся сделать на их основе биометодический календарь. Ждите обновлений!
Появление и развитие технологий секвенирования
С момента открытия нуклеиновых кислот прошло уже почти полторы сотни лет. В далеком 1869 году Иоганн Фридрих Мишер выделил из находившихся в гное клеток неизвестное доселе вещество, содержащее азот и фосфор, которое назвал нуклеином, а затем (из-за его свойств) — нуклеиновой кислотой. Первоначально считалось, что молекулы нуклеиновых кислот — резерв фосфора в клетках, однако уже в первой половине XX века ученые доказали их наследственную природу. Тогда же появилось понятие гена —наименьшей структурной и функциональной единицы наследственности, — и сформировалась новая наука — генетика.
Вплоть до середины прошлого века структура носителей генетической информации и способы ее передачи оставались неясными. Модель двойной спирали ДНК, которая входит во все современные учебники генетики и молекулярной биологии, предложили в 1953 году Френсис Крик и Джеймс Уотсон (за это в 1962 ученые получили Нобелевскую премию). Последовавшие следом открытие генетического кода и разработка центральной догмы молекулярной биологии дали мощный толчок к развитию естественных наук, в первую очередь — генетики. Основные исторические вехи этого процесса показаны на рисунке 1.
Рисунок 1. История геномных исследований и секвенирования нуклеиновых кислот. 8 марта 1865 г. — Грегор Мендель доложил результаты своих опытов, объясняющие механизм наследования. 1869 г. — Иоганн Фридрих Мишер выделил из клеток в гное неизвестное доселе вещество, содержащее азот и фосфор, которое назвал нуклеином. 1905–1909 гг. — появление терминов «ген» и «генетика». 1953 г. — Френсис Крик и Джеймс Уотсон предложили структуру двойной спирали ДНК. 1958 г. — Френсис Крик сформулировал центральную догму молекулярной биологии. 1975 г. — Сэнгер с коллегами разработал «плюс-минус» метод секвенирования ДНК. 1977 г. — группа Сэнгера разработала метод «терминаторов». 1977 г. — Максам и Гилберт предложили метод секвенирования ДНК путем химической деградации. 2001 г. — опубликован первый полный геном человека. 2005 г. — коммерциализация технологии пиросеквенирования. 2006 г. — коммерциализация технологии Solexa (Illumina). 2006 г. — коммерциализация технологии лигазного секвенирования. 2010 г. — коммерциализация технологии ионного полупроводникового секвенирования (технология PostLight TM ). 2011 г. — первый коммерческий релиз секвенаторов PacBio, основанных на технологии одномолекулярного SMRT-секвенирования. 2015 г. — начало продаж первых приборов, основанных на секвенировании через нанопору. Чтобы увидеть рисунок в полном размере, нажмите на него.
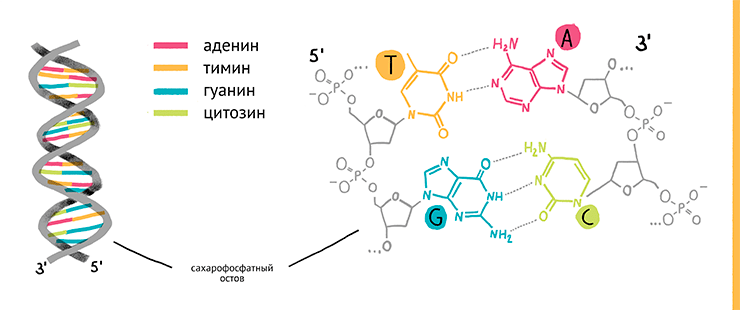
Осознав основные принципы функционирования нуклеиновых кислот (НК), научное сообщество предприняло грандиозные усилия для того чтобы разработать быстрые и эффективные методы определения их первичной последовательности (рис. 2) — как это принято говорить сегодня, секвенирования. Спустя десятилетия после открытия Уотсона и Крика в биологической науке наступила новая эпоха — эра секвенирования нуклеиновых кислот и геномики.
Рисунок 2. Секвенирование нуклеиновых кислот (другими словами, определение их нуклеотидной последовательности) — это расшифровка первичной структуры линейных молекул ДНК или РНК, состоящих из последовательности «букв» — нуклеозидтрифосфатов: дАТФ, дГТФ, дЦТФ, дТТФ и УТФ. Эти «буквы» зачастую именуют просто по азотистому основанию, входящему в их состав — аденин (А), гуанин (Г), цитозин (Ц), тимин (Т), а также урацил (У) в случае РНК.
Секвенирование белковых молекул
Кстати, секвенировать можно не только нуклеиновые кислоты, но и другие биополимеры — например, пептиды и белки, «сотканные» из аминокислотных остатков. Однако в этом спецпроекте мы предпочли подробно остановиться на секвенировании только нуклеиновых кислот и не затрагиваем отдельно тему белкового секвенирования.
Примечание от «Диаэм»: Белковое секвенирование методом Эдмана проводят на приборах Shimadzu в сочетании с ВЭЖХ.
Словарик
Почти четверть века назад в Соединенных Штатах стартовал грандиозный по своему масштабу научный проект, посвященный определению последовательности генома человека [1]. Основной его целью стала расшифровка генетической информации, заключенной в хромосомах (компактизованная ДНК), которые мы наследуем от своих родителей. В течение тринадцати лет многочисленные исследовательские группы по всему миру работали над определением полной последовательности генома человека. Почти три миллиарда долларов, потраченные на этот проект, открыли перед исследователями замечательные перспективы. Используя полученные данные, появилась возможность искать и находить участки ДНК, связанные с генетически обусловленными заболеваниями. И если природа многих моногенных болезней (вызываемых отказом единственного гена нашего генома) стала понятна уже давно, то некоторые заболевания — сердечно-сосудистые, онкологические, болезни Альцгеймера [2] и Паркинсона — являются многофакторными: вызвать их может широкий спектр изменений генома, многие из которых до сих пор неизвестны. Информация о генетических вариантах, связанных с человеческими недугами, позволяет формировать научно-обоснованный подход при их диагностике и лечении.
Расшифровка и аннотация (маркировка генов и других объектов в последовательности ДНК) генома человека поставили вопрос об использовании генетической информации как для диагностики заболеваний и их долговременного прогнозирования у человека, так и для исследования популяционной структуры сообществ, этногенеза и эволюционных процессов. Применение современных технологий секвенирования и генотипирования предлагает перспективные способы решения задач современной медицинской геномики и эпигеномики.
Такие результаты могут быть использованы при создании систем для проведения дифференциальной диагностики и выявления генетической природы заболеваний, для проведения персональной терапии и подбора методик лечения на основе анализа индивидуальных генетических характеристик. Решение таких задач тесно связано с разработкой эффективных алгоритмов и математических моделей для биоинформатической обработки данных геномного секвенирования и их использованием на базе суперкомпьютерных кластеров.
Геномные исследования позволяют решать массу задач как прикладного, так и фундаментального плана. Благодаря им разрабатываются новые лекарства и продукты, они же позволяют проникнуть в глубокую историю человечества [3] или понять причину массового вымирания видов.
Сейчас разработано несколько способов секвенирования НК. Самый популярный и надежный из них — секвенирование по Сэнгеру — позволяет «считывать» последовательности до 1000 пар оснований (п.о.) и используется для небольших фрагментов генома/генов или для валидации результатов более современного секвенирования нового поколения (next-generation sequencing, NGS), где размер одного прочитанного фрагмента варьирует от 25 до 500 п.о. В отличие от секвенирования по Сэнгеру, методы NGS используют для глубокого (многократного) прочтения генетического материала, которое необходимо, например, для ресеквенирования и сборки новых геномов (de novo), транскриптомных и эпигеномных исследований [4]. Помимо этого, NGS-секвенирование значительно производительнее, позволяя одновременно считывать миллионы и даже миллиарды коротких фрагментов. Такой рост производительности привел к возможности определения последовательности сразу десятков геномов (в зависимости от их размера) за один запуск прибора (рис. 3).
Рисунок 3. Современные технологии делают процесс секвенирования ДНК рутинной процедурой.
Стремительно развивающиеся новые технологии секвенирования ДНК позволяют быстро и эффективно определять особенности организмов на уровне их геномов. Главным итогом развития геномных и постгеномных технологий стало существенное расширение возможностей изучения генетической природы целого спектра заболеваний человека. Масштабные ассоциативные исследования на больших клинических выборках позволяют получать данные о генетических характеристиках, присущих конкретным группам людей (семьям, популяциям), развивая методы персонализированной медицины. В связи с этим, изучение механизмов генетической предрасположенности к многофакторным заболеваниям и выявление специфических генетических маркеров сегодня имеет особенную актуальность. Подобные методы широко применяются за рубежом и в России, где технологии современного секвенирования также постепенно внедряют в медицинские исследования и медицинскую практику с целью персонификации стратегии лечения [1].
Технологической основой для подобных исследовательских и сугубо прикладных проектов служат геномные секвенаторы (приборы, на которых проводят секвенирование), поставляемые различными коммерческими компаниями, такими как Illumina, Thermo Fisher Scientific, Oxford Nanopore Technologies, Pacific Biosciences и другие.
В 2017 году на рынке представлены сразу несколько перспективных разработок в области секвенирования НК. Эти подходы применены в секвенаторах нового поколения:
и некоторых других.
Современные технологии делают процесс секвенирования ДНК рутинной процедурой, особенно в том случае, когда речь идет об организмах с уже известной последовательностью генома — их последующая биоинформатическая обработка не представляет значительного труда, поскольку исследователь уже имеет референсный (ранее отсеквенированный) геном, который позволяет избежать ошибок при анализе полученных данных. При анализе нового, неопубликованного ранее, генома (de novo секвенирование и сборка) перед исследователем стоит ряд более сложных задач, в ходе решения которых он пытается сложить единичные фрагменты в цельную последовательность, задействуя многочисленные математические алгоритмы и суперкомпьютерные мощности [5], [6].
Однако наибольший интерес представляет не сама последовательность генома, а понимание того, как он функционирует: какие гены обеспечивают жизнедеятельность клетки, как происходит регуляция (включение или выключение генов) или какие генные пути начинают работать в ответ на стрессовые факторы.
Все современные секвенирующие платформы отличаются от метода секвенирования по Сэнгеру тем, что не требуют этапа клонирования фрагментов ДНК. Это экономит рабочее время и позволяет избежать ряда проблем с клонированием АТ-богатых участков. Общий принцип пробоподготовки для большинства современных (NGS) секвенаторов включает фрагментирование ДНК, привязку к субстрату, амплификацию фрагментов с помощью ПЦР (в одномолекулярном секвенировании от ПЦР удалось отказаться) и последующее считывании последовательности НК. В отличие от метода секвенирования по Сэнгеру, современные платформы обеспечивают параллельное проведение миллиардов реакций в малых объемах, что позволяет получить намного больший объем информации на выходе.
Рассмотрим основные технологии секвенирования нуклеиновых кислот подробнее.
Секвенирование по Сэнгеру
«Плюс-минус» метод секвенирования ДНК
Один из наиболее популярных методов секвенирования обязан своим появлением английскому биофизику Фредерику Сэнгеру (1918–2013) — единственному ученому в истории мировой науки, получившему сразу две Нобелевские премии по химии (в 1958 и 1980 годах). Первую премию присудили за установление структур белков, особенно инсулина, а вторую награду ему вручили в том числе и за разработку методов определения первичной последовательности нуклеиновых кислот.
Методику секвенирования ДНК с использованием радиоактивно меченых нуклеотидов и ДНК-полимеразы (или фрагмента Кленова ДНК-полимеразы I) предложили Сэнгер и его коллеги в 1977 году, причем с течением времени этот метод прошел несколько модификаций и к настоящему моменту считается золотым стандартом современного секвенирования.
Первоначально Ф. Сэнгер и Алан Коулсон разработали так называемый «плюс-минус» метод секвенирования ДНК [7], который можно подразделить на две основные стадии:
Рисунок 4. «Плюс-минус» метод секвенирования ДНК, предложенный Ф. Сэнгером и А. Коулсоном.
Секвенирование ДНК по Сэнгеру: метод «терминаторов»
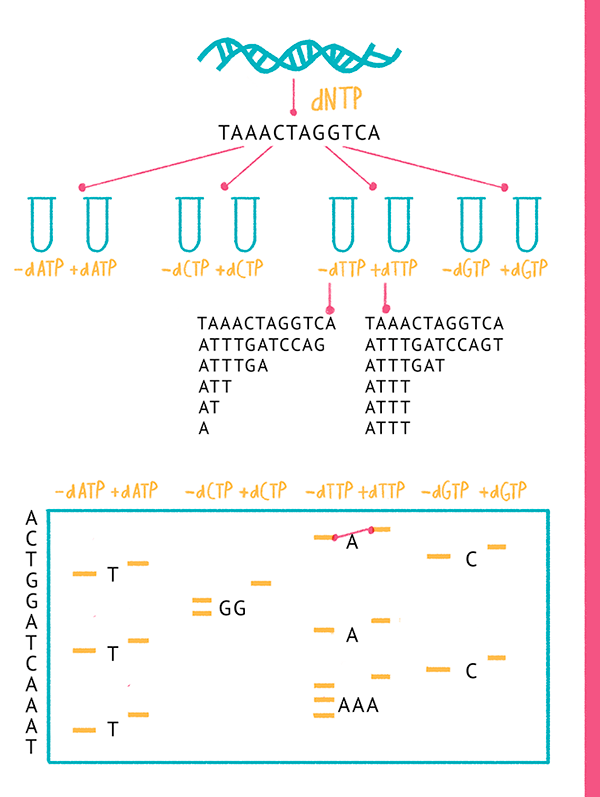
Спустя пару лет Сэнгер с коллегами предложил еще один способ секвенирования, получивший название метода «терминаторов» или метода «обрыва цепи» [9]. Суть этого метода заключается в том, что в реакционную смесь добавляют аналоги привычных нуклеотидов (дидезоксинуклеозидтрифосфаты), включение которых в синтезируемую цепь приводит к невозможности ее дальнейшего синтеза (терминации), а по образовавшемуся «обломку» можно установить последнюю букву секвенируемого фрагмента ДНК (рис. 5).
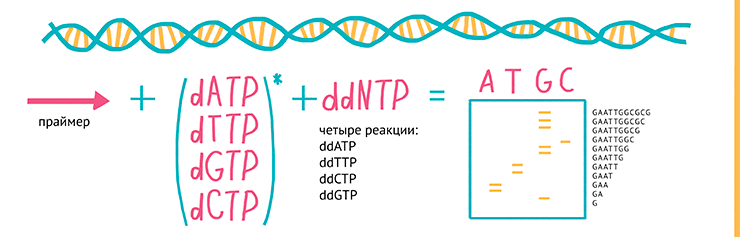
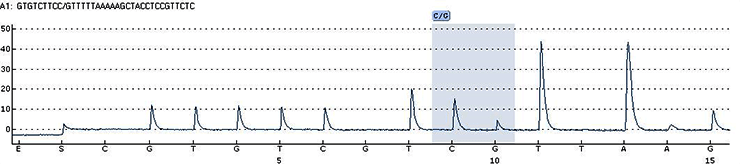
Рисунок 5. Метод «терминаторов»: используют ДНК-полимеразу, олигонуклеотидные праймеры и смесь четырех дезоксинуклеотидов (dNTPs) (А, Т, G и C), один из которых радиоактивно помечен по α-положению фосфата ( 32 P). В каждую из четырех реакций добавляется по одному 2’,3’-дидезоксинуклеозидтрифосфату (ddATP, ddTTP, ddCTP или ddGTP), которые терминируют дальнейшую реакцию (синтез комплементарной молекулы ДНК с матрицы) — таким образом в каждой пробирке образуется набор фрагментов ДНК разной длины, которые заканчиваются одним и тем же нуклеотидом. Затем полученные фрагменты визуализируют с помощью электрофореза и, сравнивая длины фрагментов из четырех реакций с ddATP, ddTTP, ddCTP или ddGTP, восстанавливают последовательность ДНК.
Автоматизированные модификации метода «терминаторов» активно применяют до сих пор в специальных приборах — секвенаторах. Открытие многочисленных флуоресцентных молекул позволило отказаться от использования радиоактивной метки и сделало возможным проведение реакции в одной пробирке. Реакционную смесь разделяют капиллярным электрофорезом, a выстроившиеся в синтезируемую цепочку ДНК меченые нуклеотиды затем регистрируют детекторами флуоресценции, предоставляя возможность считывать последовательность всего секвенируемого ДНК-фрагмента.
Секвенаторы по Сэнгеру: решения от «Диаэм»
Капиллярные секвенаторы ДНК Applied Biosystems (Thermo Fisher Scientific) — золотой стандарт секвенирования по Сэнгеру. Производительность — 4, 8, 24, 48 и 96 образцов. Они предназначены для секвенирования относительно небольших фрагментов ДНК длиной до 1000 нуклеотидов, характеризуются высокой точностью и используются для генотипирования человека, животных и других организмов (в том числе в медицине — трансплантологии, перинатологии, онкологии, фармакогенетике и др.), для выявления точечных мутаций, делеций и инсерций, для валидации мутаций, выявленных NGS-секвенированием, для анализа метилирования ДНК, для идентификации личности в криминалистике и др.
Новейшая разработка в этой области — капиллярный секвенатор SeqStudio (Applied Biosystems):
Первые впечатления пользователей нового капиллярного секвенатора SeqStudio
Материал предоставлен партнёром — компанией «Диаэм»
Другие методы секвенирования «старого поколения»
Кроме методов, предложенных Сэнгером, в конце прошлого века развивались и другие подходы к определению последовательности НК, которые — в частности, метод химической деградации, разработанный Максамом и Гилбертом [10], — не получили дальнейшего распространения из-за быстрого развития энзимологии (раздел биохимии, изучающий ферменты), которая предоставила преимущество методу «терминаторов» Сэнгера.
Использование секвенирования по Сэнгеру
Секвенирование по Сэнгеру позволяет «считывать» последовательности до 1000 пар нуклеотидов и применяется для небольших фрагментов генома/генов. В частности, оно используется для:
Наиболее популярными секвенаторами, использующими технологию секвенирования по Сэнгеру, являются приборы, производимые компанией Thermo Fisher Scientific: 3730xL, 3730, 3500xL, 3500, 3130xL, 3130, 310.
Следует отметить, что все описанные выше типы исследований сейчас можно проводить с помощью секвенирования «нового поколения», речь о котором пойдет в следующей главе, однако главные плюсы секвенирования по Сэнгеру — высокая точность (достоверность) полученных данных и невысокая стоимость работ при анализе небольшого количества ДНК-фрагментов — сохраняют актуальность этого типа определения последовательности НК.
Секвенирование «нового поколения» — next-generation sequencing (NGS)
За последние полтора десятилетия были разработаны, коммерциализированы и продолжают успешно развиваться совершенно новые технологии определения последовательности НК, в основе которых лежит стремление к миниатюризации, автоматизации, увеличению объема получаемых данных, а также удешевлению процесса. Появление NGS впервые позволило значительно ускорить и удешевить определение полной последовательности миллионов геномов организмов, начиная от бактерий и заканчивая человеком. Более того, появилась реальная возможность единовременно оценивать экспрессию (работу) тысяч генов в организмах, тканях и единичных клетках (секвенирование транскриптомов), а также анализировать регуляцию их активности (анализ экспрессии микроРНК и метилирования генома). В настоящее время на рынке представлено сразу несколько разработок, позволяющих определять последовательность полных геномов организмов, проводить анализ экспрессии генов и метилирования генома. Эти подходы реализуются на секвенаторах нового поколения производства коммерческих компаний Illumina, Thermo Fisher Scientific, Pacific Biosciences и Oxford Nanopore Technologies. Часть разработанных платформ уже ушли с рынка (например, GS FLX, 454/Roche или HeliScope/Helicos Bioscience); другие, пройдя несколько реинкарнаций и модификаций, прочно закрепились на нем (Illumina и Thermo Fisher Scientific); третьи только нащупывают почву, намереваясь занять свою нишу и найти своего потребителя (например, Oxford Nanopore Technologies).
Появление высокопроизводительных технологий секвенирования сопровождается прогрессом программного обеспечения — создаются алгоритмы с открытым программным кодом, появляются открытые источники данных и платформы для вычислений. Новые математические и информационные технологии позволяют геномике развиваться быстрее и использовать более сложные алгоритмы. Эти алгоритмы могут включать в себя сразу несколько приложений и программ и позволяют работать с очень большим объемом данных.
Секвенирование «нового поколения» применяется как для анализа геномов организмов, для которых уже доступен референсный геном (ресеквенирование), так и для того, чтобы впервые расшифровать геном организма (секвенирование de novo).
Для ресеквенирования успешно используют платформы, генерирующие большое количество коротких чтений (секвенируемых фрагментов ДНК), поскольку даже относительно короткие фрагменты ДНК успешно картируются (картирование, или выравнивание, — процесс биоинформатического поиска расположения конкретного короткого фрагмента в полной геномной последовательности) на референсный геном (последовательность ДНК в цифровом виде, составленную учеными как общий репрезентативный пример последовательности генома конкретного вида) при биоинформатическом анализе данных. Такие выравненные чтения могут использоваться для поиска однонуклеотидных полиморфизмов (SNPs), малых делеций и инсерций или других структурных изменений в геноме.
Что касается секвенирования de novo и сборки новых, ранее не прочитанных, геномов, то использование коротких чтений сильно усложняет сборку, особенно в случае больших по размеру и сложно устроенных геномов эукариот (например, полиплоидных геномов). В этих случаях используют комбинированный подход — сочетание платформ, генерирующих как короткие, так и длинные чтения. При сборке генома de novo ученые уподобляются ребенку, пытаясь правильно сложить элементы геномного пазла (короткие фрагменты отсеквенированной ДНК) в единую картину, созданную эволюцией за сотни миллионов лет (рис. 6).
Рисунок 6. Cеквенирование de novo и сборка новых, ранее непрочитанных, геномов требует значительных усилий.
В то же время наибольший интерес представляет отнюдь не сама последовательность генома, а понимание того, как он функционирует. Новые методы секвенирования НК позволяют оценивать уровень метилирования ДНК, проводить анализ дифференциальной экспрессии генов, в том числе и генов-регуляторов (например, микроРНК). Возможность анализа экспрессии генов в биологических системах открывает перед исследователем огромные возможности. Например, этот метод можно применять при исследовании функционирования центральной нервной системы человека (для понимания основных молекулярных аспектов работы головного мозга [11], [12]), при оценке защитного ответа клеток на атаки вирусов [13] или ответной реакции на стресс [14]. Не менее интересные данные может дать изучение регуляции экспрессии генов посредством анализа их метилирования [15] или изучение экспрессии некодирующих РНК [16], [17].
Оценка уровня метилирования генома, например, позволяет определить, какие генные пути и сети включаются в ответ на меняющиеся факторы окружающей среды; такие работы зачастую проводят для изучения эволюционных механизмов в живых системах. Изучение экспрессии кодирующих белки и некодирующих РНК в разных тканях и клетках также позволяет понять и описать гены, вовлеченные в жизнедеятельность клеток, органов и организмов.
Пиросеквенирование
Технологию предложил в 1996 году Пол Нирен с коллегами из Королевского технологического института в Стокгольме [19]. Затем ее коммерциализировали (2005 год) и воплотили в приборе GS FLX, 454 производства Roche (2008 год). Этим методом можно определять нуклеотидную последовательность фрагментов геномной ДНК размером 300–500 пар оснований (п.о.). Особо следует отметить тот факт, что подавляющее большинство NGS-методов требуют предварительной фрагментации ДНК для упрощения ферментативных реакций. К обоим концам фрагментированной ДНК «пришивают» ДНК-адаптеры (данная конструкция называется ДНК-библиотекой), необходимые для эмульсионной ПЦР (эПЦР) на магнитных сферах и последующего секвенирования.
Готовые ДНК-библиотеки иммобилизуют на магнитных сферах. Затем магнитные сферы с нанесенной на них клональной библиотекой доставляют на проточную ячейку, где в присутствии праймера, дезоксинуклеотидтрифосфатов и ферментов — ДНК-полимеразы, люциферазы, АТФ-сульфурилазы — происходит циклический синтез новой цепи.
Во время цикла пиросеквенирования при образовании фосфодиэфирной связи между матричной цепочкой ДНК и нуклеотидом синтезируемой цепи выделяется пирофосфат, который запускает каскад химических реакций, приводящих к выделению АТФ, необходимой для реакции окисления люциферина с выделением кванта света, который фиксируют аналоговой интегральной микросхемой (ПЗС-матрицей), состоящей из светочувствительных фотодиодов. Нуклеотиды, не вовлеченные в синтез новой цепи, удаляют из проточной ячейки, и начинается следующий реакционный цикл, в ходе которого добавляют дезоксинуклеотидтрифосфат другого типа (рис. 7).
Рисунок 7. Принцип пиросеквенирования. При включении нуклеотида в синтезируемую цепочку ДНК происходит регистрация высвобождающихся пирофосфатов — побочного продукта реакции полимеризации нуклеотидов в ДНК.
Пиросеквенирование от «Диаэм»
Принцип пиросеквенирования используется в секвенаторе PyroMark Q24, производимом компанией Qiagen. Этот прибор предназначен для одновременного прочтения 24 коротких последовательностей (до 100 нуклеотидов) и широко применяется в научных исследованиях и диагностике для точечного генотипирования и анализа метилирования. Основное достоинство секвенатора PyroMark — высокая точность и возможность анализа практически любого точечного полиморфизма.
Материал предоставлен партнёром — компанией «Диаэм»
Технология секвенирования на молекулярных кластерах с использованием флуоресцентно меченых нуклеотидов
Технология секвенирования на молекулярных кластерах, так же как и пиросеквенирование, подразумевает синтез новой молекулы ДНК по матрице. Этот метод начали разрабатывать еще в середине 90-х годов прошлого века химики Шанкар Баласубраманиан и Дэвид Кленерман из Кембриджа, изучавшие работу ДНК-полимеразы на молекулярном уровне, используя флуоресцентно меченые нуклеотиды и ДНК-матрицу, иммобилизованную на поверхности [20]. Творческие семинары в лаборатории и дружеские посиделки в баре привели к коммерциализации этой технологии в 2006 году под брендом Solexa, который спустя год был приобретен компанией Illumina. Сейчас платформа продолжает развиваться, и потребителям предлагают новые линейки приборов.
Суть метода заключается в следующем. К обоим концам предварительно фрагментированной ДНК лигируют адаптеры, необходимые для ПЦР и последующего секвенирования на молекулярных кластерах. Полученные ДНК-библиотеки иммобилизуют на поверхности проточной ячейки, где и проводят циклический процесс секвенирования. Реакционная смесь для синтеза комплементарной ДНК подается на поверхность проточной ячейки и содержит ферменты, олигонуклеотиды, а также четыре типа флуоресцентно меченых дезоксинуклеозидтрифосфатов. После включения в синтезируемую цепь ДНК нуклеотида-терминатора идентифицируют с помощью ПЗС-матрицы как тип включенного нуклеотида, так и его положение. Затем терминирующая группа и флуоресцентная краска отщепляются от нуклеотида, и цикл синтеза повторяется. Эта серия шагов продолжается определенное количество раз, число которых задает пользователь (рис. 8).
Рисунок 8. Принцип секвенирования на молекулярных кластерах: полимеризация (синтез «дочерней» цепочки) ДНК с использованием флуоресцентно меченых нуклеотидов внутри специальной камеры, регистрирующей флуоресценцию.
Размер чтений, получаемых с секвенатора, может достигать 300 п.о. (прибор Illumina MiSeq). Кроме того, серия секвенаторов 2017 года NovaSeq позволяет определять последовательность до 48 геномов человека за один запуск прибора.
Технология циклического лигазного секвенирования
Технология циклического лигазного секвенирования была разработана группой Джорджа Макдональда Черча [21] и, в отличие от представленных выше, использует метод лигирования (формирование химических связей между нуклеотидами при помощи специального фермента — лигазы). Данный подход к секвенированию НК коммерциализировали в 2006 году, и приборы, известные под брендом SOLiD, уже длительное время представлены на рынке (первоначально развитием этой системы секвенирования занималась компания Applied Biosystems, а затем Life Technologies и Thermo Fisher Scientific).
Суть метода заключается в определении нуклеотидной последовательности фрагментов геномной ДНК размером 25–75 п.о. К обоим концам предварительно фрагментированной ДНК лигируют адаптеры, необходимые для эПЦР на магнитных сферах и последующего секвенирования на проточной ячейке.
Магнитные сферы с нанесенной на них клональной библиотекой помещают на проточную ячейку, где и происходит секвенирование с помощью лигирования восьминуклеотидных зондов, несущих четыре различных флуорофора на 5’-конце. Флуоресценция считывается с помощью специальной камеры после каждого цикла секвенирования и, затем переводится в последовательность нуклеотидов (рис. 9).
Рисунок 9. Принцип лигазного секвенирования и последовательность зондов, которые используют при секвенировании. Зонды для секвенирования можно разделить на несколько участков (начиная с 3’-конца): первые два нуклеотида зонда лигируются к комплементарным участкам на секвенируемой ДНК-библиотеке, нуклеотиды с третьего по пятый — вырожденные (т.е. могут гибридизоваться с любыми тремя нуклеотидами секвенируемой ДНК-библиотеки). Нуклеотиды с шестого по восьмой также способны гибридизоваться с любыми тремя нуклеотидами секвенируемой ДНК-библиотеки, однако они отщепляются вместе с флуоресцентным красителем в конце каждого цикла секвенирования.
Технология лигазного секвенирования применялась в приборах, выпускаемых под брендом SOLiD. Спустя несколько поколений приборов пробоподготовку усовершенствовали, и на рынок вышла новая линейка приборов — 5500, 5500xl, а также 5500w, использующий изотермальную ПЦР (WildFire технология) для клонирования ДНК-библиотек [22].
Ионное полупроводниковое секвенирование
Технология, предлагаемая в этой приборной линейке, основана на использовании полупроводниковых микрочипов для секвенирования. Суть этого подхода весьма проста и заключается в регистрации локального изменения рН на микрочипе в момент удлинения синтезируемой цепи ДНК-полимеразой на ДНК-матрице (рис. 10).
Рисунок 10. Принцип полупроводникового секвенирования основан на обнаружении ионов водорода, которые выделяются во время полимеризации ДНК.
Секвенаторы нового поколения от «Диаэм»
Высокопроизводительные секвенаторы нового поколения Ion S5/S5 XL (Thermo Fisher Scientific) работают по технологии полупроводникового секвенирования Ion Torrent, которая обеспечивает простейшую процедуру таргетного секвенирования, высокую скорость и экономичность. Использование микрочипов различной производительности позволяет проводить на одном приборе анализ как отдельных генов, бактериальных геномов, так и экзомов и транскриптомов.
Материал предоставлен партнёром — компанией «Диаэм»
Пробоподготовка (приготовление ДНК-библиотек) напоминает таковую при циклическом лигазном секвенировании. Первоначально ДНК фрагментируют, затем к концам полученных фрагментов лигируют специфические ДНК-адаптеры, необходимые для эмульсионной ПЦР на магнитных сферах и последующего секвенирования.
Подготовка библиотек для NGS: решение от «Диаэм»
Выделение НК и подготовка библиотек для NGS — это довольно трудоемкий процесс, который включает множество шагов, занимает немало времени и требует максимальной сосредоточенности оператора. На помощь ученым-лаборантам приходят автоматизированные технологии на каждом из этапов пробоподготовки:
Материал предоставлен партнёром — компанией «Диаэм»
Одномолекулярное секвенирование
SMRT-секвенирование (single molecule real time sequencing), предложенное сотрудниками компании Pacific Biosciences, не только позволило отказаться от проведения полимеразной цепной реакции при пробоподготовке, но и дало возможность наблюдать за работой ДНК-полимеразы, наращивающей синтезируемую цепь, в реальном времени [23].
Создание платформы Pacific Biosciences не только решило проблему ПЦР-дупликатов, но и значительно увеличило длину чтений, что крайне важно при сборке геномов de novo. Суть метода заключается в определении нуклеотидной последовательности фрагментов геномной ДНК размером до 20 000 п.о. с лигированными к их концам специфическими ДНК-адаптерами, необходимыми для последующего секвенирования.
Сама реакция секвенирования молекул ДНК проходит в специальных ячейках (SMRT-ячейки) на прозрачной (кремниевой) подложке, с напыленным на нее слоем алюминия. В основе метода лежит использование технологии Zero-mode waveguide (ZMW) [24]. Сквозь дно в ячейку подается свет, однако благодаря особенностям ее строения, пучок фотонов не рассеивается, а освещает только конкретную часть (на подложке), где закреплена молекула phi29 ДНК-полимеразы. Эта полимераза была выбрана в качестве «считывающего» фермента благодаря своей высокой точности, скорости синтезирования дочерней цепи и эффективной работе с нуклеотидами, несущими флуоресцентную метку [25].
Смысл SMRT-секвенирования схож с описанными ранее методами NGS — ДНК-полимераза достраивает вторую цепь исследуемой молекулы ДНК, используя нуклеотиды, меченные различными флуоресцентными метками, которые регистрируют при помощи конфокальной микроскопии. В 2016 году анонсировали покупку платформы Pacific Biosciences биотехнологическим гигантом Roche Diagnostics, однако сделка так и не состоялась [26].
Разработка другого способа одномолекулярного секвенирования (коммерциализированного к настоящему времени) началась в конце прошлого века, когда группа американских ученых наглядно продемонстрировала возможность побуждать молекулы ДНК и РНК проходить сквозь ионный канал диаметром 2,6 нм в двуслойной липидной мембране под воздействием электрического поля. Более того, уже тогда исследователи сумели различать ДНК и РНК, а также оценивать длину входящих в нанопору олигонуклеотидов [27]. Спустя 13 лет впервые продемонстрировали возможность определения последовательности НК нанопоровым секвенированием [28], а затем данную технологию коммерциализировала и представила на рынок компания Oxford Nanopore Technologies (рис. 11).
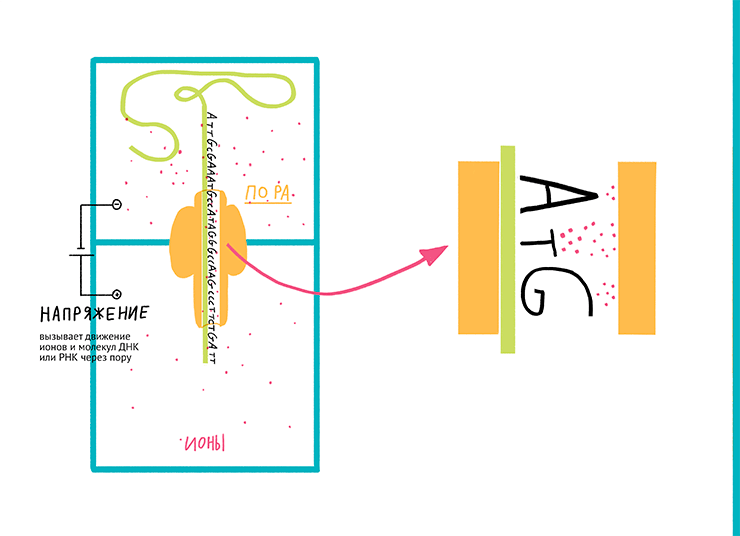
Рисунок 11. Принцип нанопорового секвенирования, коммерциализованный компанией Oxford Nanopore Technologies. Данный тип секвенирования основан на измерении меняющейся силы тока при прохождении молекулы НК сквозь нанопору в двухслойной мембране.
Суть работы нанопоровых систем (MinION, GridION X5, PromethION и SmidgION), предложенных британской компанией, достаточно проста. Реакционная камера, в которой проходит процесс считывания последовательности НК, разделена двухслойной мембраной с единичной порой. К камере прикладывается напряжение, вызывающее движение ионов и молекул ДНК или РНК через пору. При прохождении молекулы НК сечение поры (доступное для миграции ионов) уменьшается, в результате чего сила тока падает. Таким образом, считывая изменение силы тока, можно определять тип нуклеотида, проходящего через пору в конкретный отрезок времени.
Кроме описанных выше двух технологий компания Helicos Biosсiences пыталась продвинуть на биотехнологический рынок свою технологию одномолекулярного секвенирования — true Single Molecule Sequencing (tSMS). Данный подход во многом схож с технологией секвенирования на молекулярных кластерах (Illumina), однако позволяет обходиться без ПЦР при пробоподготовке.
Суть метода заключается в определении нуклеотидной последовательности фрагментов геномной ДНК размером до 50 п.о. К обоим концам предварительно фрагментированной ДНК лигируют адаптеры. Полученные ДНК-библиотеки иммобилизуют на поверхности проточной ячейки, где и проводят циклический процесс секвенирования. Один цикл состоит из удлинения синтезируемой на матрице цепочки за счет одного из четырех флуоресцентно меченых нуклеотидов, присоединение которого детектируется прибором.
Небольшая длина чтения (до 50 п.о., медиана — 30 п.о.) и большое количество ошибок (3–5%) данной платформы привели к оттоку потенциальных покупателей. Технология не получила широкого распространения, несмотря на потенциальную применимость в работе со сложными образцами, например, в палеогеномике [29], где отказ от ПЦР мог бы привести к сокращению процентного соотношение экзогенной (мусорной) ДНК в анализируемых образцах древней ДНК [30]. В итоге, в конце 2012 года компания Helicos Biosciences была признана банкротом и прекратила свое существование [31].
Одномолекулярное секвенирование длинных фрагментов ДНК может найти свое применение в самых разнообразных областях, и, что самое интересное, при работе с единичными клетками позволяет описывать их молекулярный «портрет» [32]. Это особенно важно при анализе транскриптомов клеток, позволяя описывать все возможные изоформы активных генов — благодаря длине чтений, недоступных для технологии Solexa или PostLight [33].
Секвенирование третьего поколения
Технологию одномолекулярного секвенирования можно также назвать технологией третьего поколения, поскольку она работает по принципу, совершенно отличному от того, который применяется в секвенаторах второго поколения. Кроме того, характерной особенностью таких секвенаторов является их сверхкомпактность. Например, самый компактный портативный секвенатор MiniION имеет вес всего 100 граммов и работает от USB 3.0 обычного компьютера или ноутбука. Первые приборы MiniION уже применяют и в России (официальный дистрибьютор Oxford Nanopore — компания «Диаэм»).
MiniION — портативный прибор для прямого секвенирования ДНК/РНК онлайн от Oxford Nanopore.
Для высокопроизводительного секвенирования Oxford Nanopore разработал приборы, в которые можно параллельно установить несколько секвенаторов MiniION:
В настоящее время Oxford Nanopore работает над созданием модели секвенатора SmidgION, который будет работать от обычного смартфона и сможет применяться в полевых условиях, где нет лаборатории и даже компьютера.
Материал предоставлен партнёром — компанией «Диаэм»
Партнер этой публикации — компания SkyGen: молодой игрок на рынке продукции для LifeScience-лабораторий в России и СНГ
У нас есть три основных принципа:
Бóльшая часть производителей в нашем портфолио — это прямые эксклюзивные поставщики. Мы являемся первым звеном в поставках для таких компаний как Agilent Technologies, New England Biolabs, Oxford Nanopore, QIAGEN, Macherey-Nagel, NIMAGEN, EdgeBio, Thermo Scientific, SIGMA-ALDRICH, Santa Cruz Biotechnology, ChemGenes, Bruker, Dornier, Bio Molecular Systems, Gilson, Opentrons, Titertek-Berthold.
В 2017 году компания «СкайДжин» стала официальным дистрибьютором нанопоровых секвенаторов Oxford Nanopore Technologies в России, Белоруссии и Казахстане. Наши специалисты окажут техническую поддержку и проведут обучение на месте. С нами технология нанопорового секвенирования стала доступной для вас!
Мы верим: чтобы быть близкими к вам, недостаточно просто выставлять счета и осуществлять доставку. Нам важно глубоко разобраться в теме и быть поддержкой для вас. Для этого мы публикуем новости, обзоры и высоко ценим любые замечания и критику. Каждый продукт мы «пропускаем» через себя. Анализируем плюсы и минусы, представляем, как и где он будет работать, консультируемся с вами. И, как результат, создаем методички, проводим семинары и презентации.
Сегодня мы предлагаем современные решения для проведения секвенирования на различных платформах — от капиллярного секвенирования и NGS до мономолекулярного анализа с технологией Oxford Nanopore. Выбор за вами!
Ознакомиться с потенциалом применения новой технологии нанопорового секвенирования MinION можно здесь.
Вы всегда можете обратиться к нам, связавшись с менеджерами или написав по адресу info@skygen.com, а также позвонив по телефону +7 (495) 215-02-22 или бесплатной линии 8 (800) 333-12-26.
Мы стараемся угнаться за вами в научном познании мира, мы стараемся учиться и расти вместе с вами!
Материал предоставлен партнёром — компанией «СкайДжин»
Использование секвенирования нового поколения
Производительность и относительная доступность NGS-методов привели к настоящей революции в биологической и медицинской науке. Более того, благодаря новым подходам появилась реальная возможность проводить ранее технически недоступные исследования. Использование секвенирования нового поколения позволяет проводить такие проекты как:
HLA-типирование с помощью NGS-методик
Примером практического применения таргетного секвенирования в медицинских целях может быть HLA-типирование — секвенирование генов главного комплекса гистосовместимости, ответственных за распознавание организмом клеток по типу «свой-чужой». HLA-типирование проводят при трансплантации, при патологиях беременности, при аутоиммунных заболеваниях и др. NGS, в отличие от других методов HLA-типирования (серологический анализ, методы SSP и SSO, секвенирование по Сэнгеру), позволяет получить полную последовательность генов главного комплекса и гистосовместимости и, соответственно, точный генотип.
Набор для HLA-типирования Holotype HLA от компании Omixon позволяет не только секвенировать эти гены, но и правильно интерпретировать результаты секвенирования. Этот продукт включает в себя реагенты для пробоподготовки и программное обеспечение HLA Twin для интерпретации и предназначен для всех современных моделей NGS-секвенаторов.
Материал предоставлен партнёром — компанией «Диаэм»
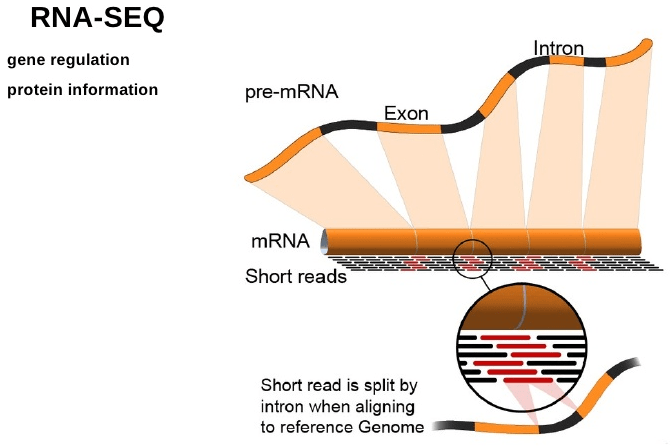
Решение по анализу транскриптома от «Диаэм»
Большим недостатком метода NGS является высокая стоимость реагентов. Однако на сегодняшний день можно найти на рынке относительно недорогую альтернативу: например, наборы Lexogen для анализа транскриптома. Это хорошее решение для полнотранскриптомного секвенирования, построения экспрессионного профиля, обогащения фракции мРНК и удаления нецелевых фракций РНК. Для интерпретации данных секвенирования хорошим помощником является программное обеспечение RNA-Seq от Lexogen.
Материал предоставлен партнёром — компанией «Диаэм»
Заключение
В наши дни происходит бурное развитие технологий, связанных с исследованием генов, белков и других молекулярных структур живых организмов. Разрабатываются портативные, быстрые, точные и универсальные методы исследований биологических объектов. Появление высокопроизводительных технологий секвенирования НК сопровождается развитием в области программного обеспечения, создаются алгоритмы с открытым программным кодом. Новые математические и информационные технологии позволяют геномике развиваться быстрее и использовать более сложные алгоритмы (например, нейронные сети).
На сегодняшний день объемы получаемой секвенаторами информации значительно обогнали возможности математического анализа получаемых результатов. Но даже несмотря на это, биомедицинская наука вовлечена в круговорот геномной революции, когда новые данные появляются ежедневно, а биотехнологические компании предлагают все новые и новые решения, значительно облегчающие диагностику заболеваний, приближая мир к новому направлению — персонализированной медицине [34].
Календарь
На основе статей спецпроекта мы решили сделать календарь «12 методов биологии» на 2019 год. Эта статья представляет апрель.