Mycobacterium avium и Mycobacterium avium-комплекс
 |
| Инфекция Mycobacterium avium. Микроскопическая картина ненекротической гранулёмы в лимфатическом узле в области шеи |
Микобактерии авиум (англ. и лат. Mycobacterium avium) — вид грамположительных неподвижных аэробных медленнорастущих кислотоустойчивых палочкообразных микобактерий, которые характеризуются высоким содержанием липидов в клетке и, особенно, в клеточной стенке. Mycobacterium avium являются типичными обитателями окружающей среды и, одновременно, возбудителями микобактериоза, оппортунистическими патогенами диких и домашних животных (свиней и др.), птиц и человека.
Относятся к так называемым нехромогенным нетуберкулёзным микобактериям (НТМБ).
Mycobacterium avium в гастроэнтерологии
Mycobacterium avium являются также возбудителями инфекционных заболеваний желудочно-кишечного тракта, в частности, инфекционного гастрита и дуоденита.
В МКБ-10 Mycobacterium avium выделен только как возбудитель лёгочной инфекции [A31.0].
Проект МКБ-11ß (от 20.01.2015) отдельными строками упоминают «Mycobacterium avium-intracellulare gastritis» («Гастрит, обусловленный инфицированием Mycobacterium avium») и «Non-tuberculous mycobacterial duodenitis» («нетуберкулезный микобактериальный» дуоденит). В классификации гастритов и дуоденитов, основанной на этиологическом принципе, предложенной Киотским консенсусом 2015 г. также имеются «Mycobacteria gastritis» («микобактериальный» гастрит) и «Mycobacterial duodenitis» («микобактериальный» дуоденит) (Sugano K. et al., Маев И.В. и др.).
Mycobacterium avium, в отличие от других микобактерий, в том числе, входящей в Mycobacterium avium complex (МАС) Mycobacterium intracellulare, способны проникать в организм человека не только через респираторный, но и через желудочно-кишечный тракт, попадая с пищей или водой в полость рта, способен сохраняться в кислой среде желудка и поражать слизистую кишечника.
При гастрите, вызванном Mycobacterium avium, наблюдаются следующие микроскопические изменения: в собственной пластинке монотонный инфильтрат из пенистых гистиоцитов, гранулёмы отсутствуют. А также имеет место позитивное окрашивание возбудителя прочными кислыми красителями.
Беррилл Бернард Крон (1884-1983), впервые (вместе с коллегами) описавший заболевание, впоследствии названное его именем, полагал, что его вызывает бактерия Mycobacterium avium subsp. paratuberculosis. Но при более поздних исследованиях это было опровергнуто.
МАС-инфекции желудочно-кишечного тракта у ВИЧ-инфицированных
Mycobacterium avium в современной систематике бактерий. Mycobacterium avium complex (МАС)
Вид Mycobacterium avium по современной систематике* входит в Mycobacterium avium complex (МАС), который относится к роду микобактерии (лат. Mycobacterium), семейству Mycobacteriaceae, порядку Corynebacteriales, классу Actinobacteria, типу Actinobacteria, Terrabacteria group, царству Бактерии.
Активность антибактериальных средств в отношении Mycobacterium avium и Mycobacterium avium complex
Лечение инфекций, вызванных микобактериями Mycobacterium avium complex вследствие природной множественной лекарственной устойчивости к большинству противотуберкулезных и других антибактериальных препаратов, обычно не применяющихся для терапии туберкулеза не просто. Лечение микобактериоза зачастую требует использования комбинации из нескольких препаратов, хирургического вмешательства или сочетания обоих методов. Попытки лечения больных с диссеминированными процессами, вызванными МАС, в большинстве случаев оказываются безуспешными. Природная множественная лекарственная устойчивость Mycobacterium avium обусловлена низкой проницаемостью клеточной стенки для лекарственных препаратов, поэтому условия, способствующие нарушению ее целостности, приводят к повышению лекарственной чувствительности микроба (Старкова Д.А.).
В профилактике и лечении различных форм нетуберкулезных микобактериозов, в том числе инфекции, вызванной Mycobacterium avium complex, свою эффективность доказали азитромицин и кларитромицин в комбинации с другими препаратами, например, с этамбутолом (Геппе Н.А. и др.).
Mycobacterium chimaera — причина инвазивной нетуберкулезной микобактериальной инфекции у пациентов, оперированных на открытом сердце
Mycobacterium chimaera — один из видов нетуберкулезных микобактерий, встречающихся повсеместно в почве и воде. Весной 2015 года в Швейцарии было выявлено шесть пациентов с инвазивной инфекцией Mycobacterium chimaera. Инфицированные пациенты подверглись хирургическому вмешательству на открытом сердце и у них использовалось загрязненное устройство регулирования температуры крови при искусственном кровообращении Stockert 3T. В июле 2015 года в клинике Пенсильвании также выявлены пациенты с инвазивной нетуберкулезной микобактериальной инфекцией, перенесшие хирургическую операцию на открытом сердце и у которых также использовалось устройство Stockert 3T. Stockert 3T — наиболее распространённое в США устройство, применяемое для нагрева или охлаждения крови при искусственном кровообращении.*
* CDC-MMWR. Notes from the Field: Mycobacterium chimaera Contamination of Heater-Cooler Devices Used in Cardiac Surgery — United States. October 14, 2016 / 65(40);1117–1118.
Mycobacterium avium complex что это
Насыщенная липидами клеточная стенка микобактерии обусловливает их кислотоустойчивость. Существует более пятидесяти видов микобактерии, большинство из которых присутствует в окружающей среде и не представляет опасности для человека.
Эпидемиология и патогенез туберкулеза (Mycobacterium tuberculosis)
Основной путь передачи туберкулёза — воздушно-капельный. Лёгкие являются первым органом, поражаемом при туберкулёзе. В месте проникновения возбудителя формируется воспалительный очаг (первичный комплекс), из которого инфекция может распространиться по всему организму (милиарное распространение). Заболевание может неожиданно разрешиться либо перейти в локализованный процесс (например, менингит).
Устойчивость к туберкулёзу обеспечивает Т-клеточное звено иммунитета. При его нарушении болезнь может рецидивировать (предполагаемый риск составляет 10%). Яркую клиническую картину заболевания чаще обнаруживают у пациентов со сниженным иммунитетом (например, у больных с ВИЧ-инфекцией).
Mycobacterium tuberculosis фагоцитируются макрофагами, но не инактивируются фаголизосомами, а размножаются в цитоплазме клеток. Выраженный иммунный ответ приводит к локальному разрушению тканей (образование полостей в лёгких — каверн) и возникновению симптомов, обусловленных цитокин-индуцированной системной воспалительной реакцией (лихорадка, потеря массы тела).
В качестве факторов вирулентности выступает большое количество антигенов, в том числе липоарабиноманнан (стимулятор цитокинов) и супероксиддисмутаза (обеспечивает выживаемость внутри макрофагов).
Клинические признаки туберкулеза
Возбудитель может поражать любой орган: он имитирует как воспалительные заболевания, так и злокачественные новообразования. Симптомы туберкулёза лёгких — хронический кашель, кровохаркание, лихорадка, потеря массы тела, рецидивирующая бактериальная пневмония. При отсутствии лечения болезнь переходит в хроническую форму, характеризующуюся постепенным ухудшением состояния.
При туберкулёзном менингите отмечают повышение температуры, помутнение сознания, при поражении почек — лихорадку, потерю массы тела, а также признаки локальной инфекции, осложнённой фиброзом мочеточников и гидронефрозом. Прогрессирование туберкулёза костей, обычно поражающего пояснично-крестцовый отдел позвоночника, характеризуется признаками вертебрального коллапса и сдавления нервов.
Кроме того, гной из очага инфекции может проникать под оболочку поясничной мышцы, в результате чего возникает паховый абсцесс. Поражение крупных суставов приводит к артриту и разрушению суставной ткани. При абдоминальной инфекции наблюдают брыжеечную лимфаденопатию, хронический перитонит, а также лихорадку, потерю массы тела, асцит, признаки нарушения всасывания в кишечнике. Диссеминированная (милиарная) инфекция может протекать без симптомов поражения лёгких.
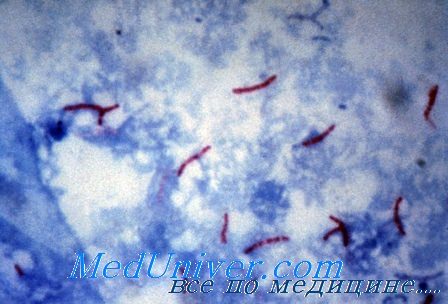
Лабораторная диагностика туберкулеза (Mycobacterium tuberculosis)
• Культивирование на средах, обогащенных липидами (яичные среды), или с добавлением малахитового зелёного (среда Левенштейна—Йенсена) для подавления роста других бактерий. Препарат окрашивают по методу Циля—Нильсена.
• Определение чувствительности штаммов на скошенной питательной среде Левенштейна—Йенсена.
• Молекулярно-генетические методы (помогает уточнить наличие гена ргоВ, идентифицировать туберкулёзный антигенный комплекс и определить устойчивость к рифампицину).
• Типирование Mycobacterium tuberculosis с помощью анализа полиморфизма длины рестрикционных фрагментов.
• Измерение уровня цитокинов периферической крови, продуцируемых моноцитами (для диагностики остроты процесса).
Лечение и профилактика туберкулеза
Для лечения туберкулёза лёгких применяют этамбутол в комплексе с пиразинамидом (в первые 2 мес) и рифампицин и изониазид (на протяжении 6 мес). При поражении других органов используют такую же схему лечения, основанную на способности лекарственного препарата проникать в различные ткани (например, в спинномозговую жидкость). В последнее время всё чаще выделяют мультирезистентные штаммы возбудителя туберкулёза.
Вероятность их обнаружения зависит от числа случаев неполного излечения, уровня жизни и др. В этом случае для лечения используют препараты второй линии: аминогликозиды, фторхинолоны, этионамид или циклосерин (после обязательного определения чувствительности возбудителя к антибиотикам).
Вакцинация аттенуированными (ослабленными) штаммами (вакцина для профилактики туберкулёза, синоним — вакцина Кальметт—Герена, БЦЖ) позволяет избежать милиарного распространения инфекции, но клинические исследования в некоторых странах не подтвердили её эффективности. Пациентам с высоким риском развития туберкулёза назначают профилактическое лечение рифампицином и изониазидом, а лицам с ВИЧ-инфекцией рекомендован приём рифабутина или кларитромицина в течение длительного времени.
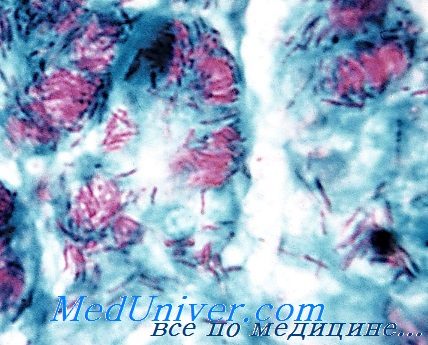
Возбудителя лепры (проказы) до настоящего времени не удалось культивировать на искусственных питательных средах.
Mycobacterium leprae вызывает поражение периферических нервов, сопровождаемое нарушением болевой чувствительности. Разрушение и деформация суставов и фаланг пальцев делают пациентов физически недееспособными. Итог заболевания индивидуален и зависит от иммунного ответа. В настоящее время выделяют три типа иммунного ответа при лепре:
• туберкулоидный (превалирует Thl-ответ);
• лепроматозный (преобладает Тh2-ответ);
• пограничный.
При туберкулоидном типе инфекции у пациентов развивается стойкий клеточный иммунитет, возникает большое количество гранулём, трофические поражения нервов. В тканях обнаруживают небольшое количество бактерий. Для лепроматозного типа характерен слабый клеточный иммунитет, отсутствие гранулём и генерализованная инфекция (леонтиаз, депигментация и нарушение чувствительности).
Диагноз основан на результатах микроскопического исследования препаратов поражённой кожи (окраска по Цилю-Нильсену) и биоптатов кожных покровов гистологического исследования. Для лечения применяют рифампицин, дапсон и клофазимин, эффективные на ранних стадиях заболевания, но неспособные препятствовать повреждению нервов и деформации конечностей, при возникновении которых необходимо хирургическое вмешательство.
Микобактерии не вызывающие туберкулез
Различные виды микобактерий могут вызывать локализованные или диссеминированные заболевания у лиц со сниженным иммунитетом. Некоторые из них могут инфицировать имплантируемые ткани.
Mycobacterium avium. В состав комплекса входят Mycobacterium avium, M. intracellular и М. scrofulaceum. Некоторые из них поражают птиц, других животных, являясь санрофитами окружающей среды. Их считают наиболее распространённой причиной микобактериального лимфаденита у детей, остеомиелита у пациентов со сниженным иммунитетом и пневмонии у лиц пожилого возраста. При прогрессирующей ВИЧ-инфекции эти микроорганизмы способны вызывать диссеминированные инфекции и бактериемию.
Возбудители из авиум-внутриклеточного комплекса устойчивы к действию большинства противотуберкулёзных препаратов, поэтому для лечения инфекций, вызванных ими, применяют методы комплексной терапии с использованием рифабутина, кларитромицина и этамбутола. При развитии лимфаденита иногда требуется хирургическое вмешательство.
Mycobacterium kansasi, M. Malmoense, M. Xenopi. Вызывают вялотекущую инфекцию лёгких, похожую на туберкулёз, у пациентов с хроническими заболеваниями лёгких (бронхоэктазией, силикозом, хронической обструктивной болезнью лёгких). Начальную терапию осуществляют с помощью стандартных препаратов после определения чувствительности микроорганизмов к антибиотикам.
Mycobacterium marinum, М. ulcerans. Mycobacterium marinum вызывают хронические гранулематозные инфекции кожи. Возбудитель обитает в реках, запущенных бассейнах и неухоженных садках для рыбы. Заболеванию свойственно возникновение множественных гнойничковых очагов, покрытых твёрдой коркой. Инфекции, вызванные М. ulcerans, распространены в сельскохозяйственных зонах Африки и Австралии. Бактерии обычно поражают нижние конечности, при этом обнаруживают папулёзные очаги, сопровождаемые изъязвлением и глубоким повреждением тканей (включая костную).
Видео диагностика и лечение микобактериоза. Д.м.н., профессор В.Н. Зимина
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Публикации в СМИ
Инфекция микобактериальная атипичная
Атипичная микобактериальная инфекция — комплекс гранулематозных поражений, вызываемых микобактериями, отличающимися от классических патогенов — возбудителей туберкулёза и лепры.
Этиология. Возбудители — кислотоустойчивые бактерии Mycobacterium ulcerans, M. marinum (M. balnei), M. kansasii, M. avium-intracellulare, M. xenopi, M. scrofulaceum.
Эпидемиология. Большинство возбудителей широко распространено в окружающей среде; некоторые обитают в воде и прибрежной зоне, вызывая заболевания у рыб, другие (например, Mycobacterium avium-intracellulare) — у птиц. Наиболее часто заражение происходит при вдыхании микобактерий, употреблении заражённых продуктов и проникновении возбудителя через микротравмы кожи и слизистых оболочек.
Патогенез. Проникшие микобактерии фагоцитируются макрофагами и транспортируются в регионарные лимфатические узлы; фагоцитарные реакции незавершённые, и возбудитель персистирует в цитоплазме макрофагов. Воспалительная реакция незначительная, но в месте проникновения развивается первичный аффект. В динамике по ходу регионарных лимфатических путей и узлов формируется первичный комплекс, характеризующийся развитием гранулём. Микроскопия биоптатов выявляет в последних очаги неказеозного некроза, содержащие кислотоустойчивые бактерии.
Клиническая картина
• Туберкулёзоподобные поражения. В патологический процесс вовлекаются лёгкие, почки, кожные покровы и костно-суставная система. Часто осложняют течение эмфизематозных процессов. У 40–50% больных с иммунодефицитными состояниями вызывают генерализованные поражения.
• Лимфадениты. Клинически чаще проявляются поражениями шейных лимфатических узлов (так называемые скрофулы); последние безболезненны, могут изъязвляться либо дренироваться наружу; системные проявления слабые или чаще отсутствуют.
• Кожные поражения. Типичным считают инфицирование ран конечностей, полученных при ударе о стенку бассейна или любой объект на дне и берегах водоёма. Чаще наблюдают образование изъязвляющейся гранулёмы, спонтанно ограничивающейся в течение нескольких недель, в более редких случаях формируется хроническая инфекция.
• Реже наблюдают хронические лёгочные поражения у лиц среднего возраста, зарегистрированные к настоящему времени повсеместно. Возможны бурситы локтевого сустава при повторных травмах и кожные поражения, цервикальные лимфадениты и синдром запястного канала у лиц с иммунодефицитами (наиболее часто после терапии гормональными препаратами).
Методы исследования • Выделение и идентификация возбудителя по скорости роста, образованию пигментов (на свету или в темноте) и патогенности для лабораторных животных • АТ к Mycobacterium kansasii перекрёстно реагируют с Аг Mycobacterium tuberculosis и у инфицированных лиц отмечают положительную реакцию Манту.
Дифференциальная диагностика • Лепра • Туберкулёз • Боррелиоз • Чума.
Лечение • При лёгочных поражениях •• Рекомендовано сочетание изониазида 600 мг, рифампицина 300 мг, стрептомицина 1 г и этамбутола 15–25 мг/кг 1 р/сут •• При поражении M. marinum — миноциклин по 100 мг каждые 12 ч в течение 6–8 нед •• При поражении M. kansasii и M. xenopi эффективна стандартная противотуберкулёзная терапия с обязательным назначением рифампицина •• Оперативное вмешательство рекомендовано при локализованных поражениях у пациентов молодого возраста без патологии других органов и систем • При лимфадените — у детей от 1 до 5 лет показано хирургическое лечение • При кожных поражениях, вызванных M. marinum, — тетрациклин (1–2 г/сут) и сочетание рифампицина и этамбутола в течение 3–6 мес • При инфекциях, вызванных ранами или инородными телами •• Хирургическая обработка раны и удаление инородного тела •• Лекарственная терапия: доксициклин (200–400 мг/сут), цефокситин (200 мг/кг/сут), амикацин (10–15 мг/сут) в течение 3–6 мес • При диссеминированных поражениях — сочетание противотуберкулёзных средств (как при лёгочных поражениях) лишь уменьшает бактериемию и временно ослабляет симптомы.
Течение и прогноз. Течение — прогрессирующее. Более чем у 20% пациентов отмечают рецидивы заболевания в течение 5 лет.
МКБ-10. A31 Инфекции, вызванные другими микобактериями
Код вставки на сайт
Инфекция микобактериальная атипичная
Атипичная микобактериальная инфекция — комплекс гранулематозных поражений, вызываемых микобактериями, отличающимися от классических патогенов — возбудителей туберкулёза и лепры.
Этиология. Возбудители — кислотоустойчивые бактерии Mycobacterium ulcerans, M. marinum (M. balnei), M. kansasii, M. avium-intracellulare, M. xenopi, M. scrofulaceum.
Эпидемиология. Большинство возбудителей широко распространено в окружающей среде; некоторые обитают в воде и прибрежной зоне, вызывая заболевания у рыб, другие (например, Mycobacterium avium-intracellulare) — у птиц. Наиболее часто заражение происходит при вдыхании микобактерий, употреблении заражённых продуктов и проникновении возбудителя через микротравмы кожи и слизистых оболочек.
Патогенез. Проникшие микобактерии фагоцитируются макрофагами и транспортируются в регионарные лимфатические узлы; фагоцитарные реакции незавершённые, и возбудитель персистирует в цитоплазме макрофагов. Воспалительная реакция незначительная, но в месте проникновения развивается первичный аффект. В динамике по ходу регионарных лимфатических путей и узлов формируется первичный комплекс, характеризующийся развитием гранулём. Микроскопия биоптатов выявляет в последних очаги неказеозного некроза, содержащие кислотоустойчивые бактерии.
Клиническая картина
• Туберкулёзоподобные поражения. В патологический процесс вовлекаются лёгкие, почки, кожные покровы и костно-суставная система. Часто осложняют течение эмфизематозных процессов. У 40–50% больных с иммунодефицитными состояниями вызывают генерализованные поражения.
• Лимфадениты. Клинически чаще проявляются поражениями шейных лимфатических узлов (так называемые скрофулы); последние безболезненны, могут изъязвляться либо дренироваться наружу; системные проявления слабые или чаще отсутствуют.
• Кожные поражения. Типичным считают инфицирование ран конечностей, полученных при ударе о стенку бассейна или любой объект на дне и берегах водоёма. Чаще наблюдают образование изъязвляющейся гранулёмы, спонтанно ограничивающейся в течение нескольких недель, в более редких случаях формируется хроническая инфекция.
• Реже наблюдают хронические лёгочные поражения у лиц среднего возраста, зарегистрированные к настоящему времени повсеместно. Возможны бурситы локтевого сустава при повторных травмах и кожные поражения, цервикальные лимфадениты и синдром запястного канала у лиц с иммунодефицитами (наиболее часто после терапии гормональными препаратами).
Методы исследования • Выделение и идентификация возбудителя по скорости роста, образованию пигментов (на свету или в темноте) и патогенности для лабораторных животных • АТ к Mycobacterium kansasii перекрёстно реагируют с Аг Mycobacterium tuberculosis и у инфицированных лиц отмечают положительную реакцию Манту.
Дифференциальная диагностика • Лепра • Туберкулёз • Боррелиоз • Чума.
Лечение • При лёгочных поражениях •• Рекомендовано сочетание изониазида 600 мг, рифампицина 300 мг, стрептомицина 1 г и этамбутола 15–25 мг/кг 1 р/сут •• При поражении M. marinum — миноциклин по 100 мг каждые 12 ч в течение 6–8 нед •• При поражении M. kansasii и M. xenopi эффективна стандартная противотуберкулёзная терапия с обязательным назначением рифампицина •• Оперативное вмешательство рекомендовано при локализованных поражениях у пациентов молодого возраста без патологии других органов и систем • При лимфадените — у детей от 1 до 5 лет показано хирургическое лечение • При кожных поражениях, вызванных M. marinum, — тетрациклин (1–2 г/сут) и сочетание рифампицина и этамбутола в течение 3–6 мес • При инфекциях, вызванных ранами или инородными телами •• Хирургическая обработка раны и удаление инородного тела •• Лекарственная терапия: доксициклин (200–400 мг/сут), цефокситин (200 мг/кг/сут), амикацин (10–15 мг/сут) в течение 3–6 мес • При диссеминированных поражениях — сочетание противотуберкулёзных средств (как при лёгочных поражениях) лишь уменьшает бактериемию и временно ослабляет симптомы.
Течение и прогноз. Течение — прогрессирующее. Более чем у 20% пациентов отмечают рецидивы заболевания в течение 5 лет.
МКБ-10. A31 Инфекции, вызванные другими микобактериями
Вышла статья Пановой А.Е. «Микобактериоз легких. Чем он опасен и как его лечить?»
В конце прошлого века микобактериоз называли «болезнью будущего» и рассматривали его как новую патологию, которая распространяется во всех странах мира, как бы вопреки усилиям, направленным на борьбу с туберкулезом. Сейчас микобактериоз превратился в серьезную реальность.
Повсеместно отмечаются изменения в эпидемиологии микобактериоза, связанные с увеличением количества людей, относящихся к группам риска, и в совершенствовании методов выделения и идентификации возбудителей микобактериоза. В какой-то степени он занимает «нишу», которую «освобождает» туберкулез при значительном снижении заболеваемости в последние годы.
Чаще всего микобактериоз является не самостоятельной болезнью, а осложнением, возникающим в результате нарушения работы каких-либо систем организма. Такая патология возникает после попадания в организм человека нетуберкулезных микобактерий (НТМ). Без современной диагностики, определения причины и терапии болезнь способна привести к непоправимым последствиям.
Что же это такое, в чем опасность и как справляться с микобактериозом, АиФ.ru рассказала заведующая отделением лабораторной диагностики ФГБУ «Национальный медицинский исследовательский центр фтизиопульмонологии и инфекционных заболеваний» Министерства здравоохранения Российской Федерации, врач-бактериолог, кандидат медицинских наук Анна Панова.
В чем суть проблемы?
Микобактериозы (МБ) — группа заболеваний, характеризующаяся поражением различных органов, с преимущественной локализацией в бронхолегочной системе, говорит специалист. «Особенностью этиологии микобактериозов является очень высокое разнообразие возбудителей, относящихся к группе нетуберкулезных микобактерий (НТМ). Такие постоянно обитают в окружающей среде. Так, они выявлены в воде: питьевой, бутилированной, в биопленках водопроводных труб», — говорит Анна Панова.
Сегодня насчитывается более 200 видов бактерий, из них около 70 являются факторами заболеваний человека в разных органах и системах, отмечает медик. Наибольшее значение в клинической практике имеют виды МАС, M. kansasii, M. fortuitum, M. abscessus и M. Chelonae.
В последние десятилетия заболеваемость и распространенность микобактериозов значительно увеличились, став серьезной проблемой общественного здравоохранения во всем мире. «Главным образом это связано с резким подъемом заболеваемости ВИЧ-инфекцией, что затем привело к увеличению показателя смертности от генерализованных форм инфекций, вызываемых НТМ. Наиболее частой причиной микобактериозов у ВИЧ-инфицированных больных является Mycobacterium avium complex (МАС). По частоте заболеваний этот вид далеко опережает все остальные нетуберкулезные микобактериозы и составляет более 95% случаев, а у лиц без ВИЧ-инфицирования — более 65% случаев», — отмечает Анна Панова.
Группы риска
Риску заражения наиболее подвержены:
Соответственно, с вопросами диагностики микобактериозов сталкиваются врачи самых разных специальностей.
Как заражаются?
«Человек источником инфекции не является, так как факт передачи НТМБ от человека к человеку не доказан. Т. е. человек от больного человека не заражается. В большинстве случаев источником инфекции для человека является окружающая среда (водопроводная вода, вода открытых водоемов, почва)», — говорит Анна Панова.
Основным природным резервуаром M. avium, отмечает специалист, служат открытые водоемы, M. Kansasii — водопроводная вода, M. xenopi — система горячего водоснабжения. Есть данные о том, что НТМ выделяются из биоматериала животных (крупный рогатый скот, свиньи) и птиц (голуби, воробьи, куры).
«Входными воротами для микобактерий являются дыхательные пути, кожные покровы, желудочно-кишечный тракт. Таким образом, отмечаются следующие механизмы передачи: аэрогенный, контактный, фекально-оральный. Естественная восприимчивость человека к НТМ довольно низкая и, как уже отмечалось, связана с иммуносупрессиями», — говорит бактериолог.
Симптомы проблемы
«К сожалению, нет какого-либо одного признака, характерного только для этого заболевания. Клинически, рентгенологически и гистологически микобактериозы весьма сходны с туберкулезом, и доказательный диагноз позволяют поставить лишь данные бактериологических и молекулярно-генетических методов. Диагностика микобактериозов имеет много общего с исследованиями на туберкулёз и, как правило, проводится одновременно с диагностикой туберкулеза в противотуберкулезных учреждениях. Но имеются важные особенности лабораторных исследований и интерпретации результатов», — отмечает Анна Панова.
Следует учитывать возможную транзиторную колонизацию слизистых оболочек верхних дыхательных путей НТМ из окружающей среды, в связи с чем выделение микроорганизмов данной группы не всегда является критерием для постановки диагноза.
Важна оценка клинического значения в следующих случаях:
«Для установления диагноза „микобактериоз“ необходимо выделение одного и того же вида НТМ не менее двух раз от одного пациента с учетом того, что исследование назначается при наличии симптомов заболевания», — говорит Анна Панова.
Но есть и исключения, когда для этиологического подтверждения диагноза «микобактериоз» достаточно однократного выделения НТМ. Это возможно, если:
«Для правильного установления диагноза и назначения адекватного лечения крайне важно не только выявить НТМ, но и определить их видовую принадлежность и лекарственную чувствительность», — говорит Анна Панова. Для этого необходимы современное высокотехнологичное оборудование и квалифицированный персонал в микробиологической лаборатории.
Как лечат
«Назначение терапии необходимо в тех случаях, когда имеет место выраженная симптоматика заболевания и определены микобактериологические аспекты микобактериозов. Лечение микобактериоза является еще более сложным по сравнению с лечением туберкулеза.
Он требует назначения многокомпонентной химиотерапии с большой продолжительностью курса (не менее 6-12 месяцев). Химиотерапия микобактериозов должна строиться на определении лекарственной чувствительности НТМ, что приведет к повышению эффективности лечения», — говорит Анна Панова.


