ВСЁ ПРО МЕДИЦИНУ
Липосомное железо – новое слово в лечении и профилактике анемии
Железодефицитная анемия (ЖДА) имеется почти у 25% населения планеты и является общенациональной проблемой здравоохранения многих стран. Это самая распространенная форма среди всех анемий. В высокоразвитых странах примерно 12% женщин страдают ЖДА, а у беременных ЖДА составляет от 20% до 80%. Скрытый дефицит железа встречается почти в два раза чаще, чем ЖДА, и составляет в странах Европы и в России 30-40%, а в некоторых российских регионах (Север, Северный Кавказ, Восточная Сибирь) достигает 60%. Распространенность дефицита железа зависит от возраста, пола, социально-экономических условий, наличия сопутствующих заболеваний.
Основные патологические изменения, возникающие при ЖДА и скрытом дефиците железа, связаны со снижением участия железа в тканевом дыхании, что оказывает на здоровье человека значительное воздействие. В программе ЮНИСЕФ «Micronutrient Initiative» показана взаимосвязь между ЖДА и увеличением материнской и младенческой смертности, задержкой умственного и психомоторного развития детей, ускорением развития и более тяжелым течением хронических заболеваний у взрослых и, особенно, пожилых пациентов.
Основными жалобами при ЖДА являются слабость, головокружение, головная боль, сердцебиение, одышка, обмороки, снижение работоспособности, сонливость. Кожные покровы становятся бледными, сухими, появляются трещины, заеды в углах рта, волосы становятся ломкими, интенсивно выпадают, ногти могут изменить форму, появляется мышечная слабость, изменения со стороны сердечно-сосудистой системы.
Количество железа в организме человека составляет 3-4 г. Основная часть железа (65%) находится в гемоглобине, 3,5% в миоглобине, 0,5% в составе тканевых ферментов, 0,1% в плазме крови, остальное (чуть более 30%) – в различных депо (костном мозге, селезенке, печени). Железо является незаменимым микроэлементом, абсолютно необходимым для нормальной жизнедеятельности человека. Железо в составе гема эритроцитов участвует в доставке кислорода в органы и ткани, входит в состав дыхательных ферментов и участвует в тканевом дыхании. Многие другие процессы также протекают с участием железа: синтез стероидов, метаболизм лекарственных препаратов, рост и формирование клеток, регуляция активности генов.
Биодоступность железа в составе традиционных препаратов колеблется от 2% до 15%. Особенно низка биодоступность у так называемых полимальтозатных (полисахаридных) комплексов трехвалентного железа (не более 4%).
Итальянские фармацевты из Pharmanutra совместно с Junia Pharma и компанией АО «Мединторг» вывели на российский рынок «СидерАЛ Форте», первый препарат липосомного железа для использования при анемии. Липосомная технология является настоящей инновацией и служит революционной альтернативой традиционным железосодержащим препаратам.
«СидерАЛ Форте» относится к группе специализированных продуктов лечебно-профилактического питания, что повышает его доступность для пациентов. На протяжении нескольких лет он занимает первое место в рейтинге железосодержащих препаратов в Италии и в некоторых других странах Европы.
Сложная технология включения пирофосфата трехвалентного железа внутрь фосфолипидной сферы обеспечивает хорошую переносимость и всасываемость железа, содержащегося в липосомах. Это повышает его биодоступность до 100%. наличие липосомной оболочки у «СидерАЛ Форте» позволяет избежать контакта железа со слизистой желудочно-кишечного тракта и предупреждает любые нежелательные окислительные эффекты в организме.
Каждая капсула «СидерАЛ Форте» содержит 30 мг железа в сочетании с витамином С. Препарат показан пациентам с железодефицитной анемией любого генеза, в том числе вследствие острой кровопотери или хронически низкой кишечной всасываемости, а также анемии, вызванной инфекционными или хроническими заболеваниями, то есть при таких формах анемии, при которых традиционные препараты железа неэффективны.
Производитель приложил большие усилия к разработке продукта и для применения у детей, выпустив «СидерАЛ капли» во флаконе с пипеткой. В каждой капле содержится 0,7 мг железа (7 мг железа на 1 мл). «СидерАЛ капли» рекомендован для детей в возрасте до 6 лет, в том числе для новорожденных с низким весом и недоношенных детей, которым всегда требуется дополнительное железо.
АО «Мединторг». 123103, Москва, Проспект Маршала Жукова, д. 74, корп. 2, +7 (495) 921-25-15 | msk@medintorg.ru
Лицензия на осуществление фармацевтической деятельности № ФС-99-02-003715 от 19 февраля 2014 года.
Липосомная форма железа в профилактике железодефицитных состояний у детей раннего возраста
Опубликовано в журнале:
«ПРАКТИКА ПЕДИАТРА»; март-аперль; 2015; стр. 10-14.
Е.В. Полевиченко, д. м. н., профессор, ГБОУ ВПО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава РФ, г. Москва
Естественной профилактикой железодефицитных состояний у детей первых месяцев жизни считается исключительно грудное вскармливание до 4-6 месяцев жизни. Концентрация железа в женском молоке невысока и составляет 0,2-0,4 мг/л, однако это обеспечивает потребности ребенка в железе благодаря его высокой биодоступности (50%). Физиологические потребности в железе детей раннего возраста, учитываемые при оценке алиментарных факторов риска развития ЛДЖ, приведены в табл. 1.
Таблица 1.
Физиологические потребности и рекомендуемые нормы потребления железа детьми 0-2 лет*
| Возраст потребности | Физиологические (мг/сутки) | Нормы потребления (мг/сутки) | |
| Россия | США | ||
| 0-3 мес. | 0,96 | 4,0 | 6,0 |
| 4-6 мес. | 0,96 | 7,0 | 6,0 |
| 7-12 мес. | 0,96 | 10,0 | 10,0 |
| 1-2 года | 0,61 | 10,0 | 10,0 |
При искусственном вскармливании для детей первого полугодия жизни используют молочные питательные смеси с относительно невысоким содержанием железа от 0,4 до 0,8 мг / 100 мл, так как ребенком еще используются пренатальные запасы железа. К 4-6-месячному возрасту ребенка они истощаются, и поэтому стандартное содержание железа в адаптированных молочных смесях для детей второго полугодия жизни возрастает до 0,9-1,3 мг / 100 мл. Для первичной профилактики железодефицитных состояний в качестве прикорма рекомендуются продукты промышленного производства, обогащенные железом (инстантные каши, вэллинги, фруктовые соки, фруктовые и овощные пюре). Для оценки пищевой обеспеченности ребенка железом и возможного восполнения его дефицита необходимо учитывать не только абсолютное содержание железа в продуктах рациона, но и уровень его всасывания и усвоения (табл. 2).
Таблица 2.
Содержание и биодоступность железа в продуктах детского питания*
| Продукты | Содержание железа, мг/100 г | Всасываемое железо, мкг/100 г | Всасывание железа, % |
| Женское молоко | 0,04 | 0,02 | 20-50 |
| Коровье молоко | 0,02 | 0,002 | 10 |
| Детская молочная смесь | 0,7-0,9 | 0,12 | 20 |
| Детская молочная смесь, обогащенная железом | 1,1-1,4 | 0,22-0,28 | 20 |
| Каши, обогащенные железом | 1,6-1,9 | 0,33-0,34 | 20 |
| Морковь | 0,5 | 0,02 | 4 |
| Говядина | 1,2 1,8 | 0,46 (всего) | 23 (гемовое) 8 (негемовое) |
Разнообразие педиатрических подходов к профилактике железодефицитных состояний детей раннего возраста в настоящее время суммировано в Клинических рекомендациях, разработанных ведущими отечественными экспертами с учетом общепризнанного международного опыта. В 2010 году Американская академия педиатрии (American Academy of Pediatrics) выпустила очередной пересмотр клинических рекомендаций по профилактике железодефицитных состояний у детей первого года жизни и детей раннего возраста (1-3 года). Основные положения этих рекомендаций сводятся к следующему:
Помимо широко применяемых и хорошо известных солевых и несолевых ферропрепаратов, обладающих доказанной клинической эффективностью, у детей 0-3 лет жизни для профилактики ЛДЖ в целях пищевой сапплементации могут использоваться также и продукты лечебно-профилактического питания. Новые возможности минимизации побочных эффектов перорального железа в жидкой форме предоставляет недавно зарегистрированный препарат Сидерал Капли (производство компании «Фарма Нутра», Италия), являющийся специализированным продуктом лечебно-профилактического питания. Он содержит уникальную комбинацию, необходимую для профилактики железодефицита: железо в легкоусваиваемой липосомальной форме. Действующим веществом Сидерала Капли является липосомный пирофосфат железа.
Сидерал Капли представляет собой инновационный и легкоусваиваемый источник железа, представленный в виде комплекса липосом. Запатентованная технология позволяет избежать побочных эффектов, столь распространенных при приеме препаратов железа, а именно: срыгиваний, неустойчивого стула, окрашивания слизистой оболочки рта и эмали зубов. Сидерал нетоксичен, поэтому может быть рекомендован во всех случаях дефицита железа, в том числе при беременности и кормлении грудью.
Сидерал Капли могут приниматься в неразбавленном виде либо могут быть разбавлены в половине стакана воды или другой жидкости комнатной температуры. Сидерал Капли могут профилактически вводиться в рацион питания у детей в случаях недоношенности, при слишком позднем отнятии от груди, а также при всех других стандартных показаниях, предусмотренных клиническими рекомендациями по профилактике железодефицитных состояний у детей раннего возраста.
НОВЫЕ ТЕХНОЛОГИИ В ЛЕЧЕНИИ ЖЕЛЕЗОДЕФИЦИТНОЙ АНЕМИИ
О.Н. МИНУШКИН, д.м.н., профессор, Г.А. ЕЛИЗАВЕТИНА, к.м.н., О.И. ИВАНОВА, к.м.н., Ю.С. БАРКАЛОВА
Центральная государственная медицинская академия Управления делами Президента РФ, Москва
НОВЫЕ ТЕХНОЛОГИИ
В ЛЕЧЕНИИ ЖЕЛЕЗОДЕФИЦИТНОЙ АНЕМИИ
В статье представлены сравнительные результаты лечения железодефицитной анемии специализированным продуктом лечебно-профилактического питания на основе комбинации липосомного железа и витамина С в суточной дозе 30 (1 капе.) и 60 мг (2 капе.) и комбинированного препарата двухвалентного железа и витамина С в суточной дозе 100 (1 табл.) и 200 мг (2 табл.) в течение 2-х мес. Получены приблизительно схожие результаты, но достигнутые меньшими дозами препарата липосомного железа при отсутствии побочных эффектов.
Ключевые слова: железодефицитная анемия, липосомное железо, двухвалентное железо, витамин С.
O.N. MINUSHKIN, MD, Prof., G.A. ELIZAVETINA, PhD in medicine, O.I. IVANOVA, PhD in medicine, Y.S. BARKALOV
FSBI CSMS of the RF President Affairs Management
NEW TECHNOLOGIES IN TREATMENT OF IRON-DEFICIENT ANEMIA
The article presents the comparative results of treatment of iron-deficient anemia by a specialized therapeutic and preventive product based on a combination of liposomal iron and vitamin C at a daily dosage of 30 (1 capsule) and 60 mg (2 capsules) and a combination drug of bivalent iron and vitamin C at a daily dose of 100 (1 capsule) and 200 mg (2 capsules) for 2 months. The approximately similar results were obtained but they were achieved by lower dosages of drug contained combination of liposomal iron and vitamin C in the absence of side effects.
Keywords: iron-deficient anemia, lyposomic iron, bivalent iron, vitamin C.
По данным литературы, ЖДА наблюдается у 30% населения планеты, а скрытый дефицит железа встречается в 2 раза чаще [3]. В некоторых российских регионах (Север, Северный Кавказ, Восточная Сибирь) латентный дефицит железа достигает 50-60%.
Есть надежды, что с открытием возможности определения уровня гепсидина будут синтезированы новые лекарства для больных, страдающих анемией. Если причиной нехватки железа является избыток гепсидина в организме, то синтез антигепсидина поможет этим больным.
В настоящее время выделяют 3 глобальные причины дефицита железа в организме:
■ недостаточное поступление с пищей (вегетарианство, анорексия), повышенная потребность в железе вследствие возрастания его утилизации (период роста и полового созревания ребенка, беременность, лактация);
■ нарушение всасывания железа в кишечнике (резецированные желудок и кишечник, целиакия, синдром ма- льабсорбции, синдром слепой петли кишечника, применение гормональных контрацептивов);
■ острые или хронические потери крови:
■ прежде всего из ЖКТ (скользящие диафрагмальные грыжи, варикоз вен пищевода, язвы, злокачественные опухоли, дивертикулез, геморрой);
■ из органов мочевыделительной системы;
■ мено- и метроррагии;
■ кровотечения вследствие применения НПВП, ГКС, антикоагулянтов, длительное донорство, программный гемодиализ, травмы.
У больных с воспалительными заболеваниями кишечника (ВЗК) (язвенным колитом (ЯК), болезнью Крона) наиболее часто комбинируются АХЗ и ЖДА [2].
На сегодняшний день главным звеном в патогенезе АХЗ считается гиперпродукция провоспалительных цитокинов, таких как ФНО-альфа, интерлейкины 1, 6, 10, гамма-интерферон. Они приводят к угнетению синтеза эритропоэтина и значительно снижают его эффекты, направленные на усиление пролиферации и созревания эритроидных предшественников, а также усиливают свободнорадикальные реакции и процессы апоптоза 11. Выраженность анемии при ВЗК может усиливаться вследствие действия других факторов (повторных эпизодов кровопотерь, влияния лекарственных средств, дефицита витаминов и др.).
Таким образом, достижение успеха в лечении ЖДА невозможно без терапии основного заболевания, устранения, по возможности, этиологического фактора, снижения активности патологического процесса и коррекции самой анемии. Лечение анемии должно быть комплексным и включать оптимизацию питания и назначение современных препаратов железа, эффективность которых зависит от выбора препарата и способа его введения.
Основным источником железа для человека являются продукты животного происхождения. В природе железо существует в двух химических формах: закисное 2-валентное (гемовое) и окисное 3-валентное (негемовое). Гемовое железо хорошо всасывается в кишечнике. Наиболее богаты гемовым железом мясо, особенно говядина, кровяная колбаса. В птице и рыбе гемового железа меньше. Печень (свиная и телячья), почки, сердце, ливерная колбаса богаты ферритином и гемосидерином, содержащими негемовое железо (последнее плохо всасывается в ЖКТ). Много негемового железа содержится в некоторых марках красного вина, фруктовых соках, яблоках, гранатах, гречневой крупе, молочных продуктах, яйцах, орехах и шоколаде. Биодоступность такого железа минимальна, и все эти продукты не являются источником железа [18]. Вегетарианство является мощным фактором риска ЖДА в любом возрасте. При этом в рацион должны входить зелень, овощи, фрукты, т. к. усвоение железа улучшается при наличии в пище витамина С. Аскорбиновая кислота препятствует окислению железа, тем самым способствуя его всасыванию. Всасывание железа ухудшают танин (содержащийся в чае и кофе), фитин (содержащийся в рисе, соевой муке), молоко и творог из-за высокого содержания кальция.
Поскольку усвоение железа из пищи ограничено, медикаментозная терапия анемии является основной. Гемотрансфузии в лечении тяжелой анемии могут использоваться только по жизненным показаниям, т. к. железо плохо утилизируется из перелитых эритроцитов. Показанием к проведению трансфузии крови является не столько уровень гемоглобина, сколько состояние гемодинамики.
Принципы лечения ЖДА были сформулированы Л.И. Идельсоном в 1981 г. и сегодня остаются основополагающими. Они включают следующие положения:
■ эффекта невозможно добиться только с помощью диеты;
■ препараты железа следует назначать преимущественно внутрь, до еды;
■ исключение для инъекционных форм железа делается в случаях выраженного нарушения всасывания железа в ЖКТ и при абсолютной непереносимости энтерального железа;
■ улучшение показателей крови еще не означает, что в организме восстановлен запас железа;
■ после нормализации уровня гемоглобина следует продолжить прием железа еще 1-2 мес. с уменьшением суточной дозы наполовину, чтобы наполнить депо.
Лечение препаратами железа должно быть длительным и зависит от исходной тяжести анемии (уровня гемоглобина и дефицита железа).
Существенным недостатком парентерального применения железа является то, что необходимо использовать строго рассчитанное количество препарата. Врач может назначать инъекционные препараты только в условиях стационара. При применении инъекционных форм чаще наблюдаются побочные эффекты вплоть до анафилактического шока, возможны аллергические реакции, передозировка железа, системный и локальный сидероз, высок риск лекарственного отравления. Предпочтение следует отдавать внутривенному пути введения. В настоящее время чаще всего используют (100 мг в 5 мл) ликферр 100. Препараты железа для парентерального введения находятся в 3-валентной форме в отличие от пероральных препаратов.
Основой патогенетической терапии ЖДА является применение препаратов железа внутрь. Безопасность этого способа приема достоверно выше, чем безопасность парентерального. При этом целесообразно, чтобы суточная доза 2-валентного железа составляла 100-300 мг/сут (Идельсон Л.И., 1981). В связи с этим при выборе препарата железа и определении его суточной дозировки клиницисты ориентируются не только на общее содержание в нем соли железа, но и на количество элементарного железа, содержащегося в данном препарате [13]. В настоящее время имеется большой выбор железосодержащих препаратов. Для повышения биодоступности и улучшения переносимости железа фармакологическими фирмами используются различные методические подходы: поддержание железа в 2-валентном состоянии, использование «носителей», усиление гемопоэза, утилизации и абсорбции железа, обеспечение независимости абсорбции от рН среды и активности ферментов.
Лекарственные препараты железа различаются количеством содержащихся в них солей железа, в т. ч. 2-валентного, наличием дополнительных компонентов (аскорбиновая и янтарная кислоты, витамины, фруктоза и т. д.), лекарственными формами (таблетки, драже, сиропы, растворы), переносимостью, стоимостью.
При выборе лекарственного препарата и оптимального режима дозирования необходимо помнить, что адекватный прирост показателей гемоглобина при ЖДА может быть обеспечен поступлением в организм от 30 до 100 мг 2-валентного железа. Учитывая, что при развитии ЖДА всасывание железа увеличивается на
2- валентного железа в сутки. Применение более высоких доз не имеет смысла, поскольку всасывание железа при этом не увеличивается.
Степень абсорбции 2-валентных солей железа в несколько раз выше, чем 3-валентного, поэтому препараты, содержащие 2-валентное железо, дают быстрый эффект и нормализуют уровень гемоглобина в среднем через 1-2 мес., а нормализация уровня железа в депо происходит через 3-4 мес. от начала лечения и зависит от степени тяжести анемии и дозы препарата. Требуется более длительное применение препаратов, содержащих железо в 3-валентном состоянии, в случае дефицита меди в организме они будут неэффективны. Нормализация уровня гемоглобина при лечении препаратом
Основные требования к проведению лечения препаратами железа:
■ достаточное содержание элементарного железа в препарате;
■ использование соли железа, обеспечивающей его наибольшую биодоступность;
■ введение с препаратом железа аскорбиновой кислоты, повышающей биодоступность препарата, а также витаминов: фолиевой кислоты, цианокобаламина, играющих важную роль в гемопоэзе; недостаток этих витаминов вызывает нарушение синтеза ДНК в кроветворных клетках, что негативно влияет на скорость синтеза гемоглобина.
В 2014 г. на фармацевтическом рынке России зарегистрирован специализированный продукт в качестве лечебно-профилактического питания при анемии на основе комбинации Липосомного железа и витамина С. В 1 капсуле содержатся 30 мг пирофосфата железа в липосомальной форме, 70 мг аскорбиновой кислоты. Преимущества препарата [17]:
■ нетоксичен, показан к применению у беременных женщин;
■ альтернатива инъекционным формам железа, что подтверждено европейскими клиническими испытаниями;
■ рекомендован при железодефицитных состояниях любой степени тяжести;
■ отсутствие проокисляющего действия железа;
■ снижает уровень воспалительных маркеров (СРБ).
В 2015 г. на кафедре терапии и гастроэнтерологии ФГБУ ДПО ЦГМА УД Президента РФ [19] проводилось сравнительное исследование эффективности липосомного железа и 2-валентного железа при ЖДА у разных категорий больных.
Больные с ЖДА легкой и средней степени тяжести получали препараты в течение 2-х мес. Оценивались скорость наступления эффекта, динамика уровня гемоглобина и эритроцитов, а также переносимость препаратов.
Лечение осуществлялось в режиме монотерапии. Эффективность препаратов оценивалась по следующим критериям:
■ динамика уровня гемоглобина через 2 нед., 1 и 2 мес. лечения по сравнению с исходным значением;
■ частота нормализации уровня гемоглобина крови через 2 нед., 1 и 2 мес. приема вышеуказанных препаратов;
■ динамика уровня ретикулоцитов крови через 2 нед., 1 и 2 мес. по сравнению с исходным значением;
■ динамика уровня сывороточного ферритина, транс- феррина, сывороточного железа через 2 мес. лечения по сравнению с исходными значениями;
■ переносимость и нежелательные явления применения препаратов.
В исследование были включены 80 пациентов мужского и женского пола с ЖДА легкой и средней степени тяжести (уровень гемоглобина 10 г/л (15 чел.)
Сывороточное железо (мкмоль/л)
7,9 ± 1,9 р 10 г/л (19 чел.) 47,5%
Сывороточное железо (мкмоль/л)
GlobiFerr не токсичен, поэтому может быть рекомендован во всех случаях дефицита железа, в том числе при беременности и кормлении грудью.
Новое поколение препаратов железа – бисглицинат (хелат) железа
Распространенность анемии
Значимость анемии как проблемы современного мира не вызывает сомнений. Несмотря на все достижения цивилизации, дефицит железа является основным и наиболее распространенным нарушением питания в мире. Дефицит железа, от которого страдают многие дети и женщины в развивающихся странах, является единственным видом недостаточности питательных веществ, который также в значительных масштабах распространен в экономически развитых странах. Уровни его распространенности поражают: 2 миллиарда человек, то есть более 30% населения мира, страдают от анемии. 1
Среди анемий ведущими являются железодефицитные, составляя в структуре у женщин до 90% и среди мужчин — до 80%. Важным является высокая распространенность среди населения латентного дефицита железа, которая колеблется от 19,5% до 30%, кроме того, от 50% до 86% женщин имеют факторы риска развития анемии.
Железодефицитная анемия (ЖДА) — заболевание системы крови, обусловленное дефицитом железа в организме, сопровождаетcя изменениями параметров его метаболизма, уменьшением концентрации гемоглобина в эритроцитах, количественными и качественными их изменениями и клинически выражается анемической гипоксией и сидеропенией.
Сидеропения и развивающаяся в последующем тканевая и гемическая гипоксия приводят к расстройствам сердечно-сосудистой (миокардиодистрофия и нарушение кровообращения различной степени), нервной системы (вегетативно-сосудистые, вестибулярные нарушения, астенический синдром), снижению детородной функции женщин, а также развитие осложнений во время беременности и родов, изменению интеллекта и поведенческих настроений, хронизацию различных заболеваний и как следствие снижение работоспособности и ухудшение качества жизни. 4
Эволюция синтетических лекарственных средств терапии железодефицитной анемии
Фармакотерапия ЖДА базируется на введение в организм железа из состава железосодержащих лекарственных средств. Выбору препарата для коррекции сидеропении придается особое значение, так как важна не только эффективность, но и отсутствие побочных реакций и осложнений при их применении.
Существует условное деление препаратов железа на двух- и трёхвалентные. Однако, сама по себе валентность железа не представляет какой-либо ценности.
Известно, что всасывание железа в кишечнике возможно лишь тогда, когда микроэлемент находится в двухвалентной форме, которая способна проходить через клеточную мембрану слизистой оболочки кишечника. Низкое значение рН желудочного содержимого способствует растворению алиментарного железа и переходу трехвалентного железа (окисное) в двухвалентную форму (закисное). 17
При поступлении желудочного содержимого в кишечник рН пищевого комка повышается и в отличие от ферро-иона (Fe2+), ферри-ион (Fe3+) образует нерастворимые соли. В этих условиях только муцин, хелатируя железо, способен поддержать ферри-ион в растворимом состоянии. 4
Таким образом, соединения железа в составе препаратов должны обладать хорошей растворимостью, высокой биодоступностью, достаточным содержанием элементарного железа и малой токсичностью. Рассмотрим особенности абсорбции каждой из трёх известных групп препаратов железа.
Первое поколение препаратов железа
Одной из первых групп препаратов железа стали применять ионные соли двухвалентного железа. Эта группа характеризуется довольно быстрым наступлением эффекта в плане повышения гемоглобина и улучшения гемодинамических показателей в периферической крови.
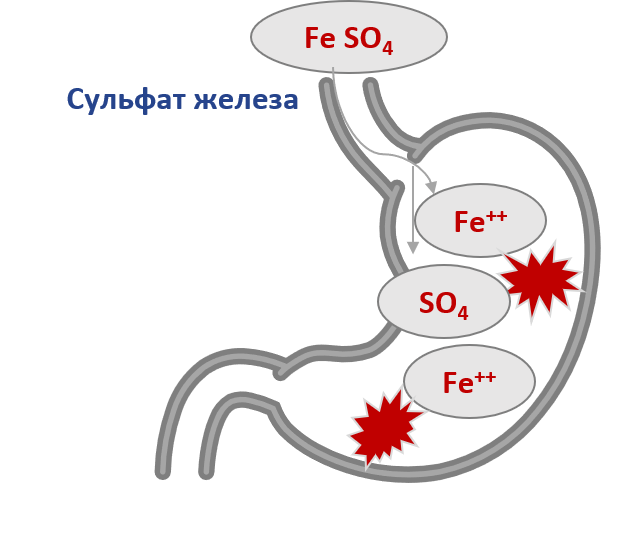
Тем не менее, лечение ионными препаратами железа, в частности сульфатом железа, вызывает побочные реакции у 44,7% пациентов. Чаще всего страдает желудочно-кишечный тракт (ЖКТ). Симптомы дисфункции его верхних отделов обычно проявляются в течение часа после приема лекарства и могут протекать как в легкой (тошнота, дискомфорт в эпигастрии), так и в тяжелой форме — с болью в животе и/ или рвотой. Кроме того, ферротерапия солевыми препаратами железа нередко сопровождается появлением металлического привкуса в течение первых дней лечения, потемнением зубной эмали и десен, возможны также диарея или запор. хорошо известно, что солевые препараты железа в просвете кишечника взаимодействуют с компонентами пищи, лекарствами, затрудняя абсорбцию в том числе и железа. В связи с этим, их рекомендуют назначать за 1 час до приема пищи, однако это усиливает повреждающее действие соединений Fe2+ на слизистую кишечника, вплоть до развития ее некроза. 5
Причиной возникновения данных побочных явлений является гидролиз солей железа в желудке. Под действием желудочного сока ионные соли железа подвергаются гидролизу(диссоциации) в желудке, в результате чего свободные молекулы железа негативно воздействуют на слизистую оболочку ЖКТ и провоцируют возникновение побочных эффектов: тошнота, боль в животе, металлический привкус во рту, диарея/запор.
Второе поколение препаратов железа
Абсорбция железа в виде гидроксид-полимальтозного комплекса (ГПК) железа-III имеет принципиально иную схему по сравнению с его ионными соединениями и осуществляется путем активного всасывания при конкурентном обмене лигандами, уровень которых определяет скорость абсорбции железа Fe3+. Неионная структура, обеспечивающая стабильность комплекса и перенос железа с помощью транспортного белка, предотвращает в организме свободную диффузию ионов железа, то есть прооксидантные реакции. Однако биодоступность полимальтозного комплекса железа-III самая низкая среди всех препаратов железа, всего 10–15%.
В связи с большим размером молекулы (55 kDa), ее пассивная диффузия примерно в 40 раз медленнее, чем у ионов железа. 6 Такую низкую биодоступность приходится компенсировать большими суточными дозами ГПК.
Новое поколение препаратов железа — новое решение проблемы анемии
С конца 90-х начала 2000-х годов начали активно внедрять применение хелатных комплексов железа для терапии дефицита железа и анемии у людей. Хотя данная группа препаратов появилась гораздо раньше, и использовалась изначально в качестве пищевых добавок и в ветеринарии.
В 1893 году Альфред Вернер выдвинул постулат о новой молекулярной структуре, характеризующей эти стабильные молекулы. Спустя несколько лет, в 1920 году Морган и Дрю применили термин «хелат» к молекулярной структуре, постулированной Вернером. 7
Хелаты металлов представляют собой комплексные соединения металла с аминокислотой.
В отличие от солей металлов, лиганд в хелатном комплексе отдает электроны катиону, делая тем самым молекулу ионно-нейтральной, устойчивой к разным факторам, действующим в желудочно-кишечном тракте (рН, пища), а низкая молекулярная масса способствует максимальному усвоению железа при пероральном приеме. 8
Хелатные комплексы легче проникают через стенку кишечника и лучше усваиваются, не нарушая ионный и минеральный баланс клетки. 10
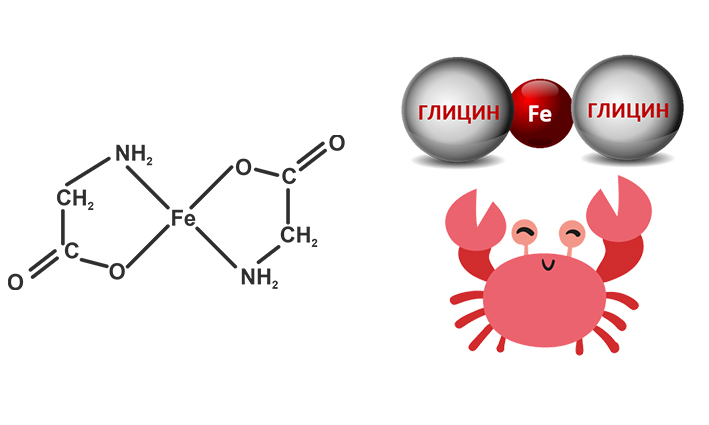
Бисглицинат железа состоит из одной молекулы железа, которая соединена с карбоксильными группами двух молекул глицина при помощи ковалентных связей.
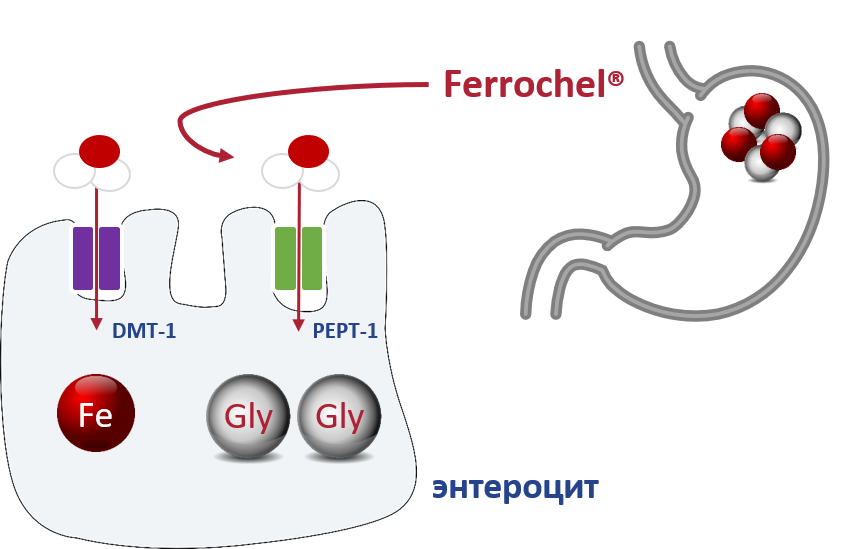
Соотношение железа к лиганду 1:2 нейтрализует валентность железа, что обеспечивает его стойкость к разным факторам, действующим в желудочно-кишечном тракте (рН, пища). Поэтому соединение хелата не поддается гидролизации в желудке, полностью абсорбируется в тонком кишечнике и в неизмененном виде попадает внутрь энтероцитов, где и происходит высвобождение молекулы железа. 8
Бисглицинат железа — это источник негемированного железа. После перорального применения соединение в неизмененном виде попадает в энтероциты, где гидролизируется на железо и глицин. Стабильность соединения бисглицината железа объясняется тем, что оно не гидролизируется при разных значениях рН, а низкая молекулярная масса (204 г/моль) способствует максимальному усвоению железа при пероральном приеме. 8
В составе Multizan ® Феррум бисглицинат железа представлен запатентованным комплексом Ferrochel ® компании Albion Minerals — мировым лидером и новатором в области минерального аминокислотного хелатного питания.
Уникальная гамма хелатных минералов Albion ® :
Даже с повышенной биодоступностью бисглицинат железа безопасен. Всасывание контролируется запасами железа в организме, при этом большие количества обычно усваиваются людьми с более низким статусом железа. Организм, страдающий железодефицитной анемией, может потреблять 90% железа, в то время как организм, не страдающий железодефицитной анемией, может потреблять всего 10%, или ровно столько, сколько необходимо организму для компенсации потерь в метаболизме. Было обнаружено, что бисглицинат железа Ferrochel ® в 2,6 раза безопаснее, чем сульфат железа, и безопаснее, чем обычное неорганическое железо, содержащееся в пищевых продуктах и пищевых добавках. 13
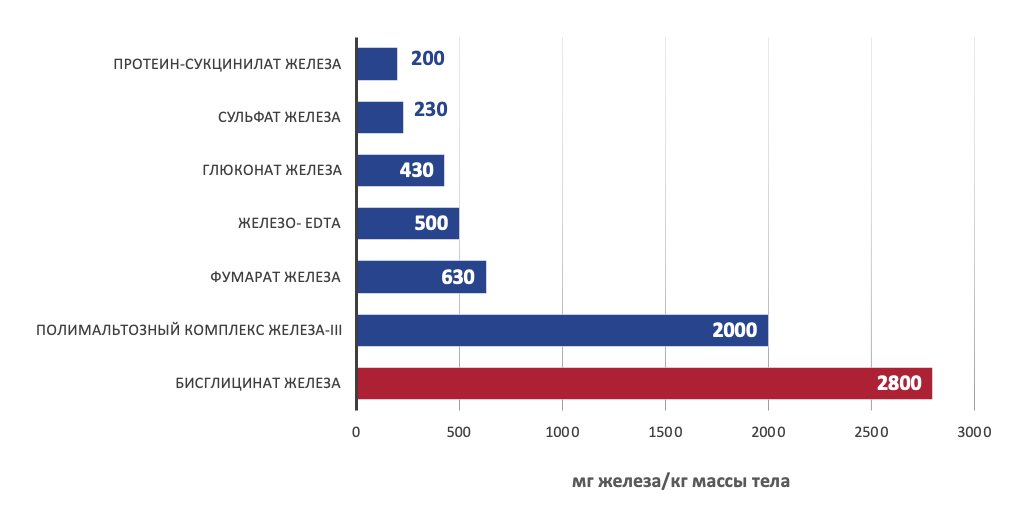
Сравнительная таблица доз LD50 (cредняя доза вещества, вызывающая гибель половины членов испытуемой группы) различных препаратов железа при пероральном введении белым мышам. 14, 15, 16