Утолщение стенок прямой кишки на кт что это может быть
МРТ прямой кишки что показывает
МРТ прямой кишки — это неиназивное, безопасное и бесконтактное исследование конечных отделов пищеварительного тракта. В отличие от других способов визуализации, вроде рентгенографии или компьютерной томографии, МРТ базируется на воздействии магнитного поля на ткани организма. Потому проводить исследование можно так часто, как того требует клиническая ситуация. Процедура может быть назначена пациентам любого возраста.
Делают ли МРТ прямой кишки?
МРТ прямой кишки проводят по показаниям. Методика позволяет оценить структуры, ткани конечного отдела пищеварительного тракта:
Методика подходит для визуализации мягких тканей, но не всегда дает однозначные результаты. Чтобы повысить информативность исследования, применяют модификации томографии: гидро-МРТ, МРТ с контрастным усилением.
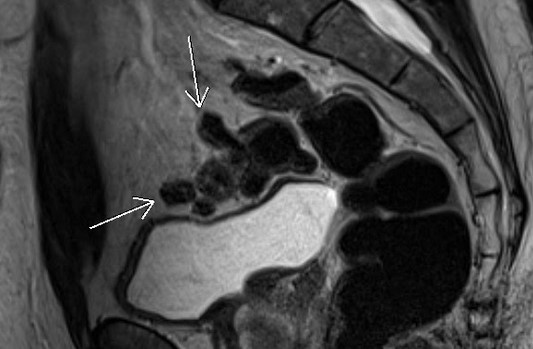
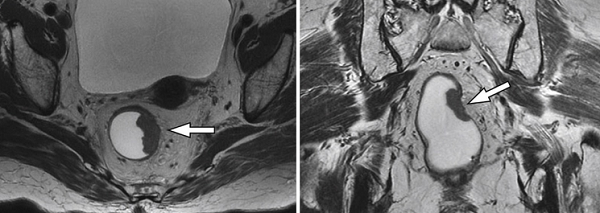
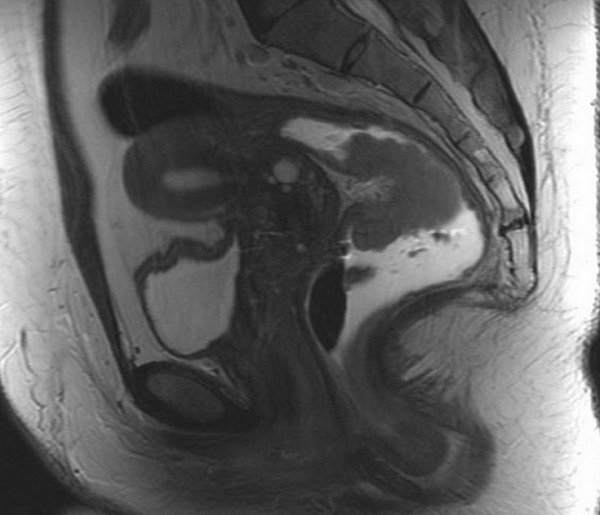
МРТ малого таза в сагиттальной плоскости. Отмечаются множественные дивертикулы сигмовидной кишки без признаков воспалительных изменений (стрелки).
Показания к МРТ прямой кишки
Показания к проведению МРТ кишечника — это воспалительные, дегенеративные, онкологические и другие заболевания конечного отдела пищеварительного тракта. Метод исследования применяется при подозрениях на патологический процесс или же в качестве способа верификации ранее установленного диагноза. Чтобы уточнить характер расстройства, окончательно развеять сомнения врача и назначить лечение.
Среди оснований для МРТ кишечника:
Среди показаний могут быть и отдельные жалобы, симптомы патологических процессов. Для чего делать томографию прямой кишки, и нужно ли это исследование — решает лечащий врач.
Какие заболевания покажет МРТ прямой кишки?
Томографический метод позволяет выявить заболевания воспалительного, дегенеративного, опухолевого характера. Среди возможных находок:
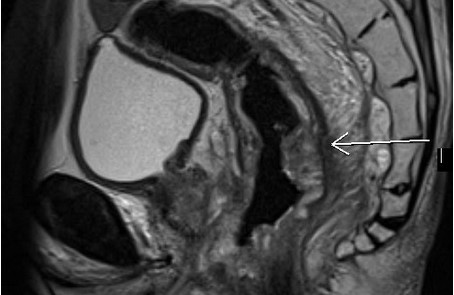
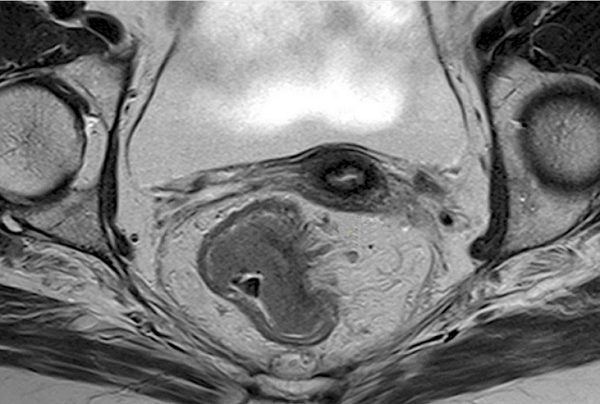
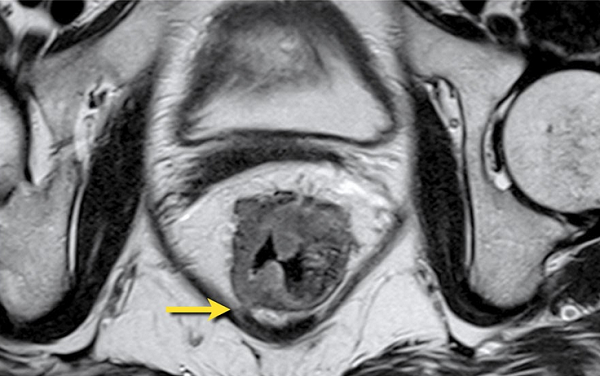
МРТ малого таза в сагиттальной плоскости. Отмечается циркулярное утолщение стенок прямой кишки за счет наличия объемного образования (стрелка), распространяющегося за пределы органа в параректальную клетчатку.
Процедура позволяет оценить структурные, анатомические особенности конечных отделов пищеварительного тракта. Но для постановки точного диагноза одной томографии достаточно не всегда. Проводится комплексная диагностика.
Подготовка к МРТ прямой кишки
Еще до того, как получено направление на томографию, пациент должен сообщить своему врачу о возможных противопоказаниях к исследованию. Среди них:
Существуют отдельные противопоказания к МРТ прямой кишки с контрастным усилением:
Большая часть противопоказаний — это относительные, временные проблемы. Как только они устранены, можно провести томографию.
Если противопоказаний нет, и врач направил на МРТ, можно приступать к подготовке. Она начинается за два дня до процедуры. Технология примерно такая же, как при подготовке к томографии органов малого таза:
В назначенный день нужно подъехать в клинику. Все запрещенные предметы оставляют в специально отведенном для этого месте. С собой нельзя брать телефон, электронику, украшения, металлические предметы, банковские карты, часы. Все то, что может среагировать на интенсивное магнитное поле.
Как делают МРТ прямой кишки?
Пациент проходит в кабинет, ложится на специальную кушетку аппарата. Ассистент врача инструктирует обследуемого. После — человека помещают в туннель томографа, начинается сканирование.
Время, которое требуется на обследование, зависит от того, что показывает МРТ прямой кишки. На все уходит до 30-40 минут. Исследования с контрастом занимают больше времени.
Контрастное вещество вводят после первичного обзорного сканирования.
Исследование с контрастом назначается при подозрениях на опухоли. Оно позволяет получить больше информации. Препарат проникает в измененные ткани, усиливает контрастность изображения. Врач получает возможность оценить точную локализацию, размеры неоплазии, ее форму, структуру, состояние окружающих тканей. Одного только МРТ органа недостаточно, чтобы выставить точный диагноз.
Нужна гистология опухоли. Его получают в ходе биопсии или операции. Затем фрагмент ткани отправляют в лабораторию для гистологической оценки. Такая процедура позволяет точно установить тип опухоли, степень ее злокачественности.
Если необходимо исследовать несколько сегментов кишечника, применяются, в том числе, и модификации стандартного метода томографии. Например, гидро-МРТ.
Через 15-20 минут после процедуры или в другой день (по договоренности), пациент получает результаты диагностики. В комплект документов входит протокол исследования, также заключение врача-рентгенолога, снимки в оцифрованном формате, на бумаге или на пленке. Зависит от конкретной клиники. Фото, результаты проведенной диагностики нужно показать своему лечащему врачу для постановки точного диагноза.
Расшифровка МРТ прямой кишки
Расшифровкой МРТ прямой кишки занимаются специалисты. Врач-рентгенолог предоставляет пациенту протокол диагностики, также собственное заключение. Но у него нет полного видения ситуации. Потому последнее слово остается за лечащим специалистом. Интерпретировать результаты нужно в системе с итогами прочих диагностических мероприятий.
Делать ли МРТ прямой кишки, зависит от особенностей конкретного клинического случая. Методика не имеет аналогов:
Дополнительные обследования назначает лечащий специалист, по показаниям.
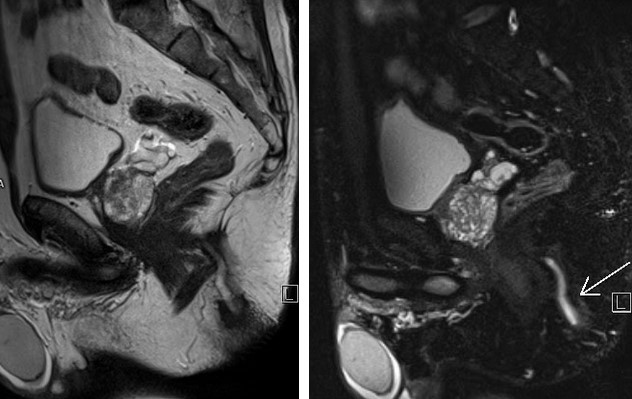
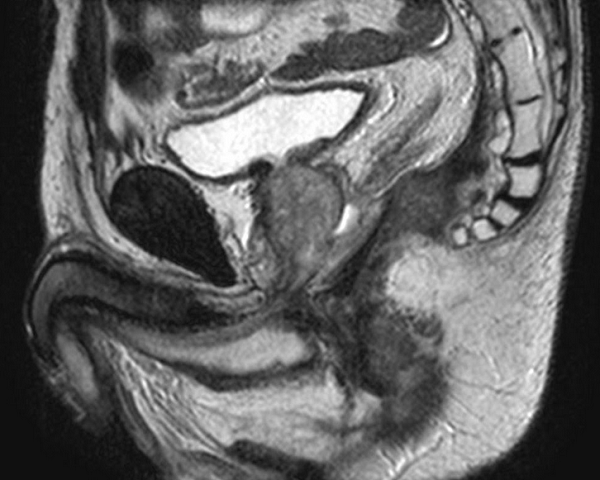
МРТ малого таза в сагиттальной плоскости. МР-признаки анального транссфинктерного свища (линейной формы, стрелка). Наружное отверстие расположено на коже перианальной области на расстоянии 32 мм от анодермальной линии.
МРТ прямой кишки что показывает
Все статьи написаны профессиональными врачами с большим опытом.
МРТ центр «МАГНИТ» не проводит «МРТ кишечника»
Магнитно-резонансная томография является высокоточным способом исследования внутренних органов и структур. Сканирование позволяет оценить состояние тонкого и толстого кишечника, не причиняя дискомфорта пациенту. Информативность томографии в некоторых случаях не уступает эндоскопическому исследованию и применяется как альтернативный метод инструментальной диагностики.
В результате МРТ прямой кишки врач получает послойные фото, визуализирующие строение рассматриваемого анатомического образования. Толщина сканируемого среза настраивается индивидуально и составляет от 1 мм.
Снимок МРТ прямой кишки
Метод основан на явлении магнитного резонанса, возникающего при воздействии индукционного поля на молекулы воды в клетках. Под влиянием направленного импульса атомы водорода совершают колебательные движения, которые считывает и преобразует в цифровую форму специальное устройство (приемник). Данные обрабатывают при помощи сложной компьютерной программы и транслируют на монитор в виде монохромных фотографий. Для повышения информативности МРТ в диагностике новообразований используют контрастное усиление.
Заболевания прямой кишки
Патологии ректального отдела на ранних этапах развития протекают бессимптомно или дают схожую клиническую картину. Дифференциальная диагностика заболеваний прямой кишки имеет большое значение для выбора эффективного метода лечения.
В медицине принято классифицировать патологические процессы в зависимости от этиологии и характера течения:
врожденные аномалии строения;
нарушение целостности слизистой оболочки;
Стенки прямой кишки состоят из мышечного слоя и слизистой оболочки, выстилающей внутреннюю поверхность. Эпителиальная ткань, в толще которой проходят кровеносные сосуды и нервы, формирует несколько поперечных и продольных складок. Мышечный слой участвует в образовании внутреннего и наружного сфинктеров.
Причинами заболеваний прямой кишки служат аутоиммунные, инфекционные, неопластические процессы, травмы, общие патологии и др.
Новообразование (указано стрелками) на Т2-взвешенном изображении МРТ
острая пульсирующая боль в области заднего прохода;
повышение температуры тела, общая слабость;
болезненные уплотнения вокруг анального отверстия;
В лечении проктитов используют противовоспалительные лекарственные препараты. Свищевой ход устраняют с помощью хирургического вмешательства.
В результате травматического повреждения слизистой оболочки прямой кишки возникают трещины или язвы анального канала. Характерным признаком служит боль во время дефекации и кал с примесью крови. В большинстве случаев повреждение слизистой наблюдают у пациентов, склонных к запорам.
Распространенной патологией кровеносных сосудов прямой кишки является геморрой. Для заболевания характерно образование венозных узлов в области анального канала. Причинами выпячивания сосудистой стенки служат:
длительное повышение внутрибрюшного давления;
врожденные патологии строения стенок сосудов;
застой крови в венах малого таза;
курение, алкоголизм и другие вредные привычки, негативно влияющие на тонус сосудов.
Геморроидальные узлы провоцируют кровотечения, боли в положении сидя и при опорожнении кишечника, возможно развитие парапроктита.
Рак прямой кишки (рецидив) на снимке МРТ
Полип анального канала – доброкачественная опухоль, на начальной стадии процесс протекает бессимптомно. При увеличении образования возникает боль при дефекации, появляются прожилки крови в каловых массах. В лечении используют хирургические методы.
Рак прямой кишки опасен отсутствием симптомов в период интрамурального роста (когда опухоль не выходит за пределы стенки ректального отдела). Развитие патологии сопровождается появлением стойкого болевого синдрома, запорами, кровотечениями, ухудшением общего состояния.
Магнитно-резонансная томография прямой кишки позволяет своевременно определить характер процесса. Ранняя диагностика положительно влияет на результативность лечения и повышает шансы пациента на выздоровление.
Делают ли МРТ прямой кишки?
Резонансная томография не является приоритетным видом изучения патологий любых органов, заполненных газом. Чаще врачи назначают КТ, но при наличии противопоказаний к использованию рентгена можно делать МРТ прямой кишки.
С помощью томографических изображений визуализируют состояние стенок дистального отдела толстого кишечника (слизистого и мышечного слоев), просвет, проходимость анального канала.
Дистальный отдел кишечника на томограммах
МРТ с усилением показывает более четкую картину расположения кровеносных сосудов. Злокачественные опухоли отличаются развитой капиллярной сетью с большим количеством анастомозов (соединений), поэтому медленнее накапливают контраст.
МРТ отличается высокой степенью визуализации тканей прямой кишки и окружающих структур. Метод позволяет оценить состояние брюшины, клетчатки, органов малого таза. По результатам МР-томографии врач делает выводы о степени поражения ректального отдела кишечника и распространении патологического процесса.
Подготовка к МРТ прямой кишки
Магнитно-резонансная томография брюшной полости и малого таза требует соблюдения специальной диеты в течение 2-3 дней до сканирования. Причиной служат особенности строения тонкого и толстого кишечника. При усиленной перистальтике и метеоризме на томограммах появляются дефекты, затрудняющие расшифровку фото.
МРТ прямой кишки необходимо делать после опорожнения дистального отдела, поэтому из рациона пациента следует исключить продукты, способствующие возникновению запора, диареи, повышению газообразования. В рамках подготовки к томографии нужно ограничить употребление алкоголя, курение.
Острая, жирная пища может спровоцировать раздражение слизистой оболочки и повлиять на результаты сканирования. Пациенту рекомендуют отварное постное мясо, каши на молоке низкой жирности, гарниры из тушеных овощей (за исключением капусты). Из напитков разрешается слабый чай, компоты, воду.
МРТ прямой кишки делают натощак, через 4-6 часов после приема пищи. При контрастном усилении следует перекусить за один час до процедуры, что позволит избежать возникновения тошноты и слабости после инъекции.
Пациент должен предупредить врача о наличии противопоказаний к магнитно-резонансной томографии. Перед сеансом нужно снять украшения, пирсинг, аксессуары из металла.
Рак прямой кишки с распространением процесса на мезоректальную клетчатку (указано стрелкой)
Кормящие женщины сцеживают молоко для малыша, так как после контрастной процедуры ребенка можно прикладывать к груди через 6-12 часов.
Показания и противопоказания к МРТ прямой кишки
Сканирование ректального отдела с помощью магнитного поля применяют в хирургии, онкологии, проктологии и др. МРТ назначают как самостоятельную диагностическую процедуру и в качестве дополнительного обследования при низкой информативности других методов.
Поводом для проведения томографии служат:
боли в области заднего прохода с иррадиацией в пояснично-крестцовую и копчиковую зоны;
частые позывы к опорожнению кишечника;
боли во время дефекации;
изменения стула (запор, диарея);
наличие патологических примесей в каловых массах;
ощущение инородного тела в заднем проходе;
МРТ прямой кишки показывает, что послужило причиной появления перечисленных симптомов, степень поражения стенок ректального отдела, состояние расположенных рядом анатомических структур. С помощью сканирования обнаруживают:
очаги воспаления слизистой оболочки кишечника;
доброкачественные образования (кисты, полипы и пр.);
дефекты слизистой оболочки;
инородные тела и конкременты.
Магнитно-резонансная томография показана перед хирургическим вмешательством. Послойные фото визуализируют точную локализацию и размеры патологического очага, позволяя оценить объем предстоящей операции. Повторные сканирования в период реабилитации делают с целью контроля процессов восстановления и своевременной диагностики осложнений.
При наличии опухоли метод используют для отслеживания роста и развития новообразования. В случае проведения лучевой и химиотерапии МРТ назначают для оценки эффективности лечения. Сканирование позволяет своевременно выявлять метастазы, диагностировать рецидив заболевания.
Первичная опухоль прямой кишки
Противопоказаниями к МРТ являются:
вживленные электромагнитные устройства медицинского назначения;
наличие в зоне сканирования металлических предметов;
грудные имплантаты (у женщин) с магнитными направляющими;
татуировки, выполненные металлсодержащими красками.
Ограничения к назначению МР-сканирования связаны с влиянием индукционного поля на некоторые вещества. Противопоказанием к контрастному усилению служат заболевания печени и почек в терминальной стадии. Выведение раствора гадолиния происходит естественным путем, с калом и мочой. Возрастает нагрузка на органы фильтрации, что приводит к декомпенсации имеющихся патологий.
Беременным женщинам нативную МРТ назначают не ранее второго триместра, контрастное усиление при обследовании будущих мам не используют.
МРТ прямой кишки, как делают?
Сканирование проводят с помощью томографа, состоящего из передвижного стола и широкого тоннеля. Аппарат генерирует постоянное магнитное поле определенной напряженности. От мощности устройства зависит качество послойных изображений.
Пациент ложится на стол томографа, тело и конечности фиксируют специальными валиками. На протяжении сеанса необходимо сохранять неподвижность, случайные перемещения приводят к появлению дефектов на снимках.
Для защиты от шума работающего аппарата используют наушники. Врач и рентген-лаборант во время процедуры располагаются за перегородкой, связь с обследуемым поддерживают через переговорное устройство.
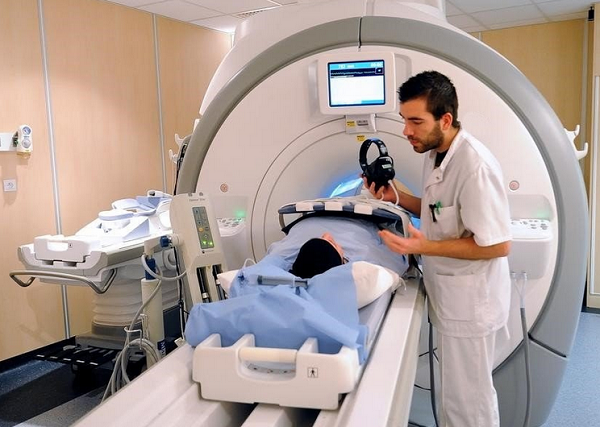
Процедура МРТ кишечника на аппарате закрытого типа
Стол с обследуемым задвигают в трубу томографа. Для лучшего результата в зоне интереса устанавливают градиентные катушки, индуцирующие переменное магнитное поле. Сканирование проводят в аксиальной, сагиттальной и фронтальной проекциях. С помощью компьютерной программы врач обрабатывает снимки и реконструирует 3D-модель изучаемого дистального отдела кишечника. Трехмерное изображение помогает визуализировать взаимное расположение анатомических структур и патологически измененного участка, для чего и назначают магнитно-резонансную томографию перед операцией на прямой кишке.
Для исследования анального канала чаще применяют нативную МРТ. В случае необходимости уточнить расположение опухоли, оценить состояние кровеносных сосудов используют контрастное усиление. С этой целью пациенту после серии нативных снимков делают внутривенную инъекцию раствора хелатов гадолиния. Манипуляцию проводят с помощью катетера и автоматического устройства (болюсное усиление).
Контраст заполняет сосудистое русло и межклеточное пространство в зоне интереса, после чего сканирование возобновляют.
По окончании процедуры больной получает результаты на руки. Врач объясняет пациенту содержание заключения, расшифровку фотографий.
КТ или МРТ прямой кишки?
Выбор метода обследования зависит от предполагаемого диагноза, состояния здоровья пациента, имеющихся противопоказаний и пр.
КТ отличается высокой информативностью при визуализации полых органов. Исследование занимает 5-15 минут, пациенту не нужно в течение продолжительного времени находиться в замкнутом пространстве, сохраняя неподвижное положение тела.
Недостатком компьютерной томографии является лучевая нагрузка на организм, получаемая во время сеанса. Процедуру не назначают беременным женщинам и людям, чье состояние здоровья не позволяет использовать рентген.
МРТ анального канала занимает 15-30 минут. При выборе правильного режима информативность метода достаточно высока и позволяет хорошо изучить состояние стенок кишечника и окружающих тканей.
Злокачественная опухоль на снимке МРТ
Магнитно-резонансная томография безопасна для здоровья пациента, не несет лучевой нагрузки и может проводиться неограниченное количество раз.
Решение о назначении КТ или МРТ прямой кишки принимает врач, учитывая клинические симптомы заболевания и особенности здоровья каждого пациента.
Утолщение стенок прямой кишки на кт что это может быть
Поражение терминального отдела подвздошной кишки при болезни Крона:
• Клинические признаки: диарея, боль в правом нижнем квадранте живота, повышение СОЭ; возможны железодефицитная анемия, стеаторея, дефицит витамина В12, синдром потери желчных кислот при желчной диарее.
• Возможные осложнения:
— Стеноз.
Образование свища: могут образовываться кишечно-кожные, кишечно-мочепузырные, кишечно-брыжеечные или кишечно-маточные свищи. Внимание: свищи также могут возникать при опухолях кишечника. Гипоэхогенные воспалительные изменения брыжейки. Образование абсцесса. Кишечная непроходимость.
• Ультразвуковые данные:
— Утолщение стенки терминального отдела подвздошной кишки более 4 мм. Увеличение содержания жидкости в просвете кишечника при утолщении стенки (жидкость скапливается в результате нарушения всасывания, в отличие от бактериального или вирусного энтерита, когда усиливается ее секреция).
— Ригидная петля кишечника при отсутствии или снижении перистальтики.
— Полипозно-измененная внутренняя стенка, имеющая вид «булыжной мостовой»
— Часто сопутствующий мезентерит.
— Признаки частичной кишечной непроходимости.
— Возможно присутствие свободной жидкости лимфаденопатия.
ЦДЭ: цветовые сигналы кровотока, указывающие на гиперперфузию воспалительного генеза.
Острый фебрильный энтерит (энтероколит):
• Клинические признаки: преимущественно поражается подвздошная кишка, однако возможно поражение тощей кишки. Острая боль в правом нижнем квадранте живота, напоминающая таковую при аппендиците.
• Патогенные микроорганизмы, вирусы (особенно ротавирусы), Yersinia, Campylobacter, стафилококки, сальмонеллы (инвазивные патогенные микробы, например, Shigella в ободочной кишке).
• Ультразвуковые критерии:
Утолщение стенки с чередованием гипоэхогенного, гиперэхогенного и гипоэхогенного слоев; часто имеется циркулярное поражение с вовлечением купола слепой кишки.
— Локальная болезненность кишечника при надавливании. Локальные скопления свободной жидкости.
Часто имеется увеличение брыжеечных лимфатических узлов («брыжеечный лимфаденит»). ЦДЭ: гиперваскуляризация воспалительного генеза.
Гематома тонкого кишечника: может развиваться на фоне применения антикоагулянтов или при коагулопатиях.
• Утолщение стенок кишечника.
• Выраженное гипоэхогенное утолщение стенки с сужением просвета (симптом «садового шланга»).
Закупорка брыжеечных сосудов:
• Гипоэхогенная неперистальтирующая петля тонкого кишечника различной длины (геморрагический некроз кишечника, суперинфекция).
• Утрата разделения стенки на слои.
• Признаки частичной или полной кишечной непроходимости.
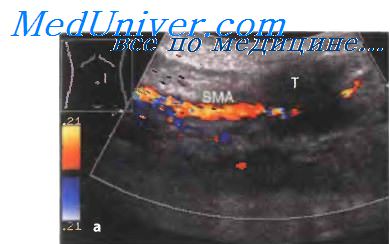
• Признаки стеноза или закупорки брыжеечных сосудов при допплеровском исследовании.
Амилоидоз: легкое утолщение длинного сегмента кишечной стенки (амилоидоз кишечника может также протекать без значительного утолщения стенки).
Ограниченное утолщение стенки кишки
Доброкачественные опухоли: например, аденома, лейомиома и нейрофиброма. Иногда, с учетом данных контрастной рентгенографии, возможна непосредственная визуализация опухоли при УЗИ.
• Полипозное утолщение стенки кишечника.
Злокачественные опухоли: примерами являются карцинома двенадцатиперстной кишки, карцинома тонкой кишки, карциноид, злокачественная лимфома, метастазы.
• Циркулярное утолщение стенки инфильтративного характера с симптомом «мишени» и клиническими проявлениями стеноза.
• Могут обнаруживаться метастазы.
Утолщение стенок прямой кишки на кт что это может быть
Как и многие другие опухоли, злокачественные новообразования колоректальной области подразделяются на эпителиальные, неэпителиальные (мезенхимальные и лимфомы), и вторичные образования согласно принципам классификации ВОЗ 2010 г. («Опухоли ободочной и прямой кишки», 2010). Из них, аденокарциномы, возникающие из клеток эпителия слизистой оболочки колоректальной области, составляют более 95% злокачественных опухолей ободочной кишки. Другие — редкие — типы опухолей включают в себя гастроинтестинальную стромальную опухоль (ГИСО), лимфому, нетипичную саркому и метастазы. Поскольку диагноз колоректального рака (КРР) основан на гистопатологической верификации путем колоноскопии, роль лучевых методов диагностики является вспомогательной и заключается в оценке преоперативных рисков, включая стадирование опухоли по TNM, определение поражения мезоректальной фасции с целью планирования лечения.
В некоторых случаях КРР приводит к существенным осложнениям, таким как обструкция, перфорация, ишемия, или инвагинация; в то же время эти проявления КРР могут быть идентифицированы с использованием соответствующих методов визуализации еще до колоноскопии (Kim et al.,2010а). В этой главе мы опишем стадирование опухоли по шкале TNM и оценку риска вне зависимости от стадии КРР. Будут также рассмотрены лучевые признаки других редких опухолей, таких как ГИСО, лимфома, и метастазов, которые могут быть применимы при определении характера КРР и в дифференциальной диагностике.
Во всем мире колоректальный рак (КРР) является третьей по частоте опухолью, обнаруживаемой и у мужчин, и у женщин. Факторами риска колоректального рака (КРР) являются возраст (старше 50 лет), принадлежность к мужскому полу, курение, злоупотребление алкоголем, особенности питания (употребление красного мяса, малого количества волокон и большого количества жира), ожирение, малоподвижный образ жизни, отягощенная наследственность, наличие полипов ободочной кишки, воспалительная болезнь кишечника, семейный аденоматозный полипоз (САП) и наследственный неполипозный колоректальный рак. Большинство случаев КРР являются спорадическими (80%), а остальные связаны с генными мутациями (20%) (Gollub et al., 2007). Патогенез КРР: в 70% случаев происходит развитие рака из аденомы, временной промежуток, необходимый для преобразования доброкачественной аденомы в злокачественную опухоль, равняется 7-10 годам; в остальных случаях рак возникает de novo (Полипы и рак ободочной кишки, 2008).
Гистопатологически колоректальные аденокарциномы подразделяются на опухоли высокой (10%), умеренной (70%) и низкой (20%) степени дифференцировки. Больше 50% случаев КРР приходится на сигмовидную и прямую кишку. Признаки и симптомы КРР могут варьировать, и включают в себя боль в животе, гематокезию, мелену, необъяснимую железодефицитную анемию, диарею, кишечную обструкцию, нарушение ритма дефекации. Тем не менее, не существует специфических симптомов рака толстой кишки на ранних стадиях. Десятки лет назад ирригоскопия с двойным контрастированием активно применялась в качестве важного метода диагностики. Однако в наши дни роль этого исследования крайне ограничена. На КТ и МРТ колоректальный рак часто проявляется асимметричным утолщением стенки короткого сегмента кишки с неправильной (либо не измененной) поверхностью. КРР на ранних стадиях может выглядеть как полиповидное или грибовидное образование без распространения за пределы кишки. На поздних стадиях КРР определяются мягкотканные «лучи», отходящие от стенки кишки и «пронизывающие» жировую клетчатку, окружающую ободочную или прямую кишку, где также могут быть обнаружены лимфатические узлы, расположенные вдоль сосудов.
В некоторых случаях дифференциальный диагноз между доброкачественными и злокачественными причинами утолщения стенки толстой кишки может быть затруднительным. Такие изменения, как асимметрия, отсутствие гаустр, нарушение «рисунка» слоев стенки и резкий переход между утолщенной и не измененной стенкой, свидетельствуют в пользу злокачественной опухоли.
а) Стадирование по шкале TNM. Рекомендации по стадированию колоректального рака (КРР) Американского объединенного комитета по раку (АОКР) (седьмая редакция) широко используются (табл. 19.1) при планировании терапии. Пациентам, страдающим раком ободочной кишки, обычно выполняется КТ органов брюшной полости и грудной клетки для определения стадии опухоли; в случаях рака прямой кишки также выполняется эндоректальная МРТ. Клинически, стратегия лечения при раке ободочной кишки редко меняется на основании определения Т или N стадии по результатам КТ, поскольку методом выбора в лечении по поводу множества типов рака ободочной кишки является колэктомия без неоадъювантной терапии. В то же время, методы лучевой диагностики больше подходят для определения отдаленных метастазов и инвазии в любой ближайший орган.
Однако при раке прямой кишки неоадъювантная терапия с последующей тотальной мезоректумэктомией (ТМЭ) является стандартом лечения для пациентов с ограниченно распространенной опухолью (Т3 или Т4, либо с наличием метастазов в регионарных лимфоузлах); таким образом, МРТ прямой кишки перед оперативным вмешательством выполняется с целью точного определения Т и N стадии и обнаружения поражения мезоректальной фасции.
б) Определение T стадии. Точное определение Т стадии требует правильной оценки глубины опухолевой инвазии. Общая точность определения стадии Т при использовании КТ составляет 41-82%, при использовании МРТ 71-91% («Полипы и рак ободочной кишки», 2008; Kim et al., 2010b).
1. Определение стадии Т1 и Т2. На стадии Т1 опухоль поражает слизистую оболочку и подслизистую основу, но не достигает мышечной пластинки (МП). На стадии Т2 происходит инвазия опухолью мышечной пластинки, но без распространения в жировую клетчатку за пределами ободочной кишки. Тем не менее, отличить стадию Т1 от Т2 достаточно сложно, даже при использовании МРТ. На КТ опухоль на стадии Т1 выглядят как выбухающее в просвет объемное образование без видимой деформации слоев стенки ободочной кишки (Dighe et al., 2008). Опухоль на стадии Т2 выбухает в просвет кишки, характеризуется асимметричным утолщением стенки, при этом окружающая жировая клетчатка остается светлой; не определяется признаков дезинтеграции мышечного слоя (Dighe et al., 2008). При использовании МРТ частичное сохранение высокой интенсивности сигнала от подслизистого слоя ниже опухоли, дающей средний по интенсивности сигнал на Т2 взвешенных томограммах, может стать признаком, полезным для дифференциальной диагностики между опухолями Т1 и Т2 (Costa-Silva и Brown, 2013). На практике, большинству пациентов, у которых обнаруживается рак прямой кишки на стадии Т1 и Т2, выполняется тотальная мезоректумэктомия, невзирая на то, какая именно стадия была установлена. Но, в то же время, встречаются случаи, когда требуется точно дифференцировать между собой стадии Т1 и Т2.
Например, когда хирург планирует ограниченную эксцизию чрезанальным доступом, при наличии высокого риска, связанного с резекцией, либо при тяжелом общем состоянии пациента может потребоваться точное определение Т стадии. К сожалению, точно отличить друг от друга стадии Т1 и Т2 невозможно при использовании КТ, и тяжело даже при МРТ; поэтому, когда точное определение Т стадии является критичным, рекомендуется эндоскопическая ультрасонография (ЭУС). При ЭУС можно определить, что нормальная стенка прямой кишки состоит из пяти чередующихся гипо- и гиперэхогенных концентрических слоев. Первый гиперэхогенный слой представляет собой поверхность слизистой оболочкой на границе с просветом. Второй гипоэхогенный слой соответствует мышечной пластинке слизистой оболочки, третий, гиперэхогенный, соответствует подслизистой оболочке. Четвертый и пятый гипо- и гиперэхогенный слои соответственно отражают мышечную оболочку и мезоректальный жир. Более тонкое разделение стенки прямой кишки при ЭУС помогает дифференцировать рак прямой кишки на ранних стадиях. Но, в то же время, недостатком ЭУС является тот момент, что этот метод является зависимым от врача, производящего исследование; требуется время, чтобы приобрести опыт в этой диагностической процедуре.
2. Определение стадии Т3 и Т4. Для опухолей, соответствующих стадии Т3, характерна инвазия в околоободочную (околопрямокишечную) жировую клетчатку. При использовании КТ и МРТ трудно отличить опухоль Т2 стадии с десмопластической реакцией от опухоли на ранней ТЗ стадии. В подавляющем большинстве случаев тонкие спикулы обусловлены десмопластической реакцией, в то время как при распространении опухоли за пределы кишки визуализируются толстые, узловидные тяжи; либо определяется выбухание контура с широким основанием (Nougaret et al., 2013). Опухоли на стадии Т4а прорастают в поверхность висцерального листка брюшины, по-разному покрывающего различные отделы ободочной и прямой кишки. Восходящая и нисходящая ободочная кишка покрыты висцеральной брюшиной только спереди и с латеральной стороны, в то время как поперечная ободочная и сигмовидная кишка покрыты брюшиной полностью. Верхняя часть прямой кишки покрыта висцеральной брюшиной спереди и с обеих боков, в средней части прямая кишка покрыта брюшиной спереди (Nougaret et al., 2013). Опухоли на стадии Т4а можно диагностировать на основании поражения брюшины, однако отличить опухоль на стадии Т3 от опухоли на стадии Т4а, полагаясь исключительно на данные лучевой диагностики, сложно. Положительным моментом является то, что рекомендуемое лечение на стадии Т3 и Т4а аналогично.
При раке ободочной кишки выполняются различные варианты колэктомии вне зависимости от того, отнесена ли опухоль к стадии Т3 или Т4а, при раке прямой кишки в обоих случаях требуется неоадъювантная химио- и лучевая терапия. Опухоли, достигшие стадии Т4b, прорастают в соседние органы; печень, смежные отделы кишечника, селезенку, поджелудочную железу, желудок, предстательную железу, семенные пузырьки, влагалище, матку или боковую стенку таза.
Определение T стадии рака прямой кишки с инвазией в анальные сфинктеры. Редко, при дистальной локализации рака прямой кишки могут поражаться анальные сфинктеры. В таких случаях инвазия опухоли во внутренний сфинктер означает стадию 1 или 2, распространение опухоли в область между сфинктерами — стадию 3, а прорастание в наружный сфинктер или окружающие органы — стадию 4 (Nougaret et al., 2013).
в) Определение N стадии. Стадия N означает метастазы в регионарных лимфатических узлах. Общая точность при идентификации метастазов в лимфоузлах с помощью КТ находится в диапазоне между 60 и 80%. Точность МРТ при определении стадии N в целом колеблется в широких пределах от 43 до 85% (Kim et al., 2010b).
Пути лимфогенного метастазирования. Метастазирование рака ободочной кишки в лимфоузлы происходит по путям лимфооттока вдоль регионарных сосудов, распределенных в брыжейке ободочной кишки. Изначально распространение рака ободочной кишки происходит главным образом в лимфоузлы, непосредственно прилежащие к ободочной кишке, находящиеся под брюшиной, вдоль стенки кишки. Затем лимфа оттекает в околоободчные лимфатические узлы, расположенные по ходу маргинальных сосудов; сосудов, обеспечивающих регионарный кровоток (например, подвздошно-ободочной или правой ободочной артерии); они образуют промежуточную группу лимфоузлов. В конечном счете лимфа попадает в главную группу лимфоузлов в месте отхождения верхней брыжеечной артерии (McDaniel et al., 1993). При раке прямой кишки отток лимфы из ее верхних отделов происходит в краниальную сторону вдоль верхней прямокишечной артерии и нижней брыжеечной артерии. Отток лимфы от нижней части прямой кишки может осуществляться двумя путями; в краниальном направлении через верхние прямокишечные лимфатические сосуды в нижние брыжеечные лимфоузлы, а также латерально через средние прямокишечные лимфатические сосуды во внутренние подвздошные лимфоузлы (Gowdra Halappa et al., 2012).
В некоторых случаях — при раке дистальных отделов прямой кишки вблизи анальных сфинктеров — возможно лимфогенное распространение в паховые лимфоузлы. Необходимо добавить, что в большинстве случаев вторичное поражение лимфатических узлов происходит на уровне опухоли либо выше. Нисходящее метастазирование (ниже уровня опухоли, каудально) встречается редко, за исключением случаев обструкции восходящих путей лимфооттока.
Характеристика лимфатических узлов и определение N стадии. В случаях наличия метастазов в 1-3 лимфатических узлах выставляется стадия N1, при вторичном поражении четырех и большего количества лимфоузлов — N2. Каждая из стадий в свою очередь предполагает разделение на подгруппы, например, N1a или N1b, в зависимости от количества лимфоузлов с метастатическим поражением. При раке прямой кишки в качестве регионарных лимфоузлов рассматриваются мезоректальные и внутренние подвздошные, даже если внутренние подвздошные лимфоузлы расположены вне области тотальной мезоректумэктомии. При наличии метастазов в других лимфоузлах, расположенных за пределами мезоректальной области, таких как наружные подвздошные, паховые, или лимфатические узлы в области общих подвздошных сосудов, подразумевается нерегионарная лимфаденопатия, и они расцениваются как отдаленные метастазы (М).
Стандартные критерии определения метастатического поражения лимфатических узлов посредством КТ четко не определены. Наиболее часто используемым признаком является размер лимфоузла. В случаях, когда лимфатический узел имеет размер больше 1 см в поперечнике, либо обнаруживается группа из трех и большего количества лимфоузлов, расположенных рядом, даже если размер любого из них меньше 1 см, предполагается их метастатическое поражение (Dighe et al., 2008). Но, в то же время, более чем в 50% случаев лимфатические узлы размером менее 5 мм оказывались вторично измененными, вследствие чего критерий размера нельзя считать достаточным сам по себе. При МРТ прямой кишки параметрами, позволяющими оценить лимфатические узлы на предмет метастатического поражения, являются характеристики краев, формы, внутренней однородности, а также размер (Kim et al., 2004). Критериями, позволяющими предположить метастатическое поражение лимфоузла, являются нечеткость или «лучистость» контура, внутренняя неоднородность интенсивности сигнала, а также округлая форма. Лимфоузлы правильной формы, с ровными краями и однородными сигнальными характеристиками расцениваются как доброкачественные. Размер лимфатического узла также является предиктивным критерием, который, тем не менее, однозначно не предполагает его метастатическое поражение (Beets-Tan et al., 2013).
г) Определение М стадии рака толстой кишки. Стадия М используется для оценки выраженности отдаленного метастазирования. КРР может метастазировать лимфогенным и гематогенным путями, путем диссеминации в полости брюшины; возможен также контактный путь метастазирования (непосредственная инвазия). Наличие отдаленных метастазов означает стадию М1, их отсутствие — МО. Стадия М1 в свою очередь подразделяется М1а и M1b. Стадия М1а означает, что метастазы имеются только в одном органе, в то время как M1b означает наличие метастазов в брюшине или вторичное поражение более чем одного органа. Органами, в которые чаще всего происходит отдаленное метастазирование, является печень, а затем легкие. Поскольку венозный отток от ободочной и прямой кишки осуществляется типично — через воротную вену, чаще всего гематогенные метастазы обнаруживаются в печени, затем следуют легкие, может также происходить метастатическое поражение головного мозга. Тем не менее, при раке дистальных отделов прямой кишки метастазы могут напрямую поражать легкие, минуя печень, поскольку средняя и нижняя прямокишечная вена впадают непосредственно в нижнюю полую вену (Gordon и Nivatvongs, 2007). В последнее время хирургическая резекция, если является возможной, становится методом выбора в лечении пациентов с метастазами КРР в печени.
Поэтому, в дополнение к точному обнаружению метастазов, рентгенологи должны учитывать возможность выполнения хирургического вмешательства, четко описывать локализацию, количество и размер вторичных очагов в печени при использовании методов диагностики, таких как МРТ с контрастным усилением печени препаратами гадоксетовой кислоты.
д) Циркулярный край резекции. Мезоректальная фасция, образованная висцеральным листком внутригазовой фасции, отражает уровень разреза при мезоректумэктомии, т. е. циркулярный край резекции (ЦКР). Эта фасция часто визуализируется на аксиальных и корональных Т2 взвешенных томограммах в виде тонкой пластинки с низкой интенсивностью сигнала. Поражение МРФ является независимым негативным прогностическим фактором. В некотором количестве исследований было показано, что инвазия МРФ тесно связана с рецидивом опухоли на ограниченном участке и низким уровнем выживаемости. Положительный ЦКР на МРТ прямой кишки означает, что наименьшее, измеренное по прямой расстояние между наиболее удаленным от центра краем зоны опухолевой инфильтрации и МРФ, составляет 1 мм и меньше. При использовании значения 1 мм в качестве оптимального порогового критерия оценки положительного ЦКР, специфичность МРТ в классификации ЦКР достигает 92%, а прогностическая ценность отрицательного результата 94% (Beets-Tan и Beets, 2011). Кроме того, потенциально угрожающий ЦКР определяется как расстояние 1-2 мм от края. Типы опухолевой инфильтрации, которые оцениваются при измерении ЦКР, включают в себя мезоректальное распространение опухоли, опухолевые депозиты, метастатическое поражение мезоректальных лимфоузлов, а также инвазию экстрамуральных сосудов (ИЭМС) (Nougaret et al., 2013). Мета-анализ применения МРТ для определения поражения ЦКР показал, что чувствительность метода колеблется в пределах 60-88%, а специфичность 73-100% (Gowdra Halappa et al., 2012).
е) Инвазия экстрамуральных сосудов. Прорастание опухоли в сосуды, располагающиеся вне стенки кишки, также является негативным прогностическим фактором, независимо от стадии TNM. ИЭМС определяется как состояние, при котором происходит инвазия опухоли в крупные сосуды, расположенные в мезоректальной области. Наличие ИЭМС связано с местным рецидивом, метастазированием, а также низким уровнем выживаемости. Такой тип инвазии может определяться на МР-томограммах прямой кишки наличием сигнала, имеющего интенсивность, характерную для опухоли, в сосуде; поражением сосудов и распространением опухоли через сосудистую стенку и вне ее с деформацией края сосуда (Nougaret et al., 2013). Прогностическая ценность положительного результата МРТ для ИЭМС подсчитана и характеризуется чувствительностью 62% и специфичностью 88% (Dewhurst и Mortele, 2013).
ж) Повторное стадирование после неоадъювантной химиолучевой терапии. Неоадъювантная ХЛТ с последующей тотальной ме-зоректумэктомией является стандартом лечения пациентов с местнораспространенным раком прямой кишки (ТЗ, Т4 или с метастазами в лимфоузлах). По результатам многих исследований использование неоадъювантной ХЛТ приводило к уменьшению частоты возникновения местного рецидива опухоли, а также к увеличению безрецидивной выживаемости и сохранению сфинктеров (Sauer et al., 2004). Приблизительно у 10-20% таких пациентов достигается полный ответ (CR) подтвержденный при гистопатологическом исследовании. Несмотря на то, что МРТ, выполняемая перед оперативным вмешательством без неоадъювантной ХЛТ, характеризуется относительно высокой точностью в определении Т стадии и оценке поражения циркулярного края резекции, точность при использовании методов визуализации при раке после лучевой терапии остается неудовлетворительной. Сообщается, что общая точность МРТ составляет приблизительно 50% при определении Т стадии рака после лучевой терапии, и около 66% при определении вовлечения ЦКР; снижение точности обусловлено сложностями дифференциальной диагностики лучевого фиброза и остаточной жизнеспособной опухоли (Kim et al., 2010b; Nougaret et al., 2013). Согласно отчету исследовательской группы MERCURY (The Magnetic Resonance Imaging in Rectal Cancer European Equivalence Study) для оценки степени опухолевой регрессии рака прямой кишки использовалась традиционная МРТ высокого разрешения (Costa-Silva и Brown, 2013; Patel et al., 2011).
Анализ осуществлялся на основании соизмерения пропорциональности сигнала различной интенсивности при использовании Т2 ВИ по сравнению с МРТ, выполненной до химиолучевой терапии. В итоге было сделано предположение, что области сигнала низкой интенсивности соответствуют зонам фиброза, в то время как области среднеинтенсивного и гиперинтенсивного сигнала отражают участки остаточной жизнеспособной опухоли. Между тем, классификация, приведенная Dworak et al., широко используется при гистопатологической оценке степени опухолевой регрессии при раке прямой кишки (Dworak et al., 1997). Гистопатологическая градация степени опухолевой регрессии осуществляется следующим образом: степень 0 (нет регрессии) означает отсутствие регрессии; степень 1 (минимальная регрессия) означает наличие доминирующего объемного образования с явным фиброзом и (или) васкулопатией; степень 2 (умеренная регрессия) означает преимущественные фиброзные изменения с малым количеством опухолевых клеток или групп клеток, которые легко обнаружить; степень 3 (практически полная регрессия) подразумевает крайне малое количество опухолевых клеток, которые с трудом обнаруживаются при микроскопии, в фиброзной ткани, с наличием слизистого компонента либо без такового; степень 4 (полная регрессия) означает отсутствие клеток опухоли, образование состоит только из фиброзной ткани.
Кроме того, во многих исследованиях были получены многообещающие результаты при использовании диффузионно-взвешенной томографии (DWI) после неоадъювантной ХЛТ для прогнозирования полного ответа (CR); другие исследования предполагают, что DWI может использоваться для прогнозирования поражения мезоректальной фасции или местного рецидива опухоли (Kim et al., 2009; Park et al., 2011; Lambregts et al., 2011). Дополнительно может использоваться качественный анализ с использованием DWI и количественная оценка измеряемых коэффициентов диффузии (ADC) (Kim et al., 2011). В основе этих исследований лежит представление, что остаточную ткань опухоли можно отличить от постлучевого фиброза при DWI с высоким значением b-фактора, поскольку резидуальная опухоль характеризуется относительно высокой целлюлярно-стью и меньшим интерстициальным пространством по сравнению с фиброзной тканью. Однако использование DWI в качестве рутинной последовательности остается спорным моментом и требует дальнейшего подтверждения. В рекомендациях, опубликованных после конференции европейского сообщества радиологов по вопросам лучевой диагностики органов желудочно-кишечного тракта и брюшной полости (European Society of Gastrointestinal and Abdominal Radiology (ESGAR) в 2012 г., однозначно говорится о трудности реальной дифференциальной диагностики полного ответа (CR) и резидуальной опухоли при использовании как Т2 ВИ, так и DWI (Curvo-Semedo et al., 2011). По результатам исследований сообщается, что уменьшение объема опухоли после неоадъювантной ХЛТ соотносится с уровнем ответа опухоли при гистопатологическом исследовании; имеются также предположения, что уменьшение объема опухоли на 70-75% и больше после неоадъювантной ХЛТ означает хороший или полный ответ (Nougaret et al., 2013).
Также, другие исследования показали, что волюметрический анализ на основании DWI после ХЛТ превосходит Т2 ВИ либо качественный или количественный анализ DWI при прогнозировании полного ответа (На et al., 2013).
После неоадъювантной ХЛТ вторично измененные лимфоузлы могут исчезнуть либо показать снижение стадии N. Повторное стадирование поражения лимфоузлов после лучевой терапии может быть сложным, поскольку охарактеризовать край, форму, внутреннюю неоднородность, а также размер более мелких лимфоузлов может быть невозможно; кроме того, затруднять повторное стадирование могут постлучевые изменения (van der Paardt et al., 2013). Тем не менее, интересно, что исследования показали большую точность при повторном стадировании поражения лимфоузлов после облучения по сравнению с МРТ до проведения ХЛТ. Эти результаты можно объяснить меньшей распространенностью и относительно большим размером лимфатических узлов, в которых не произошло уничтожения клеток опухоли после неоадъювантной ХЛТ. Точность и прогностическая ценность отрицательного результата при повторном определении стадии N, согласно докладам, составляет 67-90% и 83-94% соответственно (Beets-Tan, 2013).
з) Частые осложнения, обусловленные колоректальным раком. КРР может сопровождаться различными осложнениями, например, обструкцией, инвагинацией, ишемией, перфорацией, формированием фистулы, открывающейся в ближайшие органы; кроме того, осложнения могут маскировать первичную опухоль. Самым частым осложнением, связанным с раком ободочной кишки, является обструкция. Злокачественные опухоли ободочной кишки, расположенные слева, чаще приводят к обструкции просвета, чем при правосторонней локализации опухоли, поскольку диаметр ободочной кишки слева меньше (Kim et al., 2010а). Частота возникновения обструкции кишечника, связанной с раком ободочной кишки, составляет 8-29%. Перфорация может возникать в области первичной опухоли вследствие некроза или в проксимальной части опухоли из-за повышения давления в просвете. Сообщается, что частота возникновения перфорации и возникновения абсцесса, связанных с раком ободочной кишки, составляет 2,5-10% и 0,3-4% соответственно. (Kim et al., 2010а). Несмотря на то, что инвагинация очень редко возникает у взрослых пациентов, приблизительно в 65% случаев она связана с новообразованиями. На КТ признаком инвагинации является визуализация одной части кишки (либо кишки с брыжеечной жировой клетчаткой) внутри другой. Рак ободочной кишки, провоцирующий возникновение инвагинации, может быть обнаружен в конечных отделах дистального инвагината, и приблизительно в 30% случаев является неотличимым от отечной кишки.
е) Другие редкие типы колоректального рака (КРР). В соответствии с принципами классификации ВОЗ от 2010 г., выделяется несколько гистологических вариантов рака ободочной и прямой кишки. Из них муцинозная аденокарцинома и перстневидноклеточный рак ободочной и прямой кишки составляют 5-15% и 0,6% (соответственно) от всех вариантов первичного КРР. Диагноз муцинозной аденокарциномы при гистопатологическом исследовании устанавливается при наличии внеклеточно расположенного муцина, занимающего более чем 50% объема опухоли, в то время как перстневидноклеточный рак определяется, когда более 50% клеток опухоли являются перстневидноклеточныйыми («Опухоли ободочной и прямой кишки», 2010). Другие типы КРР, такие как мелкоклеточный, плоскоклеточный, железисто-плоскоклеточный, медуллярный, недифференцированный рак, крайне редки. При КТ важными признаками, позволяющими установить гистологический тип опухоли, особенно, муцинозной аденокарциномы, являются мелкие внутриопухолевые обызвествления и включения муцина низкой плотности («Полипы и рак ободочной кишки», 2008). Примечательно, что на Т2 взвешенных и диффузионно взвешенных томограммах муцинозная аденокарцинома характеризуется большей интенсивностью сигнала, чем типичная колоректальная аденокарцинома, дающая средний по интенсивности сигнал (Kim et al., 2010b). В дополнение, метастазы муцинозной аденокарциномы колоректальной области в печени могут визуализироваться в виде объемных образований с высокой интенсивностью сигнала на Т2 взвешенных томограммах, вследствие чего ошибочно принимаются за кисты.
1. Поскольку диагноз КРР основан на гистопатологическом подтверждении посредством колоноскопии, роль методов лучевой диагностики является вспомогательной и состоит в оценке риска перед оперативным вмешательством, в т.ч. в определении стадии TNM и оценке поражения мезоректальной фасции с целью определения плана лечения.
2. При раке прямой кишки неоадъювантная ХЛТ с последующей тотальной мезоректумэктомией является стандартом лечения пациентов с местнораспространенными опухолями (Т3, Т4 или с наличием метастазов в регионарных лимфоузлах); МРТ прямой кишки перед оперативным вмешательством рекомендуется с целью точного определения стадии (местного распространения) и обнаружения поражения МРФ.
3. Поскольку точно дифференцировать опухоль на стадии Т1 и Т2 при использовании КТ невозможно, и затруднительно даже при применении МРТ, в случаях, когда это является критичным при планировании лечения, рекомендуется ЭУС.
4. На КТ и МРТ сложно отличить друг друга опухоли на стадии Т2 с наличием десмопластической реакции и рак на ранней Т3 стадии. В большинстве случаев наличие тонких спикул обусловлено десмопластической реакцией, в то время как толстые, узловидные тяжи или выбухание контура на широком основании являются основанием для предположения распространения опухоли за пределы стенки.
5. Предиктивные критерии для определения метастазов в лимфатических узлах включают в себя размытые или лучистые края, неоднородность интенсивности сигнала от внутренней части узла, а также округлую форму. Лимфоузлы, не отличающиеся друг от друга, с ровными краями, с однородной интенсивностью сигнала рассматриваются как доброкачественные. И, хотя размер лимфоузла также является прогностическим критерием, он не является признаком, однозначно свидетельствующим о его метастатическом поражении.
6. В случаях, когда наименьшее измеренное по прямой расстояние между самым наружным краем опухолевой инфильтрации и МРФ составляет 1 мм и меньше, предполагается позитивный ЦКР. Если это расстояние составляет 1-2 мм, ЦКР считается угрожающим.
7. Колоректальный рак (КРР) может сопровождаться различными осложнениями, например, обструкцией, инвагинацией, ишемией, перфорацией и формированием фистулы с прилежащими органами; осложнения могут маскировать первичную опухоль.
8. По мере увеличения размеров ГИСО чаще наблюдается тенденция к сохранению ровных краев и отодвиганию расположенных поблизости петель кишки или сосудов, чем инвазия и десмопластическая реакция, и эти изменения могут быть полезны в дифференциальной диагностике ГИСО и аденокарцином.
9. Лучевые признаки лимфомы ободочной и прямой кишки могут сочетаться с признаками других заболеваний колоректальной области. Тем не менее, специфические лучевые признаки, такие как однородное контрастное усиление, аневризматическая дилятация, не сопровождающаяся обструкцией, распространенная лимфаденопатия, а также относительно четкая демаркация очага поражения с сохранением жировой клетчатки могут быть полезны в диагностике местно ограниченных форм лимфомы ободочной и прямой кишки, особенно диффузной В-крупноклеточной лимфомы.
з) Список использованной литературы:
Редактор: Искандер Милевски. Дата публикации: 26.5.2019