Ттг гормон что это такое у детей
Информация в статье является справочной и не может использоваться для самодиагностики и самолечения. Для расшифровки результатов анализов обратитесь к специалисту.
Анализ на ТТГ (тиреотропный гормон, тиротропин) – это лабораторное исследование, которое позволяет измерить уровень данного гормона в крови. Его результат дает возможность оценивать качество работы щитовидной железы. Чаще всего врачи проводят диагностику для выявления гипотиреоза и тиреотоксикоза. ТТГ вырабатывается гипофизом.
Тиреотропин — это
Тиреотропин — это вещество, вырабатывающееся клетками в передней доле гипофиза. Он активирует выработку и выделение в кровь этих гормонов, вырабатывающихся щитовидной железой. Гормон запускает рост клеток щитовидной железы и ускоряет их деление. Образование ТТГ запускает тиротропин-рилизинг-фактор гипоталамуса.
Этот процесс происходит, когда снижается уровень циркулирующих в крови гормонов. ТТГ имеет обратную логарифмическую зависимость от содержания Т4 в крови. Когда возрастает уровень Т4 производство, ТТГ снижается. А если снижается концентрация Т4, производство ТТГ растет.
Такой механизм поддерживает постоянство содержания гормонов на необходимом уровне. Секреция ТТГ регулируется нейрональными механизмами. Ее скорость изменяется сна, при снижении температуры, неспецифическом стрессе.
Для ТТГ типичны суточные изменения концентрации. Высшие величины ТТГ крови достигаются в промежутке с 2 до 4 часов ночи. Этот уровень остается на этих значениях с 6 до 8 часов утра. Минимальное содержание ТТГ регистрируется в 17-18 часов.
Нормальный ритм выработки и выделения ТТГ при бодрствовании в ночное время нарушается. Патологии щитовидной железы приводят к снижению уровня тиреоидных гормонов при гипотиреозе или либо к избыточному их содержанию в крови при гипертиреозе.
Гормон стимулирует работу клеток щитовидной железы. Этот орган расположен на передней части шеи и имеет вид бабочки. Железистая ткань продуцирует гормоны, регулирующие большинство функций организма. Самые важные среди них – это обмен веществ, температура тела, частота сердечных сокращений.
Гормон ТТГ регулирует производство клетками гормонов щитовидной железы по механизму обратной связи. При понижении уровня Т4 и Т3 гипофиз производит больше гормона. Так он стимулирует клетки щитовидной железы. При высоком содержании этих веществ гипофиз снижает интенсивность синтеза ТТГ.
Этот механизм поддерживает постоянный уровень тиреоидных гормонов, а также стабильность обмена веществ. При нарушении связей между щитовидной железой, гипоталамусом и гипофизом нарушается работа эндокринных желез. Возникают ситуации, когда при высоком уровне Т3 и Т4 тиреотропный гормон продолжает увеличиваться.
Тиреотропный гормон активизирует кровоснабжение тканей щитовидки. Йод, необходимый ее клеткам для работы, активнее усваивается. Этот элемент повышает выработку тиреоглобулина, трийодтиронина, тироксина.
Они ответственны за метаболизм питательных веществ (белков, жиров, углеводов) в организме. Еще гормоны определяют работу пищеварительной, а также репродуктивной системы. От них зависит функционирование системы кровообращения и высшая нервная деятельность. Как недостаток, так и избыток ТТГ, а также уровень тиреоидных гормонов влияют на состояние организма человека.
Показания к сдаче анализа на ТТГ
Исследование на ТТГ считают одним из самых важных в программе диагностики на гормоны. Часто анализ назначают одновременно с гормонами Т3 и Т4. Показания назначению исследования следующие:
Исследование производят для контроля над терапией бесплодия и патологий щитовидной железы.
Подготовка к процедуре
Накануне анализа на гормон ТТГ в крови пациенту рекомендуют с осторожностью относиться к приему медикаментозных препаратов и витаминных комплексов с содержанием йода. Он искажает результаты анализа. Врачи рекомендуют отказ от приема лекарств, угнетающих образование гормонов, за две недели до момента тестирования на гормоны.
Если по каким-либо причинам это сделать невозможно, предупредите врача лаборанта о применяемых препаратах. Чтобы результат анализа был достоверен, готовиться к нему начинают за трое суток. Для получения корректных данных тестирования рекомендуют сделать следующее:
Сдают анализ крови на ТТГ на голодный желудок. Разрешают выпить стакан воды без газа.
Что может повлиять на результаты
Перед проведением анализа на ТТГ пациенту рекомендуют исключить воздействие факторов, способных повлиять на результат анализа или серьезно затруднить его интерпретацию. К ним относят следующее:
Когда целью проведения анализа является контроль проводимой терапии заболеваний щитовидной железы, за день перед проведением диагностических процедур приостанавливают прием препаратов.
Норма ТТГ
Нормальные показатели уровня ТТГ изменяются с возрастом. Его значения могут варьировать у женщин в состоянии беременности.
Гипотиреоз у детей
Гипотиреоз — это клинический синдром, обусловленный дефицитом гормонов щитовидной железы или нарушением их эффекта на клеточном уровне. Функционировать железа начинает к 10–12 нед беременности: до этого периода развитие плода осуществляется матерински
Гипотиреоз — это клинический синдром, обусловленный дефицитом гормонов щитовидной железы или нарушением их эффекта на клеточном уровне.
Функционировать железа начинает к 10–12 нед беременности: до этого периода развитие плода осуществляется материнскими тиреоидными гормонами. Гипоталамо-гипофизарный контроль над щитовидной железой формируется вскоре после рождения ребенка. Синтез тиреоидных гормонов происходит в тироцитах, являющихся структурной единицей щитовидной железы, образующих фолликулы, заполненные коллоидом, основным компонентом которого является йод-тиреоглобулин.
Тиреоцит активно захватывает йод из крови, затем он окисляется, органифицируется и под действием пероксидазы тиреоцитов присоединяется к тирозину в составе тиреоглобулина. В результате образуются активный гормон тироксин (Т4), в меньшем количестве — трийодтиронин (Т3), которые депонируются в составе тиреоглобулина в полости фолликула щитовидной железы. Запасов тиреоидных гормонов, находящихся в ней, хватило бы на 2 мес.
На уровне клетки биологический эффект опосредуется главным образом Т3, который интенсивно образуется в почках, печени и других тканях из Т4 под действием дийодиназ путем отщепления одного атома йода. Часть свободного йода вновь улавливается щитовидной железой и включается в синтез гормонов. Лишь небольшая часть йода выводится с мочой. Низкие показатели йода в моче означают недостаточное поступление его в организм.
Процесс секреции тиреоидных гормонов начинается с захвата тиреоцитами коллоида фолликулов. После отсоединения тиреоглобулина Т4 и Т3 поступают в кровь, где связываются на 99% с белком. В свободной форме Т3 крови в 10 раз больше, чем Т4.
Регуляция синтеза и секреции тиреоидных гормонов осуществляется в рамках гипоталамо-гипофизарно-тиреоидной системы по принципу обратной связи. Тиреолиберин гипоталамуса стимулирует выработку тиреотропного гормона гипофиза (ТТГ): последний необходим для синтеза тиреоидных гормонов в щитовидной железе. Итак, высокие концентрации Т3 и Т4 подавляют продукцию ТТГ, а низкие — стимулируют.
В кровоток щитовидная железа секретирует в 20 раз больше Т4, чем Т3.
40% тироксина метаболизируется в активный Т3, другая часть в пропорциональных количествах превращается в неактивный (реверсивный) Т3. Период полужизни Т4 составляет 6–7 дней, а Т3 всего 1–2 дня. Свободный Т4 более адекватно характеризует функцию щитовидной железы, так как он образуется только в тиреоцитах, а свободный Т3 — лишь на 20% в них.
Тиреоидные гормоны необходимы для нормального развития организма в антенатальном и постнатальном периодах. Они влияют на все виды обмена веществ. Тиреоидные гормоны стимулируют кишечную резорбцию углеводов, способствуют глюконеогенезу, регулируют синтез гликогена и гликогенолиз.
Гормоны щитовидной железы способствуют распаду жиров, оказывают анаболическое действие на белковый обмен.
Крайне необходимы тиреоидные гормоны для нормального развития головного мозга — особенно во внутриутробном периоде и в первые годы жизни, когда происходит формирование мозговых структур, отвечающих за интеллект человека.
Содержание тиреоидных гормонов у плода прогрессивно нарастает начиная с 5 мес беременности, достигая максимума к моменту родов.
Значительные изменения претерпевает уровень ТТГ у новорожденного. Если у плода к моменту рождения концентрация ТТГ составляет около 10 мк Ед/мл, то через 30 мин после рождения резко повышается, в течение 2–3 дней постепенно снижаясь до исходных значений. Нарастание концентрации ТТГ вызывает в первые часы жизни ребенка повышенный выброс Т4 и Т3.
Врожденный гипотиреоз — это гетерогенная группа заболеваний, которые вызваны либо сниженной продукцией тиреоидных гормонов, либо нарушением их действия на уровне клетки.
В зависимости от уровня поражения гипоталамо-гипофизарно-тиреоидной оси различают первичный (тиреогенный), вторичный (гипофизарный) и третичный (гипоталамический) гипотиреоз.
По тяжести заболевания: транзиторный, субклинический, манифестный.
Гипотиреоз в подавляющем числе случаев — это заболевание, связанное с нарушением функции самой щитовидной железы.
Частота первичного врожденного гипотиреоза составляет от 1:1700 до 1:5000 новорожденных. Девочки болеют в 2 раза чаще, чем мальчики. У 75–85% больных врожденный гипотиреоз возникает в результате поражения зачатка щитовидной железы на 4–9 нед беременности. При сканировании у трети пациентов имеется аплазия щитовидной железы, у остальных — гипоплазия, дистопия (в корень языка, трахею, на переднюю поверхность шеи). Порок щитовидной железы может возникнуть под влиянием тиреотоксических препаратов (Мерказолил, большие дозы йода, бромиды, соли лития, транквилизаторы), которые принимают женщины во время беременности, антитиреоидных антител при аутоиммунном тиреоидите у беременных, токсических и химических веществ. Не исключается роль внутриутробных инфекций. В 15% случаев причиной врожденного гипотиреоза является дефект синтеза тиреоидных гормонов или тканевых рецепторов к ним. При ферментативном дефекте щитовидная железа значительно увеличена.
Вторичный и третичный врожденный гипотиреоз встречается либо вследствие внутриутробной аномалии гипоталамо-гипофизарной системы, либо генетических дефектов, обусловливающих выработку аномального тиреолибирина и ТТГ.
До внедрения скрининга на врожденный гипотиреоз нередко диагноз этого заболевания устанавливался поздно, что приводило к пожизненной инвалидизации больного.
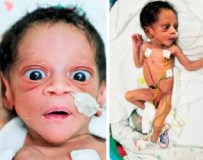
В неонатальном периоде следует обращать внимание на такие признаки, как переношенная беременность, незрелость, большая масса при рождении, низкий, грубый голос при крике, плохое отхождение мекония, затрудненное дыхание через нос, приоткрытый рот, а также увеличенный в размерах, отечный язык. Отеки могут быть локальными на любой части тела, часто бывает пупочная грыжа.
На первом месяце жизни к вышеперечисленным симптомам можно отнести позднее отпадание пупочного остатка, медленное заживление пупочной ранки, затянувшуюся желтуху и упорные запоры. В последующие месяцы появляются признаки отставания психомоторного развития. Ребенок вялый, сонливый, пассивный, быстро утомляется при кормлении. Реакция на окружающую действительность отсутствует. Лицо амимично, малыш не интересуется игрушками, часами сохраняет неподвижное положение. Нарастает отставание в двигательной сфере: больной не держит голову, не переворачивается со спины на бок, не сидит, не стоит, часами сохраняет неподвижность при голодании и наличии мокрой пеленки.
Ребенок недостаточно прибавляет в весе, кожа бледная, с ксантохромным оттенком, сухая, волосы тусклые, выпадают, живот вздут, брюшная стенка гипотонична.
К 3–4 мес развивается анемия в связи с дефицитом железа, витаминов, микроэлементов.
Многие из перечисленных выше симптомов неярко выражены у больных с гипотиреозом, которые находятся на грудном вскармливании, так как с материнским молоком ребенок получает тиреоидные гормоны. Перевод таких детей на искусственное вскармливание ускоряет появление типичных симптомов гипотиреоза.
К 6 мес характерным симптомом врожденного гипотиреоза является задержка роста за счет отставания роста трубчатых костей в длину. Развиваются хондродистрофические пропорции тела. Задерживается прорезывание зубов и закрытие родничков. Лицо одутловатое, глазные щели широко расставлены, переносица широкая, плоская, губы толстые, язык увеличен в объеме за счет отека, может не умещаться во рту. Дыхание у некоторых больных стридорозное.
Костный возраст отстает от паспортного, нарушается последовательность появления ядер окостенения.
Сердце увеличено в размере, нередко выслушивается систолический шум, который требует дифференциальной диагностики с выраженным пороком сердца. Тоны сердца приглушенные, наблюдается тенденция к брадикардии после 3 мес жизни. На ЭКГ вольтаж зубцов снижен, замедляется проводимость в желудочках.
Быстро формируется брадипсихия, которая проявляется безразличием к музыкальным звукам, а также цветам. Отсутствуют эмоциональные мимические и голосовые реакции. Ребенок не «гулит», не произносит отдельные слоги, не интересуется окружающим миром, не играет самостоятельно. Нарастание этих нарушений зависит от глубины снижения функции щитовидной железы. Данные электроэнцефалографии свидетельствуют о грубой незрелости мозговых структур. Лечение тиреоидными гормонами, начатое на первом месяце жизни, значительно компенсирует изменения со стороны центральной нервной системы (ЦНС) — дети в большинстве случаев развиваются психически удовлетворительно. Однако специальные исследования на когнитивную функцию свидетельствуют об отставании в развитии от здоровых детей.
Если заместительная терапия начата после года, то грубые изменения со стороны ЦНС остаются на всю жизнь.
В связи с трудностями клинической диагностики врожденного гипотиреоза в неонатальном периоде, с 1994 г. в нашей стране проводятся массовые обследования новорожденных на предмет данного заболевания. Скрининг позволяет выявить врожденный гипотиреоз на первом месяце жизни и начать своевременно заместительную терапию. Наибольшей информативностью для постановки первичного врожденного гипотиреоза, который встречается в 85–90% случаев, обладает исследование ТТГ.
Учитывая динамику изменения этого показателя в первые дни жизни, рекомендуется проводить забор крови из пятки на 4–5-й день у доношенных детей и на 2-й нед жизни у недоношенных. Кровь исследуется в специализированной лаборатории неонатального скрининга. Допустимый высший предел нормальных значений составляет 20 мк/Ед мл. Если этот показатель превышен, то из того же самого образца крови исследуют уже 2 параметра: ТТГ и тироксин. Когда ТТГ превышает 20 мк/Ед мл, а общий тироксин ниже 120 нмоль/л, назначают тиреоидные гормоны.
В тех случаях, когда уровень ТТГ, взятого в роддоме, превышает 50 мк/Ед мл, требуется повторное исследование ТТГ и тироксина в крови в этом образце, но параллельно в поликлинике следует взять кровь из вены для определения тех же самых гормонов. Тиреоидные препараты таким детям назначаются до получения повторных результатов.
Аналогичная тактика повторных исследований ТТГ и тироксина, а также назначения тиреоидных препаратов, применяется при обнаружении уровня ТТГ выше 100 мк/Ед мл, который типичен для врожденного гипотиреоза.
В практике врача чаще встречается умеренное повышение ТТГ у новорожденных, которое исчезает через несколько недель. Это состояние тиреоидного статуса обозначают как транзиторный гипотиреоз. Причиной временного повышения ТТГ является незрелость гипоталамо-гипофизарно-тиреоидной оси, связанная с неблагоприятным течением беременности и родов. Это внутриутробная инфекция, гипотрофия, недоношенность, дефицит йода у матери и т. д. В ответ на низкие показатели тироксина повышается уровень ТТГ, обычно не превышающий 50 мк/Ед мл. В большинстве случаев эти дети в лечении не нуждаются, т. к. через 2–3 нед показатели ТТГ нормализуются.
Итак, определение уровня ТТГ дает объективную информацию о гормонопродуцирующей функции щитовидной железы. При гипотиреозе уровень ТТГ повышается, а концентрация Т4 и Т3 снижается.
Низкий уровень ТТГ при гипотиреозе свидетельствует о нарушении в гипофизе или гипоталамусе и исключает нарушение функции щитовидной железы.
У некоторых больных с вторичным гипотиреозом уровень ТТГ в крови находится в пределах нормы либо парадоксально повышен, что связывают с секрецией иммунореактивного, но биологически неактивного ТТГ.
Лечение врожденного гипотиреоза начинают сразу после постановки диагноза. Заместительную терапию проводят тиреоидными препаратами. Из них чаще применяют L-тироксин: детям первых 3 мес жизни — 8–15 мкг на кг массы тела, до 6 мес — 8–10 мкг на кг массы тела. Лечение следует начинать с минимальных доз. Препарат назначают в утренние часы за 30 мин до еды. Увеличивать дозу следует каждые 7–10 дней, ориентируясь на стул, пульс, вес, состояние нервной системы, а также на показатели уровня Т4 и ТТГ в крови. При появлении первых симптомов передозировки (учащение пульса, беспокойство, потливость, учащенный стул) дозу препарата снижают наполовину.
Одновременно с заместительной терапией назначают витамины, глутаминовую кислоту, Церебролизин и другие препараты, улучшающие метаболизм в нервной клетке (Энцефабол, Ноотропил, Пантогам и др.), массаж, гимнастику.
Дети с врожденным гипотиреозом должны постоянно находиться под наблюдением эндокринолога. Помимо клинической оценки адекватности терапии, у больных контролируют показатели ТТГ, Т4 и Т3. После начала лечения забор крови на тиреоидный статус проводят через 2–3 нед и 1,5–2 мес. В дальнейшем до 1 года контроль ТТГ и Т4 проводят каждые 3 мес.
В последние годы в комплексное обследование больных с гипотиреозом включают ультразвуковое исследование щитовидной железы, а также определение тиреоглобулина, который является показателем наличия ткани щитовидной железы.
Прогноз психомоторного развития детей с врожденным гипотиреозом во многом зависит от возраста, начала лечения и адекватности подобранной дозы тиреоидных препаратов. Если терапия проводится с первых месяцев жизни, дети в основном развиваются нормально. Лечение гормонами щитовидной железы проводится пожизненно.
В. В. Смирнов, доктор медицинских наук, профессор
РГМУ, Москва
Гипертиреоз у детей
Гипертиреоз у детей — это клинический синдром, который характеризуется повышенной выработкой тиреоидных гормонов. Возникает при диффузном токсическом зобе, аденоме гипофиза, на начальных стадиях тиреоидитов. Основные симптомы: ускорение обмена веществ, психоэмоциональные нарушения, дисфункция пищеварительной и сердечно-сосудистой системы. Диагностика синдрома предполагает УЗИ и сцинтиграфию щитовидной железы, развернутый анализ тиреоидного гормонального профиля и специфических антител. Лечение состоит из тиреостатической терапии, препаратов радиоактивного йода и бета-адреноблокаторов.
МКБ-10
Общие сведения
Гипертиреоз встречается с частотой до 20-25 больных на 100 тыс. детского населения. В основном болеют дети предпубертатного и пубертатного возраста, причем девочки в 6-8 раз чаще мальчиков. У младенцев и детей раннего возраста симптомы гипертиреоза определяются не чаще 8 случаев на 1 млн населения. Термины гипертиреоз и тиреотоксикоз обычно используются как синонимы, хотя первый обозначает гиперфункцию щитовидной железы (ЩЖ), а второй — токсические эффекты тиреоидных гормонов на ткани. Зачастую у ребенка развиваются оба состояния, но иногда гипертиреоз может быть изолированным.
Причины
У новорожденных гиперфункция ЩЖ зачастую связана с наличием токсического зоба у матери. При этом в организме беременной вырабатываются специфические антитела, которые проникают через плаценту к плоду, присоединяются к рецепторам тироцитов и усиливают синтез гормонов. У старших детей гипертиреоз провоцируется следующими причинами:
Патогенез
Усиление выработки тиреоидных гормонов в щитовидной железе вызвано либо тиреостимулирующими антителами, либо повышением концентрации гормональных регуляторов (ТТГ и тиролиберинов) в крови. В результате этих механизмов в системный кровоток поступает неадекватное количество Т3 и Т4, которые связываются с клеточными рецепторами в разных тканях и оказывают негативные физиологические эффекты.
В норме тиреоидные гормоны участвуют во многих биохимических процессах, поэтому их избыток сопровождается системными нарушениями. У детей возникают патологические катаболические процессы, нарушается углеводный и липидный обмен. Гормоны оказывают токсическое влияние на сердечно-сосудистую и нервную систему, в период детства негативно воздействуют на психику.
Классификация
В зависимости от локализации патологии выделяют 3 типа гипертиреоза: первичный, который обусловлен поражением на уровне щитовидной железы, вторичный, характеризующийся нарушениями работы гипофиза, и третичный, связанный с заболеваниями гипоталамуса. В практической детской эндокринологии важна классификация синдрома по клиническим проявлениям, в которой различают 3 варианта:
Симптомы гипертиреоза у детей
У младенцев клинические проявления возникают в первый месяц жизни. Они включают кишечные расстройства (рвоту, диарею), проблемы с грудным вскармливанием, повышенное беспокойство и нарушения сна. Иногда у новорожденного видна увеличенная щитовидная железа. Зачастую при неонатальном гипертиреозе отмечается регресс симптоматики в течение первого полугодия жизни.
По завершении периода новорожденности среди ведущих признаков гипертиреоза преобладают психоэмоциональные симптомы. У детей появляется беспричинная раздражительность, гиперактивность, капризность и склонность к агрессии. Школьники хуже успевают в учебе, поскольку им становится сложно прилагать волевые усилия и длительно концентрироваться на одном деле.
Физиологические симптомы представлены непереносимостью жары и духоты, усиленным потоотделением, дрожанием пальцев рук. Многие дети жалуются на неприятное чувство сердцебиения, головные боли, которые вызваны повышением артериального давления. Кишечные признаки включают учащение дефекации, периодически спазмы в кишечнике. Ребенок стремительно худеет, хотя аппетит у него не нарушен.
Еще одна группа клинических проявлений включает симптомы основной патологии, которая спровоцировала тиреоидную гиперфункцию. При остром тиреоидите — фебрильная лихорадка, сильные боли по передней поверхности шеи, нарушения глотания, при подострой форме — субфебрильная температура, умеренная болезненность в проекции органа. Выпячивание глаз (экзофтальм) встречается только при гипертиреозе, вызванном болезнью Грейвса.
Осложнения
У детей, страдающих неонатальным гипертиреозом с тиреотоксикозом, риск негативных последствий варьирует в пределах 10-15%. У младенцев возникают нарушения психомоторного развития, задержка роста, а также краниосиностоз — слишком раннее окостенении черепных швов, из-за чего формируется микрокрания. Несовременно диагностированный гипертиреоз у новорожденного может иметь летальный исход.
Диагностика
При физикальном осмотре детский эндокринолог обращает внимание на увеличение щитовидной железы, появление функциональных шумов сердца при аускультации, наличие патологических глазных симптомов. При оценке неврологического статуса врач, как правило, выявляет снижение мышечной силы и тонуса. Затем проводится инструментальная и лабораторная диагностика гипертиреоза:
Лечение гипертиреоза у детей
Консервативная терапия
При тиреотоксикозе ограничивают физическую активность, чтобы не усугублять нарушения терморегуляции и не создавать чрезмерную нагрузку на сердечную мышцу. Детям запрещено давать кофе и крепкий чай, подросткам категорически нельзя употреблять энергетики и спиртные напитки. До нормализации гормонального фона ограничивают поступление в организм йода с контрастными веществами. Медикаментозное лечение гипертиреоза включает:
Хирургическое лечение
Оперативное вмешательство (тиреоидэктомия) выполняется детям с рецидивирующим гипертиреозом, при неэффективности медикаментозной терапии на протяжении 12-18 месяцев, наличии крупных узловых новообразований. Перед хирургическим лечением ребенку рекомендована терапия тиреостатиками до достижения состояния эутиреоза. После операции проводят контроль паратгормона и кальция, по показаниям назначают витамин D.
Прогноз и профилактика
При своевременном начале лечения стойкая ремиссия наступает у 75% детей. Прогноз зависит от причины и степени повышения уровня тиреоидных гормонов, скорости уменьшения зоба и наличия у пациента сопутствующих заболеваний. Первичная профилактика гипертиреоза заключается в предупреждении эндокринных болезней, сопровождающихся нарушением функции щитовидной железы.