Тромбоз: причины, симптомы, диагностика, лечение
Тромбоз – полная или частичная закупорка просвета сосуда пристеночным или подвижным тромбом. Тромб – это плотный сгусток крови, появляющийся вследствие изменения ее текучести. В норме тромбообразование – защитный механизм. Повреждение сосудистой стенки влечет замедление кровотока, накапливание тромбоцитов вокруг повреждения. Тромб буквально «штопает» стенку сосуда.
Классические причины тромбообразования описываются триадой Вихрова: повреждение сосудистой стенки, замедление кровотока и изменение свойств крови [3]. Некоторые тромбы (их называют эмболами) способны передвигаться до более узких участков сосуда, которые и закупоривает полностью или частично. Ежегодно около 25 млн человек погибают от тромбозов, еще больше сталкиваются с нарушениями трофики, вызванными тромбами [3].
Типы сосудистых тромбозов
Наиболее распространены тромбозы нижних конечностей, однако наибольшую опасность представляют собой тромбоэмболия легочной артерии – ТЭЛА – и синдром диссеминированной внутрисосудистой свертываемости – ДВС-синдром.
Тромбоз артерий развивается при закупорке ее просвета тромбом или эмболом. Клинические признаки определяются местом, где произошла такая закупорка, органом или тканью, плохо снабжающемуся кровью или не снабжающемуся ею вовсе. Если закупорка с нарушением проходимости сосуда происходит медленно, открываются «запасные», коллатеральные, сосуды, что смягчает клинические симптомы артериального тромбоза [3]. Тромбозы артерий чаще возникают у мужчин среднего и пожилого возрастов [7].
Тромбоз вен различается в зависимости от локализации поражения на тромбоз глубоких или поверхностных вен и тромбоэмболию легочной артерии. Среди всех сердечно-сосудистых патологий венозные тромбозы по частоте встречаемости занимают третье место, уступая лишь ИБС и атеросклерозам. Третье место в структуре причин смертности занимает ТЭЛА. Начиная с 40 лет, риск развития венозных тромбозов увеличивается вдвое каждые 10 лет [5].
Описывают два варианта поражения вен нижних конечностей: флеботромбоз (первичный тромбоз, тромб непрочно фиксирован) и тромбофлебит (вторичный тромбоз на фоне воспаления стенки сосуда, тромб фиксирован прочно) [6]. Тромбофлебиты чаще ассоциируются с тромбозом вен поверхностных [2]. Чем более крупная вена пострадала от тромбоза, тем ярче его клинические проявления. Окружающие ткани сдавливаются застоем крови, так как к месту окклюзии кровь пребывает, а по направлению к сердцу не движется. Венозные тромбы склонны отрываться и разноситься с током крови (тромбоэмболы). При их попадании в жизненно важные органы развиваются жизнеугрожающие состояния [3].
Причины тромбоза
Факторы риска образования тромбозов
Клиника тромбоза
Симптомы тромбоза могут быть общими независимо от локализации или специфичными. Общие симптомы включают боль при движении и в покое, ограничение подвижности и снижение функционирования пострадавшего органа или ткани.
Диагностика тромбоза
Первичная диагностика основана на подробном анамнезе и антропометрии (окружность голени или бедра). Используются шкалы Уэллса для диагностики острого тромбоза и диагностики ТЭЛА [8,9].
Инструментальная диагностика включает компрессионное или дуплексное сканирование вен, допплерографию с компрессией вен, импедансную плетизмографию, пульмоноангиографию, рентгеноконтрастную или МРТ-флебографию [6,9], КТ и МРТ-ангиографию [7,9].
Для диагностики артериальных тромбозов применяют физические тесты (тест 6-минутной ходьбы, тредмил тест), определение пульсации поверхностно расположенных артерий (артерии тыла стопы), дуплексное сканирование артерий конечностей, ангиографию (рентгеновский снимок сосуда, заполненного рентгенконтрастным веществом) и измерение транскутанного напряжения кислорода [7].
Анализы при тромбозе
Значительную роль в своевременной диагностике тромбозов играют лабораторные показатели. Так, методические рекомендации по ведению пациентов с новой коронавирусной инфекцией предусматривают стратификацию риска коагулопатии у пациентов с СOVID-19 на основе простых лабораторных тестов: D-димер, протромбиновое время, количество тромбоцитов, уровень фибриногена [1,9].
Клинический анализ крови позволяет выявить воспаление. Он же определяет уровень тромбоцитов, то есть самого субстрата тромбоза.
Дополнительно об уровне воспаления в крови и риске тромбоза свидетельствует повышенный уровень С-реактивного белка.
Биохимический анализ в первую очередь демонстрирует уровень глюкозы крови. По ней можно судить о наличии диабета, одного из серьезнейших факторов риска тромбозов.
Также биохимический анализ способен определить уровень протеина С, что также характеризует выраженность риска тромбоза.
Повышенный уровень гомоцистеина в крови также является доказанным на сегодняшний день риском тромбозов, приводящим к невынашиванию беременности и сердечно-сосудистым событиям (инфарктам и инсультам).
D-димер – лабораторный маркер фибринообразования [8]. Он же говорит о наличии воспаления, как и С-реактивный протеин. Уровень D-димера является контрольным показателем COVID-19 и его осложнений, в том числе связанных с тромбозами.
Можно сдать анализы по комплексной программе «Тромбоз», включающей определение уровней Антитромбин-III, D-димера и генетических факторов кардиологических заболеваний и уровень тромбоцитов. Эта программа позволяет определить факт свершившегося тромбоза где-то в организме, а также определить генетическую предрасположенность к нему. Такую программу, как и прочие анализы, предлагает сеть клиник СИТИЛАБ.
Дополнительное определение уровня гомоцистеина, С-реактивного белка поможет определить биохимический риск тромбоза.
Лечение и профилактика тромбозов
Лечение тромбоза включает антикоагулянтную и антиагрегантную, тромболитическую терапию, установку кава-фильтра нижней полой вены, хирургическое удаление тромба [5]. Необходимо иметь в виду осложнения антикоагулянтной терапии: большое кровотечение, гепарин-индуцируемую тромбоцитопению и варфарин-индуцируемый некроз кожи [5]. Для снижения риска продолжения тромбообразования применяют НПВС [2]. С целью вторичной профилактики назначают небольшие дозы гепарина.
Также назначают немедикаментозные методы лечения – эластичное бинтование, компрессионный трикотаж, локальную гипотермию и ЛФК [2, 4].
Профилактика тромбоза включает ряд мероприятий, применяемых в ситуациях повышенного риска тромбообразования.
Церебральный венозный тромбоз при вакцино-индуцированной иммунной тромботической тромбоцитопении
Аннотация
Весной 2021 года появились сообщения о редких и необычных венозных тромбозах, связанных с применением ChAdOx1 и Ad26 (векторная вакцина на основе аденовируса шимпанзе и векторная вакцина на основе аденовируса человека соответственно [прим. перев.]). Использование вакцин COV2.S против коронавируса на основе аденовируса в нескольких странах было на некоторое время приостановлено. Из 7,98 миллиона человек, получивших вакцину Ad26.COV2.S, у 17 пациентов, вакцинированных за 4 недели до возникшего тромбоза, отмечались тромбозы церебральных и абдоминальных вен (с тремя смертельными исходами, связанными с тромбозом вен головного мозга), а среди 35 млн вакцинированных ChAdOx1 описаны 169 случаев тромбоза вен головного мозга.
Эти случаи были связаны с возникновением тромбоцитопении и наличием анти-PF4 антител (антитела к тромбоцитарному фактору 4), что было обозначено как вакцино-индуцированная иммунная тромботическая тромбоцитопения.
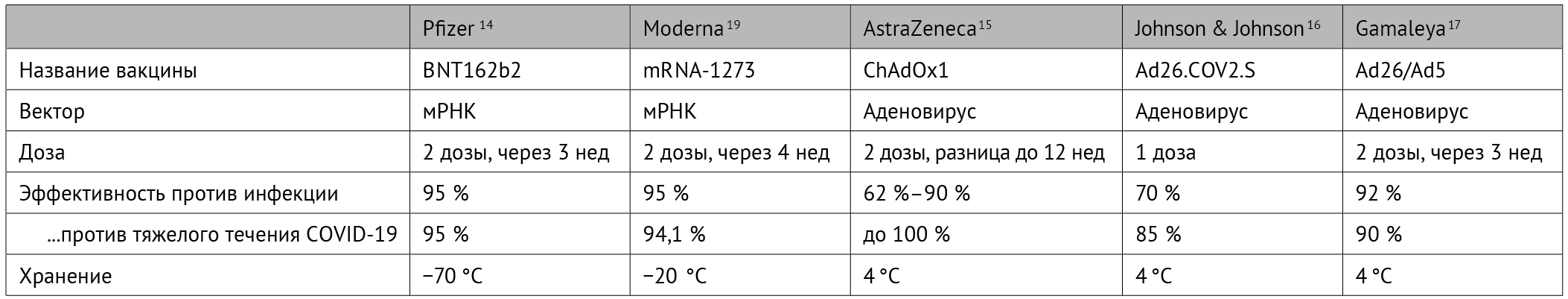
В отличие от связанной гепарин-индуцированной тромбоцитопении с оцениваемой частотой заболеваемости Таблица 1 | Краткое описание вакцин против COVID-19, используемых в настоящее время
Хотя рандомизированные исследования с участием более 60 тыс. «ослепленных» пациентов, которым была проведена вакцинация, показали низкий риск серьезных побочных эффектов, появились сообщения о редких тромботических осложнениях при применении двух вакцин. В этом комментарии авторы сравнивают суммированные известные риски этих вакцин с известными тромботическими и системными рисками от COVID-19.
Тромбоз при COVID-19
Тромботические осложнения при COVID-19 уже хорошо описаны [3, 4, 20, 21]. Как и пациентам без коронавирусной инфекции, пациентам с COVID-19, у которых развивается ВТЭ, рекомендуется терапевтическая антикоагулянтная терапия; тем не менее, нет убедительных доказательств, подтверждающих эмпирическое использование антикоагулянтов у здоровых людей [22]. В исследовании ACTIV-4 (Anti-Thrombotics for Adults Hospitalized With COVID-19, Антитромботические препараты для взрослых, госпитализированных с COVID-19), сравнивался прием антикоагулянтов в терапевтических и профилактических целях на основании уровня D-димера, но набор пациентов в критическом состоянии был остановлен из-за опасности для здоровья больных, рандомизированных на получение антикоагулянтной терапии [23]. Предварительные данные исследования REMAP-CAP (Randomized, Embedded, Multifactorial Adaptive Platform Trial for Community Acquired Pneumonia, Рандомизированное встроенное мультифакториальное исследование адаптивной платформы для внебольничной пневмонии) свидетельствуют о бесполезности терапии антикоагулянтами у пациентов с COVID-19 в критическом состоянии [24].
Среди локализаций артериального и венозного тромбоза при COVID-19 несколько отчетов [25–27] и один систематический обзор [28] указали на небольшой, но значительный риск возникновения церебрального венозного тромбоза (ЦВТ). По некоторым оценкам, COVID-19 увеличивает вероятность ЦВТ более чем в 40 раз, возникая у 1 из 5–15 тыс. госпитализированных с COVID-19 пациентов [4, 29], хотя истинная распространенность этого осложнения среди пациентов с коронавирусной инфекцией неизвестна. Более чем у двух третей пациентов с COVID-19 и ЦВТ отсутствуют традиционные факторы риска [28] с уровнем смертности выше, чем у пациентов с ЦВТ, но не имеющих коронавирусной инфекции [28,29].
Церебральный венозный тромбоз, связанный с вакцинами против COVID-19, основанными на аденовирусе
Ранние сообщения и частота событий
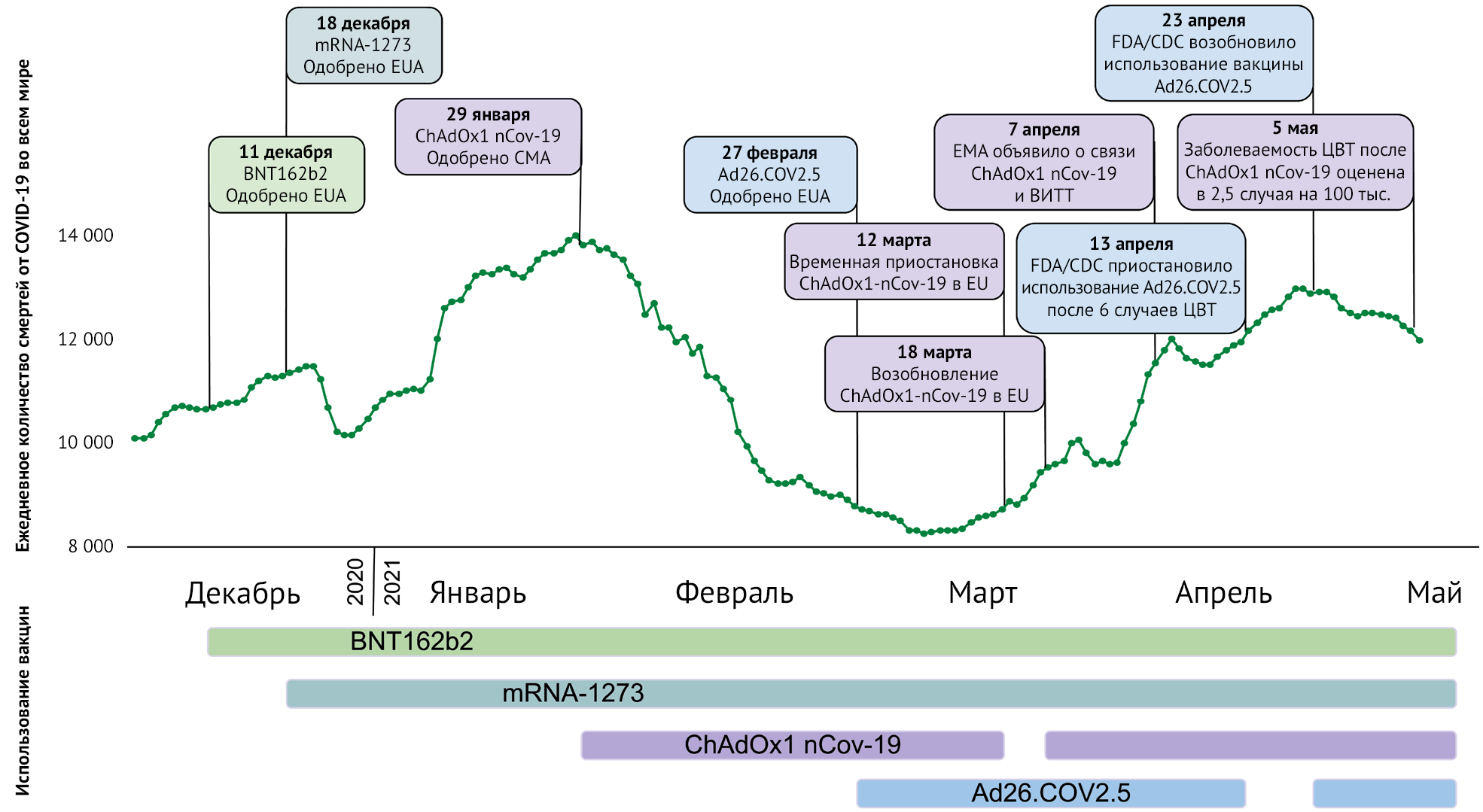
С момента утверждения вакцин против COVID-19 в декабре 2020 года Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) и Европейским агентством лекарственных средств (EMA) было введено более 116 млн доз вакцины в Европе и более 215 млн доз в США, что связано со значительным снижением числа новых случаев заболевания и смертности от COVID-19 (рисунок 1).
В феврале 2021 года после вакцинации ChAdOx1 появились сообщения о пациентах с тромбоцитопенией и ВТЭ необычной локализации, что в нескольких странах привело к приостановке ее применения в середине марта. К 4 апреля 2021 году в EMA было зарегистрировано 169 случаев ЦВТ и 53 случая тромбоза абдоминальных вен среди 35 млн пациентов, получивших вакцину ChAdOx1 [30]. В популяционном когортном исследовании от 5 мая 2021 года, проведенном в Дании и Норвегии, сообщалось об увеличении частоты венозных тромбоэмболических событий, включая ЦВТ, среди людей, получивших вакцину ChAdOx1, без увеличения аналогичных событий в артериальном русле [31]. Эти недавно полученные данные говорят о повышенной частоте возникновения ЦВТ (2,5 на 100 тыс. человек, получивших вакцину ChAdOx1), хотя лабораторные исследования не подтвердили, что эти события вызваны вакцино-индуцированной иммунной тромботической тромбоцитопенией (ВИТТ).
В Соединенных Штатах у 17 из 7,98 млн человек, получивших вакцину Ad26.COV2.S, возникли ЦВТ и тромбоцитопения. В 14 случаях ЦВТ (3 из которых закончились смертельным исходом) [32] Центры по контролю за заболеваниями (CDC) и EMA рекомендовали временное прекращение проведения вакцинации данной вакциной. Двенадцать из этих пациентов подробно описаны See et al. [33]. Авторы суммировали данные зарегистрированных случаев у пациентов в Таблице I в Приложении к данным [33–41]. Важно отметить, что большинство умерших были средней возрастной группы и старше (средний возраст составил 69 лет, диапазон 21–97 лет), что также указывает на низкий риск смерти после вакцины среди более молодых вакцинированных [32].
Уникальное проявление этих тромботических событий с тромбоцитопенией и их временная связь с вакцинацией получили название ВИТТ. Поскольку в EMA и CDC (Centers for Disease Control and Prevention, Центры по контролю и профилактике заболеваний США) поступает больше сообщений о таких случаях, оценочная частота ВИТТ составляет около 1 на 150 тыс. для вакцины ChAdOx1 nCov-19 и 1 на 470 тыс. для вакцины Ad26.COV2.S (рисунок 2), хотя риски могут варьировать в зависимости от возрастной группы и пола. Хотя эти события могут встречаться все чаще, абсолютные их количества невелики, а эпидемиологические данные в подавляющем большинстве продолжают поддерживать безопасность и эффективность вакцин в отношении снижения риска COVID-19 и смерти от COVID-19 (или вакцин) среди получивших вакцины независимо от возраста (Таблица 2) [15, 19, 32, 42].
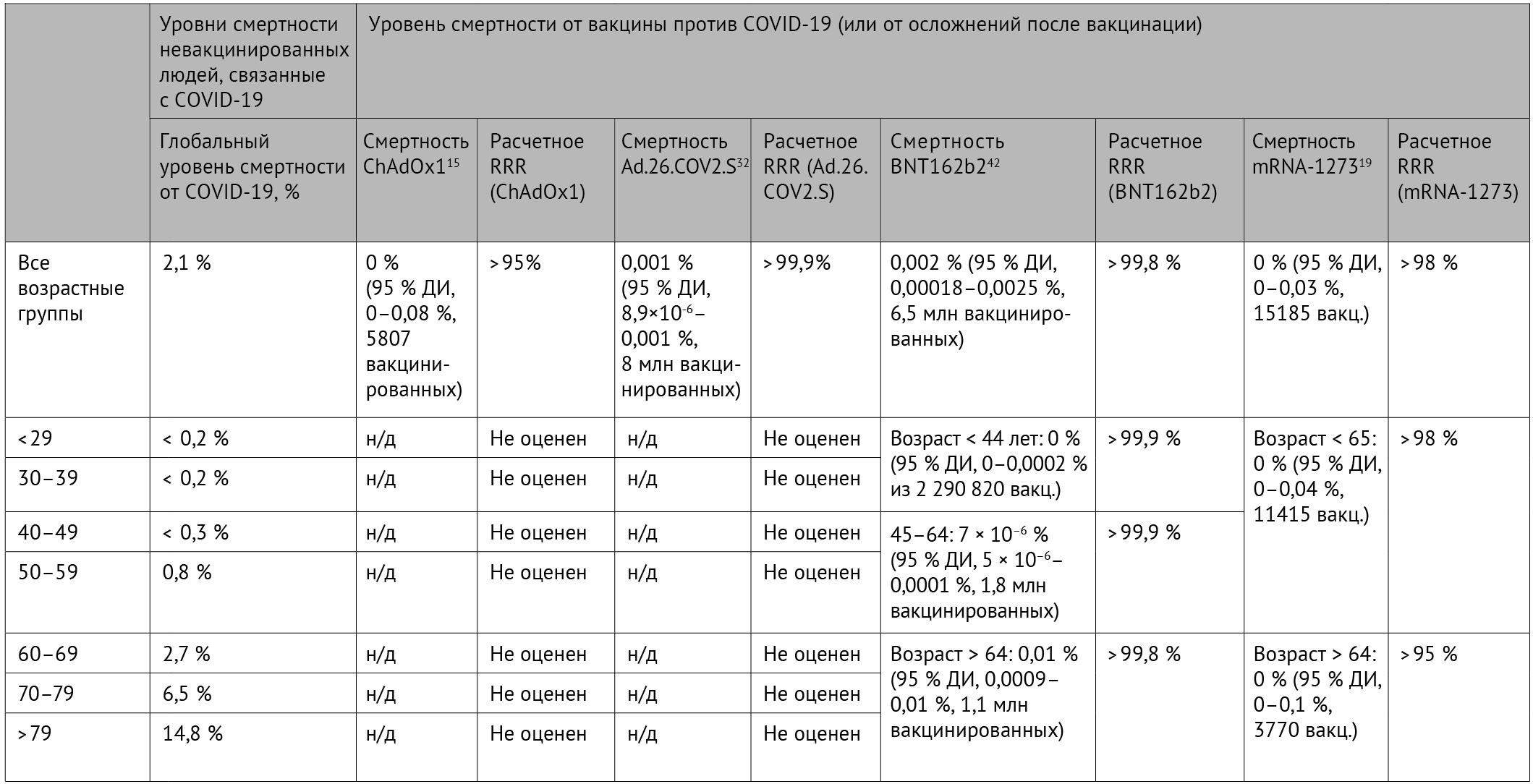
Таблица 2 | Уровни смертности по возрастным группам
Исходные данные были взяты из опубликованных клинических испытаний и обсервационных когортных исследований, в которых сообщалось о смертности после введения вакцины. Показатели смертности выражены как уровни заболеваемости с 95 % доверительным интервалом, оценивались с помощью метода Агрести-Коулла. Расчетное RRR смертности, связанное с наличием заболевания COVID-19 (или вакцинации) для каждой вакцины против коронавируса для минимальной оценки эффекта было рассчитано с использованием верхнего предела 95 % доверительного интервала. Например, 88 пациентов из 8 миллионов, получивших Ad.26. COV2.S, были исключены (по разным причинам), при этом верхний предел относительной смертности для этой вакцины составляет 0,001 %. По сравнению с глобальным уровнем смертности от COVID-19 (2,1 %), минимальный RRR составляет > 99,9 %.
RRR, относительное снижение риска.
Патофизиология
О случаях возникновения ВИТТ после других вакцин на основе аденовируса или вакцины против COVID-19 на основе мРНК не сообщалось. Хотя известно, что аденовирусы активируют тромбоциты, маловероятно, что тромбоцитопения, возникающая после вакцинации, вызвана аденовирусным вектором [15]. Кроме того, случаев ВИТТ после введения других вакцин против коронавируса, разработанных на основе аденовируса (AD5-nCOV или Gam-COVID-Vac), или вакцин против вируса Эбола на основе аденовируса (Ad5-EBOV и Ad26.ZEBOV) зарегистрировано не было [43].
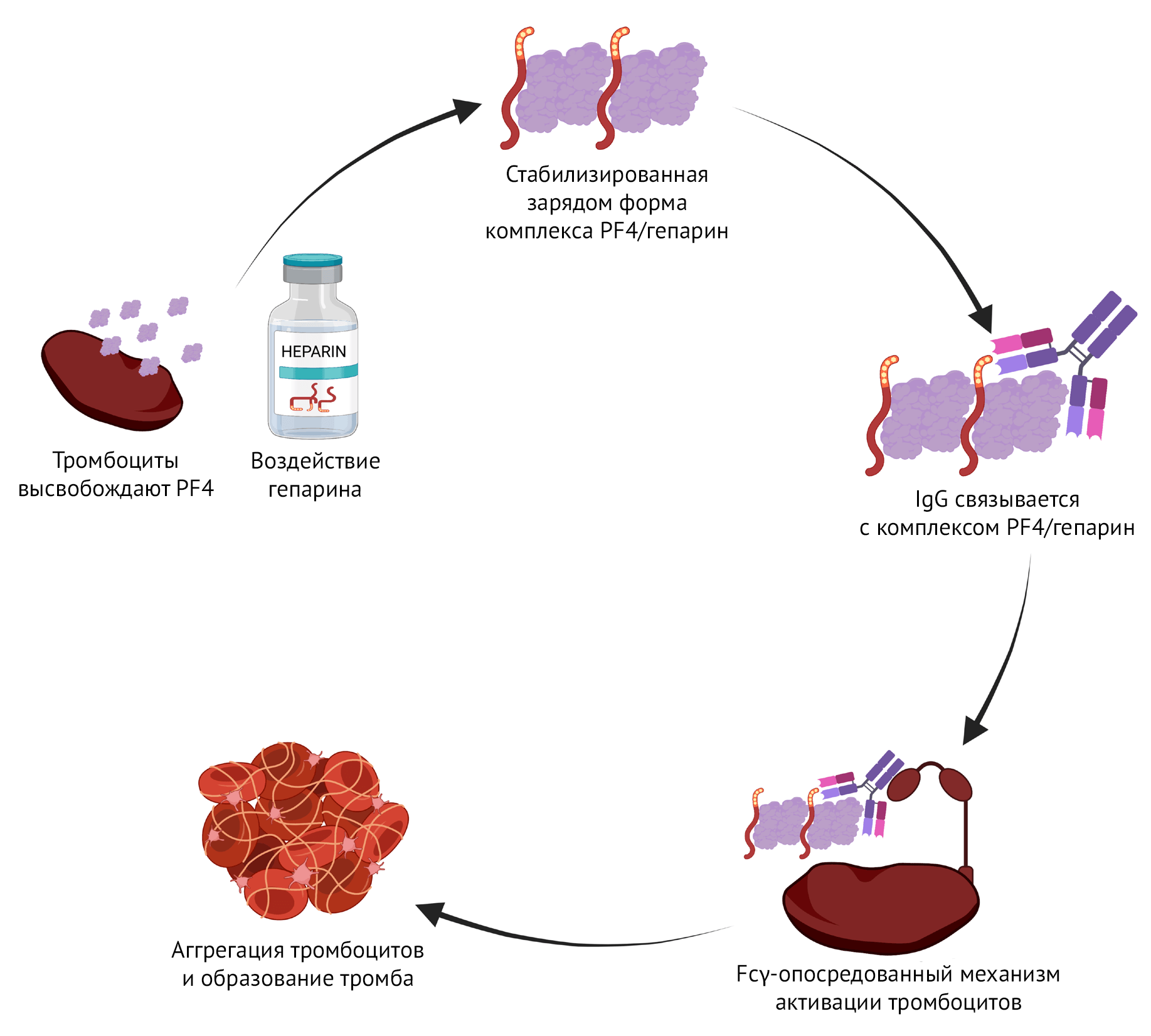
Из-за связи нетипичных тромботических осложнений с тромбоцитопенией возникло подозрение на наличие воспалительной коагулопатии. Исследователи в сыворотках пациентов с ВИТТ обнаружили антитела против PF4 [35], что свидетельствует об аутоиммунном ответе на вакцину. Аналогичный механизм был описан при гепарин-индуцированной тромботической тромбоцитопении (ГИТТ; рисунок 2) [44].
При ГИТТ антитела направлены против PF4 (обнаруженного на тромбоцитах и эндотелии сосудов) и образуют комплекс с гепарином. Как только этот комплекс формируется, область Fc на тромбоцитах захватывается областью Fc на соседних тромбоцитах, что способствует их агрегации [45]. Тромбоцитопения возникает, когда тромбоциты, покрытые IgG, удаляются ретикулоэндотелиальной системой и расходуются в местах тромбоза [46].
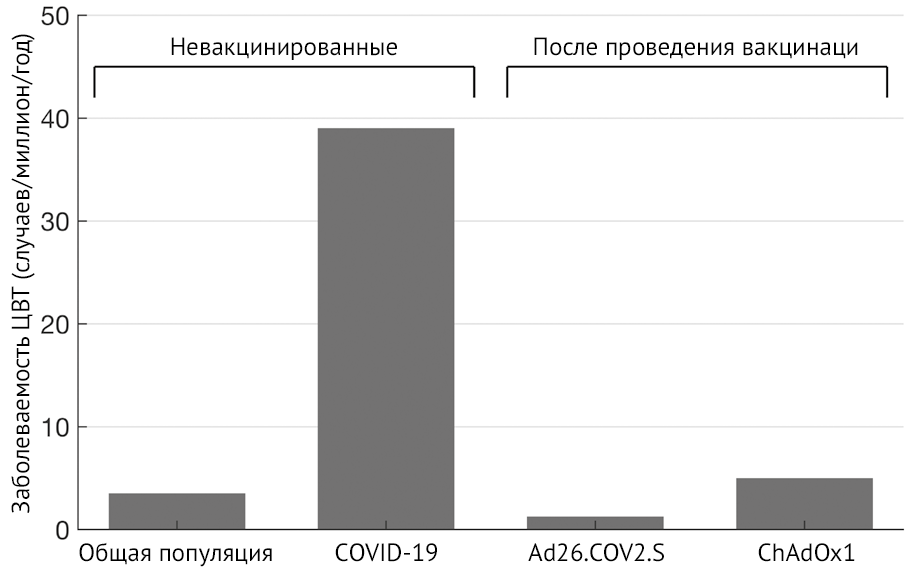
Время после вакцинации ChAdOx1 до появления симптомов составляет от 5 до 16 дней [35, 36]. Пациенты ранее не получали гепарин, что позволяет предположить, что появление анти-PF4 антител является новым гуморальным ответом на вакцину. Одним из возможных объяснений этого может быть образование комплекса нуклеиновой кислоты, содержащейся в вакцине, с PF4 [35]. Важно отметить, что частота случаев ВТЭ как части этого уникального ответа на вакцины против коронавируса остается низкой, с чрезвычайно редкими случаями тромбоза, возникающими в корковых венах и синусах твердой мозговой оболочки (рисунок 2). Новизна этого открытия предполагает, что эти случаи могут быть более частыми, чем о них сообщается (рисунок 3).
Рисунок 3 | Годовые показатели уровней заболеваемости тромбозом вен головного мозга (ЦВТ)
Диагностическая оценка церебральных венозных тромбозов и вакцино-индуцированной тромботической тромбоцитопении
У пациентов с ЦВТ, госпитализированных в течение четырех недель после вакцинации вакциной на основе аденовируса, можно с высокой долей вероятности подозревать ЦВИ с ВИТТ. У пациентов с новой сильной головной болью, подострой энцефалопатией, потерей зрения, судорогами или очаговым неврологическим дефицитом рекомендуется выполнение общего анализа крови и компьютерной томографии головы с венографией, ангиографией или без нее или магнитно-резонансной томографии с венограммой [47]. Если количество тромбоцитов
Тактика ведения пациентов с церебральным венозным тромбозом и вакцино-индуцированной иммунной тромботической тромбоцитопенией
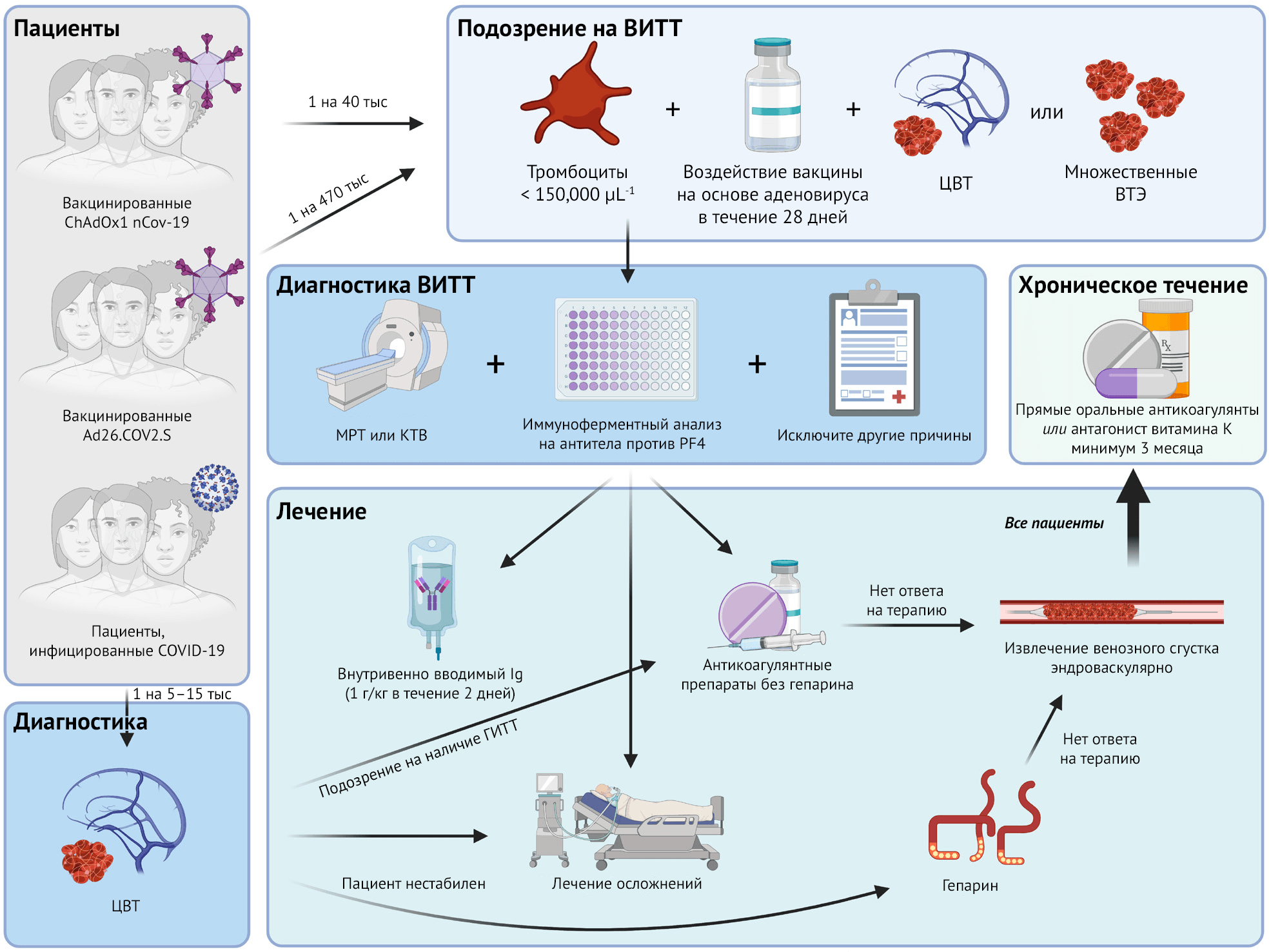
Учитывая аналогичный механизм активации тромбоцитов, индуцированный формированием анти-PF4 антител, и при ВИТТ, и при ВИТТ, эксперты рекомендуют проводить лечение ВИТТ параллельно с лечением ГИТТ (рисунок 4) [47].
Применение фармакологических препаратов при предполагаемой вакцино-индуцированной иммунной тромботической тромбоцитопении
Эмпирические медицинские вмешательства должны быть нацелены как на аутоиммунные механизмы, так и на тромботические последствия. Поскольку активация тромбоцитов через образование аутоантител считается основным посредником тромбоза, рекомендуется вводить внутривенный иммуноглобулин в дозе 1 г/кг в день в течение двух дней [37], хотя рекомендации Американского общества гематологов от 2018 года не поддерживают его рутинное использование при синдроме, вызванном ГИТТ [51]. Потенциальные побочные эффекты от применения внутривенного иммуноглобулина, включая головную боль, приливы жара и асептический менингит, следует сопоставлять с его потенциальной пользой. При тяжелой тромбоцитопении может быть рассмотрено использование высоких доз кортикостероидов, плазмафереза и заместительной терапии препаратами фибриногена.
Хотя нет никаких доказательств того, что введение гепарина при ЦВТ, связанного с ВИТТ, опасно, из-за наличия антител к PF4 и перекрестных механизмов с ГИТТ, рассматривается применение внутривенных антикоагулянтов, не содержащих гепарин (аргатробан, бивалирудин, фондапаринукс). После клинической стабилизации состояния пациента может быть рассмотрен прием пероральных антикоагулянтов (ривароксабан, апиксабан, дабигатран).
Антикоагулянтная терапия прямым пероральным антикоагулянтом или антагонистом витамина К должна продолжаться от 3 до 6 месяцев или до разрешения ЦВТ по данным нейровизуализации [49]. Клинические рекомендации Американской кардиологической ассоциации/Американской ассоциации инсульта рекомендуют начинать или продолжать антикоагулянтную терапию при наличии венозного застоя с геморрагиями [49], хотя этот вопрос остается дискутабельным [53]. В таких случаях связанный с этим отек и размер гематомы могут потребовать декомпрессивной гемикраниэктомии или эвакуации гематомы для предотвращения вклинения, способного привести к смертельному исходу. В качестве альтернативы у таких пациентов может быть использована эндоваскулярная тромбэктомия.
При тромбоцитопении при ВИТТ переливание тромбоцитарной массы не рекомендуется [37, 48], если только у пациента не имеется опасное для жизни кровотечение [48], как указано в рекомендациях по лечению ГИТТ [51]. Более того, из-за нетипичного механизма внутричерепного кровоизлияния при ЦВТ, возникающего вследствие венозного застоя, оно вряд ли прекратится при переливании тромбоцитарной массы. Восстановление венозного оттока с использованием антикоагулянтной терапии или эндоваскулярных вмешательств имеет решающее значение для уменьшения местного венозного застоя и снижения внутричерепного давления, что может предотвратить образование отека и нарастание внутричерепной гематомы.
Остается неясным, но гепарин (нефракционированный и низкомолекулярный) может ухудшить симптомы ВИТТ из-за наличия перекрестных реакций с ГИТТ. В двух ранее опубликованных сериях случаев ВИТТ [35, 36] гепарин был введен 11 из 16 пациентам, 5 из них в скором времени умерли. Основываясь на этих ограниченных данных, остается неясным, отражает ли этот уровень смертности естественное течение заболевания или он является следствием осложнений традиционных вмешательств при венозном тромбозе. Тем не менее, увеличение количества тромбоцитов без признаков рецидива или усиления тромбоза наблюдалось у пациентов, одновременно получавших преднизолон и внутривенно вводимые иммуноглобулины.
Эндоваскулярные методы лечения
У пациентов с ухудшившимся психическим состоянием можно рассмотреть возможность эндоваскулярной тромбэктомии в соответствии с рекомендациями Американской кардиологической ассоциации/Американской ассоциации инсульта (класс IIb, уровень доказательности C) [49, 54]. Однако в недавнем рандомизированном клиническом исследовании TO-ACT (Thrombolysis or Anticoagulation for Cerebral Venous Thrombosis, Тромболизис или антикоагулянтная терапия при тромбозе вен головного мозга) преимущество тромбэктомии перед медикаментозным лечением при ЦВТ продемонстрировано не было [55]. Поскольку исследование TO-ACT было преждевременно закончено из-за своей бесперспективности, возможно, тромбэктомия может быть успешно применена у некоторых пациентов с рефрактерной ЦВТ. У пациента, перенесшего венозную тромбэктомию, если у него подтверждено или подозревается наличие ВИТТ, могут быть рассмотрены альтернативы промыванию гепаринизированным физраствором (например, бивалирудин [56]).
Парадигмы и проблемы вакцины против COVID-19
Существуют трудности с оценкой рисков и преимуществ дальнейшего использования вакцин ChAdOx1 и Ad26.COV2.S. В случаях наличия потенциально жизнеугрожающих заболеваний, лечение, сопряженное со значительным риском, является допустимым. И наоборот, риски, связанные с профилактикой заболевания, гораздо менее оправданы. Вакцинация против COVID-19 с использованием этих двух вакцин сопряжена с риском серьезных осложнений с очень низкой частотой возникновения заболевания (ВИТТ). В настоящее время неизвестно, какие факторы, если таковые имеются, влияют на риск возникновения ВИТТ. Все вакцины, которые в настоящее время применяются в Соединенных Штатах и Европе, являются доступными в соответствии с постановлениями об их экстренном использовании, а не в рамках традиционного порядка их утверждения. Такие постановления выдаются на основе промежуточного анализа данных, которые могут не полностью отражать профили побочных эффектов применения препаратов. В странах с широко распространенной передачей SARS-CoV-2 и Всемирная организация здравоохранения, и EMA предположили, что преимущества вакцинации намного перевешивают риск ВИТТ. Перед проведением вакцинации вакциной на основе аденовируса, клиницистам рекомендуется принимать совместное решение и информировать пациента об очень низком риске возникновения ВИТТ.
После заявления EMA 18 марта 2021 года, использование вакцины ChAdOx1 было возобновлено во многих европейских странах. Дания 14 апреля объявила, что вакцина ChAdOx1 не будет использоваться после двух случаев возникновения ВИТТ из 140 тыс. вакцинаций. После отчета Комитета по оценке рисков фармаконадзора EMA 20 апреля 2021 года компания Johnson & Johnson объявила о своем намерении продолжить применение вакцины Ad26.COV2.S в Европе, а 23 апреля CDC и FDA рекомендовали возобновить вакцинацию Ad26.COV2.S в США на основании анализа риска и пользы в сторону положительного [57]. Для защиты от COVID-19 и новых штаммов инфекции может потребоваться ревакцинация или проведение ежегодной вакцинации. Пациентам, у которых ВИТТ развился вследствие вакцины, разработанной на основе аденовируса, авторы рекомендуют при необходимости введения второй дозы использовать вакцину на основе мРНК [58]. При отсутствии ВИТТ после первой вакцинации, CDC рекомендуют проводить повторную иммунизацию тем же типом вакцины [59].
Пробелы в знаниях
Механизм, посредством которого после применения аденовирусной вакцины формируются антитела к PF4, остается неизвестным. Не ясно, имеется ли склонность к развитию ВИТТ больше в церебральных синусах или абдоминальных венах, в отличие от более распространенных для ВТЭ локализаций (таких как легкие или ноги). На основании популяционных данных неизвестно, почему при ВИТТ возникает предрасположенность к венозной, а не к артериальной тромбоэмболии [31]. Несмотря на то, что это редкое событие, неясно, почему данное состояние чаще встречается у молодых женщин, хотя в сериях случаев ВИТТ в Великобритании сообщается, что 40 % пациентов были мужчинами, при этом их возраст был старше (до 70 лет) [37]. Прогнозировать возникновение ВИТТ будет непросто. Для пациентов с повышенным риском развития ВТЭ (например, семейный анамнез, состояние гиперкоагуляции, применение пероральных контрацептивов, предшествующая ВТЭ) остается неизвестным, входят ли они в группу риска по формированию ВИТТ. Однако когда альтернативные вакцины станут доступны, пациентам можно будет рекомендовать отдавать предпочтение вакцинам на основе мРНК.
Выводы
Последствия пандемии COVID-19 невозможно недооценить. Глобальные меры в области здравоохранения, направленные на достижение цели по сокращению распространения вируса, включая общественное просвещение, повсеместное ношение масок, социальное дистанцирование и мытье рук, лишь замедлили распространение пандемии. На сегодняшний день, наилучшее лечение коронавирусной инфекции включает поддерживающую терапию и лечение параинфекционных осложнений, в том числе тромботических. Появление более заразных штаммов вируса может ускорить его распространение.
Оптимальным средством снижения распространения SARS-CoV-2 остается массовая вакцинопрофилактика и формирование коллективного иммунитета. Вакцины против COVID-19 доказали свою эффективность против заражения SARS-CoV-2, возникновения тяжелого течения коронавирусной инфекции и доказали свою действенность против появляющихся новых штаммов SARS-CoV-2. Из более редких осложнений этих вакцин, вероятно, аутоиммунно-опосредованная тромботическая тромбоцитопения будет появляться все чаще. На данный момент, это осложнение является уникальным для вакцин против коронавируса на основе аденовируса, которому преимущественно подвержены женщины молодого и среднего возраста без ранее имеющихся заболеваний. Раннее распознавание, диагностика и лечение ВИТТ с учетом его патофизиологии (то есть подавление антительного ответа с помощью внутривенно вводимых иммуноглобулинов, предотвращение переливания тромбоцитарной массы, снижение тромбозной нагрузки с помощью негепариновых антикоагулянтов) могут снизить текущий высокий уровень смертности при ВИТТ (20–30 %) [32, 58].