Триожиналь свечи или овестин что лучше
Триожиналь свечи или овестин что лучше
А.В. Кузьменко, В.В. Кузьменко, Т.А. Гяургиев
Кафедра урологии (зав. – д.м.н., доц. А. В. Кузьменко) ФГБОУ ВО «Воронежский государственный медицинский университет им. Н. Н. Бурденко», Воронеж, Россия
1. Alyaev Yu. G., Glybochko P. V., Pushkar D. Y. Urology. Russian clinical guidelines. M.: GEOTAR-Media; 2018. Russian (Аляев Ю.Г., Глыбочко П.В., Пушкарь Д.Ю. Урология. Российские клинические рекомендации. М.: ГЭОТАР-Медиа, 2018).
2. Gadzhieva Z.K., Kasilov Y.B. Features of the approach to prevention of recurrent infections of the lower urinary tract. Urologiia. 2016;3:65–76. Russian (Гаджиева З.К., Казилов Ю.Б. Особенности подхода к профилактике рецидивирующей инфекции нижних мочевыводящих путей. Урология 2016;3:65–76).
3. Kuzmenko A.V., Gyaurgiev T.A., Kuzmenko V.V. Efficacy of phosphomycin trometamol in acute uncomplicated cystitis. Urologiia. 2018;6:70–75. Russian (Кузьменко А.В., Гяургиев Т.А., Кузьменко В.В. Эффективность применения фосфомицина трометамола при остром неосложненном цистите. Урология. 2018;6:70–75).
4. Kuzmenko A.V., Gyaurgiev T. A., Kuzmenko V.V. The Effectiveness of complex phytopreparations in the treatment of uncomplicated lower urinary tract infection in women. Urologiia. 2018;4:10–13. Russian (Кузьменко А.В.,Гяургиев Т.А., Кузьменко В.В. Эффективность применения комплексных фитопрепаратов в лечении неосложненной инфекции нижних мочевыводящих путей у женщин. Урология 2018;4:10–13).
5. Kazilov Y.B., Gadzhieva Z.K. Incidence of various urinary disorders. Urology 2016;5:109–114. Russian (Казилов Ю.Б., Гаджиева З.К. Распространенность различных нарушений мочеиспускания. Урология 2016;5:109–114).
6. Kuzmenko A.V., Gyaurgiev T. A., Kuzmenko V.V Chronobiological approach to the treatment of chronic recurrent bacterial cystitis in the acute stage. Urologiia. 2017;2:60–65. Russian (Кузьменко А.В., Гяургиев Т.А., Кузьменко В.В. Хронобиологический подход к терапии хронического рецидивирующего бактериального цистита в стадии обострения. Урология. 2017;2:60–65).
7. Balan. E.G., Esifidze Z.T., Gadzhieva Z.K. Hormone replacement therapy and urogenital disorders. Consilium Medicum 2001;7:4. Russian (Балан В.Е.,Есефидзе З.Т., Гаджиева З.К. Заместительная гормонотерапия урогенитальных расстройств. Consilium Medicum 2001;7:4).
8. Pushkar D.Yu., Gvozdev M.Yu. Dynamics of symptoms of genitourinary menopausal syndrome and frequency of recurrences of lower urinary tract infections in women in peri- and postmenopausal on the background of combined therapy with Triozhinal. Gynecology 2018;20(6):67–72. Russian (Пушкарь Д.Ю., Гвоздев М.Ю.Динамика симптомов генитоуринарного менопаузального синдрома и частоты рецидивов инфекций нижних мочевых путей уженщин в пери- и постменопаузе на фоне комбинированной терапии препаратом Триожиналь. Гинекология 2018;20(6):67–72).
9. Balan. E.G., Kovaleva L.A., Tikhomirova E.V. Genitourinary or urogenital syndrome possibility of long-term therapy. Consilium Medicum 2016;12:98–101. Russian (Балан В.Е., Ковалева Л.А., Тихомирова Е.В.Генитоуринарный или урогенитальный синдром возможности длительной терапии. Consilium Medicum. 2016;12:98–101).
10. Ermakova E.I. et. al. Genitourinary menopausal syndrome: diagnosis and principles of treatment (brief clinical recommendations). Russian Bulletin of obstetrician-gynecologist 2017;17(6):89–95. Russian (Ермакова Е.И. и др. Генитоуринарный менопаузальный синдром: диагностика и принципы лечения (краткие клинические рекомендации). Российский вестник акушера-гинеколога, 2017; 7(6):89–95).
11. Gorbunova E.A., Apolikhina I.A. Atrophic cystouretritis as one of the faces genitourinary syndrome. Effective pharmacotherapy 2015;36:32–39. Russian (Горбунова Е.А., Аполихина И.А. Атрофический цистоуретрит как одна из граней генитоуринарного синдрома. Эффективная фармакотерапия. 2015;36:32–39).
12. Andrew M. Kaunitz, JoAnn E. Manson. Management of Menopausal Symptoms. Obstet Gynecol 2016;126(4):859–876.
13. Rahn D.D., Carberry C., Sanses T.V., Mamik M.M., Ward R.M., Meriwether K.V., Olivera C.K., Abed H., Balk E.M., Murphy M.; Society of Gynecologic Surgeons Systematic Review Group. Vaginal Estrogen for Genitourinary Syndrome of Menopause: A Systematic Review. Obstet Gynecol 2014;124(6):1147–1156.
14. Erekson E.A., Yip S.O., Wedderburn T.S., et al. The VSQ: a questionnaire to measure vulvovaginal symptoms in postmenopausal women. Menopause. 2013;20(9):973–979.
15. Utian W.H., Maamari R. Attitudes and approaches to vaginal atrophy in postmenopausal women: a focus group qualitative study. Climacteric. 2014;17(1):29–36.
16. Santoro N., Epperson C.N., Mathews S.B. Menopausal Symptoms and Their Management. Endocrinol Metab Clin North Am. Author manuscript 2015;44(3):497–515.
17. Barlow D.H., Samsioe G., Van Geelen J.H. A study of European women’s experience of the problems of urogenital ageing and its management. Maturitas. 1997;27:239–247.
18. Iosif C.S., Batra S., Ek A., Astedt B. Estrogen receptors in the human female lower urinary tract.Am J Obstet Gynecol. 1981;141:817–820.
19. Wurz G.T., Kao C.J., DeGregorio M.W. Safety and efficacy of ospemifene for the treatment of dyspareunia associated with vulvar and vaginal atrophy due to menopause. Clin Interv Aging. 2014;9:1939–1950.
20. Nappi R.E., Panay N., Bruyniks N., Castelo-Branco C., De Villiers T.J., Simon J.A. The clinical relevance of the effect of ospemifene on symptoms of vulvar and vaginal atrophy. Climacteric. 2015;18(2):233–240.
21. Parsons C.L. The role of the urinary epithelium in the pathogenesis of interstitial cystitis/prostatitis/urethritis. Urol. 2007;69(4): 9–16.
22. Balan V. E., Ezeiza Z. T., Gadzhieva Z. K. urinary incontinence in menopause and principles of their treatment. BC. 2000;8(7). Russian (Балан В.Е.,Есефидзе З.Т., Гаджиева З.К. Нарушения мочеиспускания в климактерии и принципы их лечения. РМЖ. 2000;8(7)).
Урогенитальные расстройства в постменопаузе и заместительная гормонотерапия
Изменение демографической структуры общества во второй половине XX в. привело к увеличению в популяции доли женщин старшей возрастной группы. С каждым годом возрастает число женщин, вступающих в период менопаузы. Если
Изменение демографической структуры общества во второй половине XX в. привело к увеличению в популяции доли женщин старшей возрастной группы. С каждым годом возрастает число женщин, вступающих в период менопаузы. Если 75 лет принять за 100%, то продолжительность препубертатного периода составляет 16%, репродуктивного — 44%, пременопаузального — 7%, а постменопаузального — 33% (H. Нaney, 1986). То есть более трети своей жизни женщина проводит в состоянии дефицита женских половых гормонов. Менопауза, не являясь собственно заболеванием, приводит к нарушению эндокринного равновесия в организме женщины, вызывая приливы, раздражительность, бессонницу, урогенитальные расстройства, а также повышая риск развития остеопороза и сердечно-сосудистых заболеваний. Все эти данные свидетельствуют о необходимости разработки целого ряда медицинских и социальных мер по защите здоровья, сохранению работоспособности и достойного качества жизни женщин пери- и постменопаузального периода.
В последние годы в симптоматологии климактерических нарушений стала лидировать проблема урогенитальных расстройств, что связано с их выраженным отрицательным влиянием на качество жизни женщины в постменопаузе. Частота развития возрастных урогенитальных расстройств достигает 30%. В перименопаузальном периоде урогенитальные нарушения встречаются у 10% женщин, тогда как в возрастной группе 55—60 лет — у 50%. К 75 годам уже 2/3 женщин испытывают урогенитальный дискомфорт, а после 75 лет трудно встретить женщину, у которой не наблюдалось отдельных симптомов урогенитальных расстройств.
Урогенитальные расстройства в климактерии — это симптомокомплекс вторичных изменений, связанных с развитием атрофических и дистрофических процессов в эстроген-зависимых тканях и структурах нижней трети мочеполового тракта, мочевом пузыре, уретре, влагалище, связочном аппарате малого таза и мышцах тазового дна.
Прогрессирующее увеличение с возрастом частоты развития урогенитальной атрофии связывают с развивающимися на фоне эстрогенного дефицита необратимыми возрастными метаболическими изменениями. Влагалище, уретра, мочевой пузырь и нижняя треть мочеточников имеют единое эмбриональное происхождение и развиваются из урогенитального синуса. Это объясняет наличие рецепторов к эстрогенам, прогестерону и андрогенам в мышцах, слизистой оболочке, сосудистых сплетениях влагалища, мочевого пузыря и уретры, а также в мышцах и связочном аппарате малого таза.
Процессы старения урогенитального тракта развиваются в двух направлениях:
Атрофический вагинит возникает в результате эстрогенного дефицита и характеризуется резким истончением слизистой оболочки влагалища, прекращением пролиферативных процессов во влагалищном эпителии, уменьшением продукции гликогена эпителиальными клетками, снижением или полным исчезновением лактобацилл, повышением влагалищного рН (см. таблицу 1).
Основные клинические проявлениями атрофического вагинита — это сухость и зуд во влагалище, рецидивирующие выделения, диспареуния, контактные кровянистые выделения.
Диагностика атрофического вагинита включает:
К проявлениям атрофического цистоуретрита относятся «сенсорные» или раздражающие симптомы:
Обследование женщин с расстройствами мочеиспускания:
Вычленение симптомов атрофического вагинита и цистоуретрита условно, так как в большинстве случаев они сочетаются. Различные сочетания симптомов атрофического вагинита и цистоуретрита позволили выделить три степени тяжести урогенитальных расстройств (В. Е. Балан, 1997).
К легким урогенитальным расстройствам (16% женщин) относится сочетание симптомов атрофического вагинита и «сенсорных симптомов» атрофического цистоуретрита без нарушения акта мочеиспускания.
К среднетяжелым урогенитальным расстройствам (80% женщин) относится сочетание симптомов атрофического вагинита, цистоуретрита и истинного недержания мочи при напряжении.
К тяжелым урогенитальным расстройствам (4% женщин) относится сочетание симптомов атрофического вагинита, цистоуретрита, истинного недержания мочи при напряжении и неудержание мочи.
Итак, установлено, что эстрогенный дефицит является причиной развития урогенитальных нарушений у женщин в климактерии. Проблема лечения урогенитальных расстройств неоднозначна. Акцент ставится на том, какой вид заместительной гормонотерапии (ЗГТ) считать оптимальным. ЗГТ урогенитальных нарушений может осуществляться препаратами, обладающими как системным, так и местным действием. К системной ЗГТ относятся все препараты, содержащие эстрадиол, эстрадиол валерат и конъюгированные эстрогены.
К местной ЗГТ — препараты, содержащие эстриол. Выбор типа ЗГТ для лечения урогенитальных расстройств является индивидуальным и зависит от возраста пациентки, длительности постменопаузы, ведущих жалоб, необходимости лечения климактерического синдрома либо профилактики поздних метаболических нарушений.
Назначение системной ЗГТ должно соответствовать общепринятым правилам с учетом абсолютных и относительных противопоказаний. При назначении ЗГТ пациенткам с урогенитальными нарушениями преследуется цель восстановления нормального состояния местных гормонозависимых структур нижних отделов мочеполовой системы и стимуляции механизмов биологической тканевой защиты.
При решении вопроса о выборе типа препарата для ЗГТ крайне важно определить:
При интактной матке применяется комбинированная терапия препаратами, содержащими эстрогены и гестагены:
У женщин после гистерэктомии системное воздействие обеспечивает монотерапия натуральными эстрогенами в циклическом или непрерывном режиме (эстрофем, прогинова, климара, дивигель, эстрадерм).
Приоритетная роль в выборе ЗГТ расстройств урогенитального тракта, обусловленных снижением функции гонад, принадлежит эстриол-содержащим препаратам, обладающим избирательной активностью в отношении мочеполовой системы. Специфичность действия эстриола определяется особенностями его метаболизма и сродством с соответствующими рецепторными системами. Местный эффект стероидных гормонов реализуется путем пассивной диффузии их в клетки организма. Задерживаясь лишь в клетках чувствительных тканей, они образуют комплексы с цитозольными рецепторами с последующей транслокацией в ядро клетки. Таким путем реализуется действие на уровне генетических структур клетки. Это и определяет специфичность эффекта, свойственного данной ткани.
Ответ тканей на воздействие эстрогенов определяется концентрацией рецепторов, их структурой и свойствами эстрогенов. Эстриол является конечным метаболитом в обмене эстрогенов. Он выводится из организма в конъюгированной форме с мочой и лишь в незначительном количестве экскретируется с калом, в основном в неконъюгированной форме.
При пероральном введении эстриола его максимальная концентрация в плазме крови достигается через 1-2 ч. Попавший в плазму крови эстриол не связывается с глобулином, связывающим половые стероиды, и довольно быстро элиминируется. Эстриол является наименее активным эстрогеном с кратковременным действием.
Установлено, что ткани, чувствительные к эстриолу, широко представлены в нижних отделах урогенитального тракта. Терапия эстриолом способствует развитию и восстановлению влагалищного эпителия, а также приводит к восстановлению основных элементов соединительной ткани — коллагена и эластина. При этом главным в назначении эстриол-содержащих препаратов является минимальное системное действие. Известно, что для стимуляции развития эндометрия связь его рецепторов с эстрогеном должна быть длительной, не менее 8—10 ч. Эстриол же связывается с чувствительными к нему структурами не более чем на 2—4 ч. Такого непродолжительного действия недостаточно для пролиферативной реакции эндометрия, но достаточно для эффективного воздействия на структуры нижних отделов урогенитального тракта. Таким образом, при однократном введении эстриол связывается с ядерным рецептором на непродолжительное время и не вызывает пролиферацию эндометрия, поэтому при его назначении не требуется добавления прогестагенов.
При урогенитальных расстройствах традиционно отдается предпочтение местному введению эстрогенов и именно эстриола (овестин) в мазях и свечах (см. таблицу 2).
В любой форме эстриол-содержащие препараты принимаются один раз в сутки. Не рекомендуется сочетание системных и местных форм препарата.
Выбор терапии зависит также от степени тяжести урогенитальных расстройств.
При легкой степени тяжести урогенитальных расстройств применяются препараты эстриола (свечи, крем) ежедневно или три раза в неделю, в зависимости от степени выраженности клинических симптомов. При сочетании явлений атрофического вагинита или атрофического цистоуретрита с климактерическим синдромом назначаются препараты для системной ЗГТ.
При средней степени тяжести урогенитальных расстройств проводится сочетанная терапия (системная и местная) не менее шести месяцев для нормализации уродинамических показателей.
При тяжелой степени урогенитальных расстройств в случае имеющихся показаний к системной ЗГТ проводится комбинированная терапия препаратами для системной ЗГТ в сочетании с местным введением препаратов эстриола и одного из препаратов аддитивного воздействия, обладающих избирательным действием на холинергические (парасимпатические) и адренергические (симпатические) или мускариновые рецепторы, расположенные в мышечной стенке мочевого пузыря и различных структурах урогенитального тракта: гладкомышечной мускулатуре уретры и мышцах тазового дна, участвующих в создании уретральной поддержки. Комбинированную терапию необходимо проводить в течение шести месяцев и более, после чего вопрос о типе терапии решается индивидуально в отношении каждой пациентки (см. таблицу 3).
 |
| Таблица 3. Схема лечения урогенитальных расстройств. |
Такая система дифференцированной ЗГТ позволяет повысить качество жизни больных с урогенитальными расстройствами на 60—70%.
Таким образом, представленные данные позволяют говорить о ЗГТ как об основной терапии урогенитальных нарушений в постменопаузе.
В связи с прогрессирующим характером урогенитальных расстройств преимущество отдается профилактическому назначению ЗГТ и ее долговременному применению. ЗГТ урогенитальных расстройств должна назначаться длительно, практически пожизненно, и в этой ситуации на помощь приходит именно местная терапия эстриолом.
На сегодняшний день современная медицина располагает достаточно широким выбором хороших препаратов для ЗГТ и опытом их применения, свидетельствующим о том, что преимущества назначения ЗГТ заметно преобладают над риском развития побочных эффектов. Все это дает основание рекомендовать широкое применение ЗГТ для профилактики и лечения урогенитальных нарушений в пери- и постменопаузе с целью улучшения качества жизни и сохранения работоспособности женщин, вступающих в этот «осенний» период.
А. Л. Тихомиров, доктор медицинских наук, профессор
Ч. Г. Олейник, кандидат медицинских наук
МГМСУ, Москва
Лечение атрофического вагинита
Изменения слизистой оболочки влагалища, которые проявляются в виде истончения тканей, а также уменьшения концентрации гликогена и исчезновения лактобацилл. Процесс связан с возрастным дефицитом эстрогенов в постменопаузе. Лечение атрофического вагинита заключается в восполнении недостатка гормонов и восстановлении микрофлоры половых путей.
Бызова Татьяна Евгеньевна
Михальчук Диана Васильевна
Покшубина Светлана Дмитриевна
Заведующая отделением, акушер-гинеколог высшей квалификации, хирург-гинеколог
Ступина Светлана Вадимовна
Зарайская Зоя Петровна
Врач-гинеколог высшей квалификации
Причины атрофических изменений в постменопаузе
У женщин состав микрофлоры влагалища напрямую зависит от функции яичников. В них вырабатываются эстрогены, которые стимулируют накопление гликогена в клетках эпителия. Он постоянно обновляется, а слущенные клетки становятся питательной средой для лактобактерий. Здоровая микрофлора окисляет гликоген и выделяет молочную кислоту, перекись водорода и другие вещества, которые увлажняют слизистую оболочку. Благодаря кислой среде половые пути защищены от размножения патогенной флоры.
Постменопаузный атрофический вагинит формируется при недостатке эстрогенов. После 45 лет функция яичников начинает снижаться, в них прекращают созревать фолликулы, не вырабатывается нужная фракция гормонов. Поэтому с этого возраста могут появляться атрофические изменения в слизистой оболочке. Это первые симптомы приближающегося климакса.
Наиболее выраженные симптомы появляются в постменопаузу, или в период до 2 лет от последней самостоятельной менструации.
Но атрофический вагинит у женщин может появиться и до наступления менопаузы. Причинами этого могут быть:
Как проявляется вагинит?
Постменопаузальный атрофический вагинит развивается постепенно. Его первые симптомы могут появляться уже в 40 лет. Атрофия затрагивает не только слизистую оболочку влагалища, но и сосудистую стенку, связочный аппарат. Из-за недостатка эстрогенов, снижения кровотока, ткани не получают достаточного питания. Женщина может заметить, что во время полового акта появилась сухость. Со временем недостаток смазки делает интимные отношения болезненными, а после полового контакта могут появляться мажущие кровянистые выделения.
Сухость сохраняется постоянно, она дает ощущение стянутой кожи половых губ и преддверия влагалища, появляется нестерпимый зуд и жжение. Они могут усиливаться после полового акта или гигиенических процедур с мылом.
Нормальные бели исчезают, из-за гибели лактобактерий снижается защитная функция. Поэтому увеличивается риск заражения половыми инфекциями или обострения имеющихся хронических кольпитов. Постменструальный атрофический вагинит сопровождается смещением рН в щелочную сторону, поэтому у женщины развивается бактериальный вагиноз. Это невоспалительное изменение слизистой, при котором увеличивается концентрация анаэробной флоры. Беспокоят следующие симптомы:
Избавиться от признаков вагиноза можно, если провести лечение атрофического вагинита. Иначе признаки дисбактериоза будут прогрессировать.
Симптомы атрофических изменений при вагините сопровождаются дизурическими расстройствами. У женщины в постменопаузу появляется недержание мочи, которое проявляется при смехе и кашле, императивные позывы в туалет. Но если начать лечение основного заболевании, эти симптомы исчезают.
Постоянный зуд раздражает, усиливает стресс, ведет к развитию невроза. Одновременно из-за гормональных расстройств появляются нервно-психические расстройства, повышенная возбудимость, импульсивность, плаксивость.
Частота вагинита, вызванного атрофией, возрастает с возрастом. У женщин, которые вступили в фазу менопаузы 5-6 лет назад, болезнь развивается в 50% случаев. Те, у кого климакс начался 7-10 лет назад, сталкиваются с атрофией слизистой оболочки в 75% случаев.
Методы диагностики атрофического вагинита
Обследование при вагините в постменопаузу проводит врач-гинеколог. Начальным этапом обследования является сбор анамнеза. Женщина должна указать, с какого времени у нее появились признаки болезни. Если симптомы климакса выявлены раньше возрастной нормы, необходимо искать причины заболевания.
При осмотре на кресле врач отмечает истонченную слизистую оболочку влагалища, которая легко травмируется при касании инструментами. На ней могут быть заметны ссадины и мелкие трещины. Выделения при вагините могут отсутствовать, но после присоединения вагиноза отмечаются зловонные серые бели. Для уточнения состояния рН проводят нитрозаминовый тест. Для этого выделения смешивают с аммиаком на предметном стекле. При положительной реакции рыбный запах усиливается. Используются следующие методы диагностики вагинита:
Если признаки климакса появились раньше среднего возраста, проводят УЗИ малого таза, определяют гормональный профиль, исследуют щитовидную железу, а в некоторых случаях делают рентгенографию турецкого седла и КТ головного мозга.
Направления лечения вагинита
Чтобы уменьшить проявления вагинита, необходимо восполнить дефицит эстрогенов. Поэтому основное лечение постменопаузного вагинита проводится при помощи гормональных препаратов.
Женщинам с ранними симптомами климакса лечение начинают с комбинированных оральных контрацептивов. После 45 лет предпочтение отдают трехфазным препаратам. Но с 50 лет необходимо перейти на лекарственные средства, в состав которых входят натуральные эстрогены с гестагенами. Такое лечение называют заместительная гормональная терапия.
Для вагинита в постменопаузу предпочтительно использовать эстрогены одновременно с гестагенами. Это позволит избежать негативного влияния на матку и риска развития рака эндометрия. Но если у женщины была удалена матка вместе с яичниками, допускается лечение только эстрогенами.
Эстрадиол при вагините применяется в виде инъекций, депо-форм. В случаях, когда нет других признаков климакса, кроме сухости слизистой, не нужно системное применение гормонов. Пациенткам назначают свечи с гормонами или мази, крем, который втирают в кожу бедер или живота.
Использовать препараты эстрогенов постоянно нельзя. Врач назначает их по специальной схеме, когда в начале курса они используются ежедневно для насыщения организма, а затем переходят на поддерживающий режим лечения.
Негормональное лечение атрофического вагинита в постменопаузе применяется у женщин с противопоказаниями к терапии гормонами, а также, если с момента наступления климакса прошло больше 5-7 лет. Для этого применяют смягчающие и увлажняющие крема, проводят лечение антигистаминными препаратами, витаминными комплексами.
Женщинам при вагините рекомендуется специальная диета со сниженным количеством сахара, простых углеводов в виде выпечки, хлеба, макаронных изделий. Это необходимо, чтобы поддержать на нормальном уровне глюкозу крови и избежать ее повышения. Иначе гипергликемия усилит неприятные симптомы вагинита.
Гигиенические процедуры рекомендуют проводить без мыла, можно применять специальные гели для интимной гигиены, которые поддерживают рН на нормальном уровне.
Менопаузальная гормонотерапия (МГТ)

Почему же процент женщин, принимающих МГТ, остается невысоким?
Крупное американское исследование WHI (Women’s Health Initiative, 2002 г.) вызвало драматический период в судьбе менопаузальной гормонзаместительной терапии, что способствовало резкому сокращению МГТ в большинстве стран мира, появлению страхов и сомнений в отношении пользы и рисков.
Преждевременное завершение части исследования по менопаузальной гормонзаместительной терапии (МГТ) привлекло к себе всеобщее внимание. Как женщины, так и врачи чувствовали себя обманутыми, так как терапия, которая до этого считалась полезной для здоровья в долгосрочной перспективе, теперь оказалась опасной. Отличающийся от фактического изложения пресс-релиз предварительной работы прогремел в СМИ за неделю до того, как сама статья стала доступна для большинства читателей. Сообщалось, что исследование было остановлено в связи с повышенным риском развития рака молочной железы, связанным с заместительной гормональной терапией. На самом деле, в скорректированном анализе связь МГТ и рака молочной железы не была статистически значима!
Последующий углубленный анализ результатов WHI показал, что МГТ характеризуется благоприятным профилем пользы/риска у более молодых женщин, которые начинают терапию в близкие к менопаузе сроки. Эти результаты характеризовались сходным защитным воздействием терапии в отношении ИБС и снижения общей смертности, которые были продемонстрированы ранее в крупномасштабных наблюдательных исследованиях с участием относительно молодых женщин. После WHI широкое распространение получила так называемая временная гипотеза или гипотеза «окна терапевтических возможностей», согласно которой существует различное влияние МГТ на атеросклероз и связанные с ним клинические события в зависимости от возраста женщины и времени начала использования МГТ по отношению к моменту наступления менопаузы.
Основными недостатки данного исследования являлись:
Что же происходит с женским организмом в 45-55 лет?
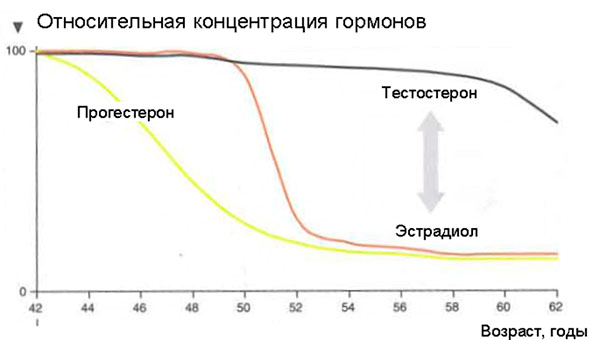
Что будет если МГТ не проводить?
А зачем нужно так «рисковать» и принимать «страшные» гормональные препараты при наступлении менопаузы? Ведь это естественный процесс, может, пусть все идет, как заведено природой? — Но тогда мы неизбежно столкнемся с заболеваниями, которые также предопределены природой.
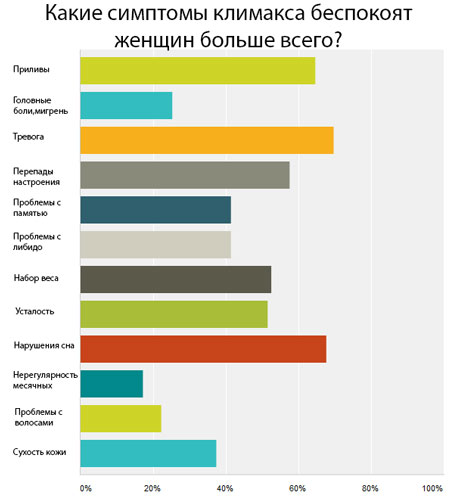
Сначала появляются ранние симптомы:
Через некоторое время появятся и поздние нарушения, связанные с длительным дефицитом половых гормонов:
Какое обследование проводится перед МГТ
Перед назначением менопаузальной гормональной терапии необходимо обследование (впрочем, которое необходимо проводить хотя бы раз в год и без терапии всем сознательным женщинам старше 45 лет).
Дополнительные обследования (при соответствующих данных анамнеза):
Когда пора начинать менопаузальную гормональную терапию?
Но проблема в том, что диапазон нормы ФСГ огромен, и для каждой женщины уровень свой. В идеале нужно сдать анализы крови на гормоны в период максимального расцвета – с 19 до 23 лет. Это и будет вашей индивидуальной идеальной нормой. А начиная с 45 лет ежегодно сверять с ней результаты. Но даже если вы впервые слышите о ФСГ – лучше поздно, чем никогда: в 30, 35, 40 лет имеет смысл выяснить свой гормональный статус, чтобы ближе к критическому возрасту было, на что ориентироваться.
Как самостоятельно понять, что пришло время МГТ?
Уровень эстрогенов снизился, если:
Препаратов огромное количество, какие из них наиболее безопасны?
Действует принцип «минимальности» и «натуральности»!
Для менопаузальной гормональной терапии применяются различные препараты, которые могут быть разделены на несколько групп:
«Натуральные» эстрогены – это препараты эстрогенов, которые по химической структуре идентичны эстрадиолу, синтезируемому в организме женщин. Благодаря современным технологиям создан синтетический эстрадиол, но по своей химической структуре он идентичен натуральному Эстрадиол–17b.
На сегодняшний день таким критериям более всего соответствует препарат Фемостон. Препараты линейки фемостона имеют различные дозировки, что укладывается в один из основных постулатов современной концепции МГТ – использование наименьшей возможной дозировки, которая сохраняет эффективность.
Препараты для двухфазной терапии – когда еще есть месячные
Фемостон 1/10 и Фемостон 2/10
В состав Фемостона 1/10 входят 28 таблеток. 14 белых, содержащих 1 мг Эстрадиола, и 14 серых, содержащих 1 мг Эстрадиола и 10 мг Дидрогестерона.
Состав Фемостона 2/10 отличается только количеством Эстрадиола
Препараты для монофазной терапии – когда месячные отсутствуют
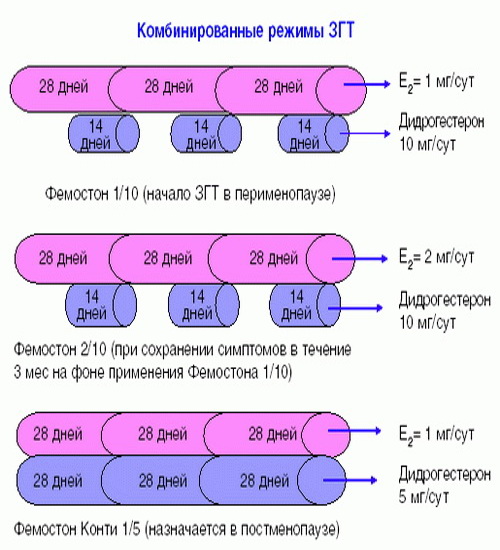
В состав Фемостона конти 1/5 входят 28 таблеток, содержащих 1 мг Эстрадиола и 5 мг Дидрогестерона.
В состав Фемостона мини 0,5/2,5 входят 28 таблеток, содержащих 0,5 мг Эстрадиола и 2,5 мг Дидрогестерона.
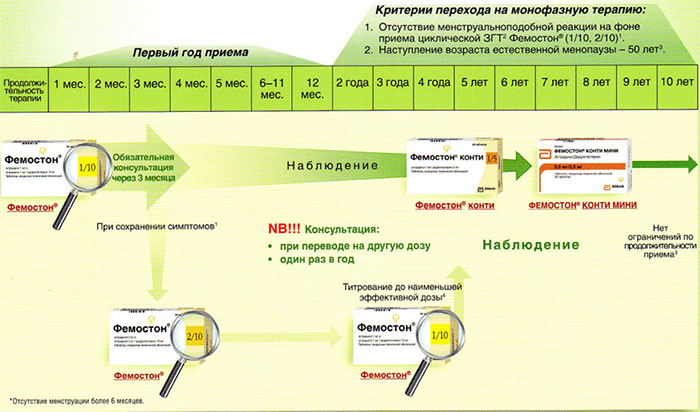
Ниже представлена более подробная схема первоначального назначения препаратов фемостон в пременопаузе (то есть до прекращения менструаций, но при наличии характерных климактерических симптомов). Пациенткам, у которых менструации не прекратились, рекомендуют начинать лечение в первый день менструального цикла. Пациенткам с нерегулярным менструальным циклом целесообразно начинать лечение после 10-14 дней монотерапии прогестагеном («химический кюретаж»).
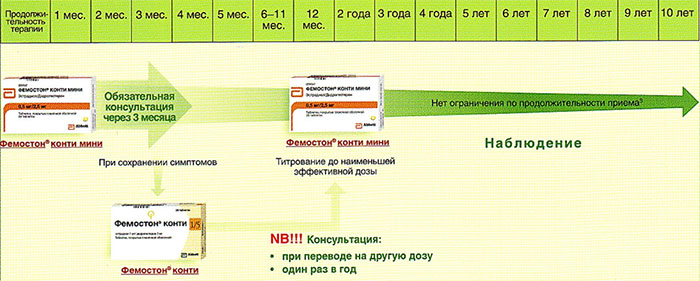
Далее Вашему вниманию представлен алгоритм первоначального назначения препарата фемостон в постменопаузе (то есть когда уже прошел год и более после последней менструации).
Какой способ применения препаратов лучше?
Трансдермальное (накожное) нанесение позволяет избежать первой стадии печеночного метаболизма, благодаря чему колебания концентрации эстрадиола в плазме крови при применении накожных препаратов незначительны. Метаболизм и выведение эстрадиола при трансдермальном введении подобен метаболизму натуральных эстрогенов.
Большинству пациентов желательно использовать оптимальную и наиболее безопасную на сегодняшний день схему: Дивигель накожно + Утрожестан интравагинально.

Схема приема для женщин, у которых сохранена менструальная функция, назначается врачом. Обычно средство прописывают циклом с первого дня после окончания менструации (5 день цикла) в течение 25 дней, после овуляции (c 16 по 25 день цикла) нужно добавлять препараты гестагенов.
Утрожестан – содержит прогестерон микронизированный, существует в двух формах — 100 и 200 мг.
При МГТ в постменопаузе в непрерывном режиме препарат Утрожестан применяется в дозе 100 мг с первого дня приема эстрогенов.
При болях в молочной железе можно добавить прожестожель ежедневно по 1 дозе на каждую молочную железу 2-4 недели.
Противопоказаниями для заместительной гормонотерапии являются:
Нужен ли женщинам тестостерон?
Согласно рекомендациям Международного общества по менопаузе (International Menopause Society (IMS)) основное показание для применения тестостерона – лечение уменьшенного сексуального влечения, которое заставляет данную женщину испытывать значительные страдания. До рассмотрения вопроса о проведении терапии тестостероном необходимо решить вопросы, связанные с другими причинами нарушенного сексуального желания и/или возбуждения. К ним относятся диспареуния, депрессия, побочные эффекты лекарственных препаратов, проблемы взаимоотношений и другие проблемы со здоровьем, влияющие на женщину или ее партнера.
В настоящее время возможно применение трансдермальных препартов. На отечественном фармацевтическом рынке существует только один вариант – Андрогель, но его применение у женщин является «off-label», то есть не разрешено инструкцией. Обычно назначается 1/5 пакета в день (то есть 1 г геля/10 мг тестостерона).
Еще более перспективным может стать интравагинальная форма тестостерона, которая также может оказывать благоприятное действие при лечении вульвовагинальной атрофии.
Ключевые положения по применению препаратов тестостерона
Самые частые заблуждения:
А как же рак молочной железы, ведь это самая главная причина смерти у женщин?
В этом утверждении много заблуждений. На самом деле рак молочной железы – причина смертности в 4% случаев. Ведущая причина преждевременной смерти – сердечно-сосудистые заболевания (50%), которые запускает инсулинорезистентность. А она возникает на фоне гормональных нарушений.
Гормоны вызывают побочные эффекты и от них толстеют?
Новые низкодозированные и высокоселективные препараты направлены четко на мишень. Врачи на протяжении многих лет наблюдали за тысячами женщин, которые получали МГТ? Сегодня уже есть уникальные гестагены, метаболически нейтральные, они не приводят к ожирению и вместе с тем не понижают тестостерон, если у женщины нет его избытка. Выработаны и новые схемы лечения. Иногда при применении таблеток с эстрогенами, где-то в 10% случаев, бывают головные боли и боль в венах. В этом случае они заменяются на трансдермальные формы в виде геля.
Зачем мне принимать гормоны, если у меня нет приливов и отличное самочувствие?
Вместе с падением уровня гормонов возникает риск развития возрастных болезней: повышается артериальное давление, возникает ожирение, увеличивается риск развития сахарного диабета второго типа, подагры, остеопороза и онкологических заболеваний.
Вместо таблеток лучше принимать травы и различные фитоэстрогены?
Эффективность данных препаратов по устранению вазомоторных симптомов составляет 30%, что равно эффективности плацебо. При этом данная группа препаратов никаким образом не оказывает профилактического действия на возрастные заболевания (сердечно-сосудистые, онкологические заболевания, остеопороз, ожирение и сахарный диабет).