с какого дня начинается выработка антител при коронавирусе
Эпидемиолог рассказала, кому и когда сдавать анализы на антитела к коронавирусу
Для того, чтобы узнать, сформировался ли иммунитет к коронавирусу, медики рекомендуют сдать анализы на выявление антител. Причем не качественно – такой тест даст ответ о том, есть ли антитела или нет, а количественно – этот анализ покажет титр антител. Об этом рассказала главный эпидемиолог МБУ ЦГБ № 2 Светлана Климина.
Иммуноглобулины М (IgM) начинают формироваться и выделять с 7 дня после заражения коронавирусом. При этом исследование мазка методом ПЦР может быть не всегда информативно, многое зависит от того, сколько времени прошло с момента заражения, от техники взятия биоматериала (например, когда наборы для забора проб доставляют на дом, и люди сами делают мазок), в итоге могут быть отрицательные результаты, хотя человек переносит инфекцию на самом деле. Положительный анализ IgM будет подтверждением острого инфекционного процесса.
Иммуноглобулины G (IgG) начинают вырабатываться с 10 дня после начала болезни. С течением времени они будут нарастать, то есть сдавать этот анализ можно на 10-14 день после заражения. Наличие IgG не говорит о стойкости иммунитета или нет, а лишь о том, что выработались защитные антитела.
По словам эпидемиолога, IgG имеет смысл сдать с разницей в 1-2 недели, чтобы проанализировать, как будет нарастать титр антител. Это будет показателем того, как формируется иммунитет. Впрочем, гарантии, что он сохранится на протяжении какого-то длительного времени, никто не даст, и единственный вариант – сдавать тесты повторно, например, спустя несколько месяцев, чтобы посмотреть, насколько снизились титры или же сохранились на том же уровне.
Врачи призывают не забывать о необходимости противоэпидемиологических мер — социальной дистанции и ношения масок.
Из какого теста: зачем проверять антитела и как делать это правильно
Для чего сдают тесты на антитела?
Тесты выполняются на наличие антител (иммуноглобулинов) IgA, IgM и IgG.
— Антитела IgG начинают вырабатываться примерно через 10-14 дней после появления симптомов. Их появление указывает на то, что у человека сформировался долговременный иммунитет. То есть речь идет либо о поздней фазе заболевания, когда больной уже выздоравливает, либо о том, что человек переболел COVID-19 раньше.
Какой тест можно сделать перед прививкой?
Сейчас тесты на антитела IgG чаще всего выполняют люди, которые собираются пройти вакцинацию, чтобы убедиться, что они не перенесли COVID-19 раньше бессимптомно и у них нет иммунитета, полученного естественным путем. Если тест показывает положительный титр антител IgG, вакцинацию можно отложить.
А если человек хочет проверить уровень антител после прививки? Сейчас многие сравнивают свои показатели.
Надо понимать, что тесты, которые используют в лабораториях, разные и шкалы у них используются тоже разные. Поэтому если пытаться сравнивать результаты (хотя большого смысла в этом нет), то надо по меньшей мере быть уверенным, что вы выполняли тестирование одним и тем же тестом.
Что такое «коэффициент позитивности»?
При этом еще раз отмечу, что у других производителей тестов шкала может быть другой и показатели, соответственно, тоже. При этом, получая результат теста в лаборатории, вы всегда можете увидеть на бланке референсные значения и сравнить результат с ними.
Каким тестом можно проверить поствакцинальный иммунитет?
Такой тест называется «Количественное определение антител к RBD домену S1 белка коронавируса (антитела IgG)» (выполняется методом хемилюминесцентного иммуноанализа сыворотки и плазмы крови, Abbot).
Это количественный анализ на IgG-антитела. Он поможет оценить иммунный ответ и в случае заражения (или перенесенного COVID-19), и для контроля поствакцинального иммунитета.
Когда делать:
— на текущую или перенесенную инфекцию не ранее чем через три недели после появления симптомов или получения положительного результата ПЦР-теста;
— для оценки поствакцинального иммунитета через три недели после второй дозы вакцины.
О чем говорят результаты:
Для чего нужно сдавать ПЦР-тест на COVID-19?
Этот тест сдается, чтобы проверить, болен ли человек или, возможно, является носителем вируса (даже если у него нет никаких симптомов нездоровья), выделяет ли он в настоящий момент вирус из верхних дыхательных путей, то есть является источником инфекции для окружающих.
Это единственный и ставший уже стандартным тест для туристов: при въезде практически все страны требуют предъявить справку о тесте, сданном перед отъездом. После возвращения из поездки тест придется сдать еще дважды и результат загрузить на портал госуслуг.
Кроме того, можно сдать ПЦР-тест, чтобы убедиться, что вы здоровы, то есть исключить бессимптомное течение заболевания. Это может понадобиться, если, например, вам предстоит встреча с пожилыми родственниками и вы не хотите рисковать их здоровьем. Кроме того, с помощью такого тестирования можно проверить, не заразились ли вы коронавирусом, если вы точно знаете, что контактировали с заболевшим.
Как правильно сдавать тесты?
Для теста ПЦР: берется мазок биоматериала со слизистой носоглотки. Анализ сдается натощак либо через три часа (или позже) после еды. За три часа до взятия мазка нельзя чистить зубы, полоскать рот, пить, жевать жевательную резинку, применять антисептические таблетки, полоскания и спреи.
Для теста на антитела: берется кровь из вены. Сдавать кровь нужно натощак утром или днем не менее чем через четыре часа после последнего приема пищи.
Можно ли заболеть после прививки и сколько работают антитела: ответы на главные вопросы о COVID-19
Можно ли заболеть ковидом, если сделал прививку, как долго защищают антитела и как часто нужно ревакцинироваться, чем опасен индийский штамм и стоит ли ждать западные вакцины — на главные вопросы о коронавирусе отвечает молекулярный биолог Ирина Якутенко
Можно ли заболеть, если привился
Говоря о защитном эффекте вакцинации, люди часто путают заражение и заболевание. Ни одна вакцина не может защитить от заражения — попадания вируса на чувствительные ткани и его проникновения внутрь клеток. Прививка не создает вокруг человека силового поля, которое не пропускает вирусы, и, если вакцинированный встретится с больным ковидом, когда тот активно распространяет вокруг себя вирусные частицы, и достаточно долго пообщается с ним в помещении без маски и соблюдения дистанции, вирусные частицы неизбежно попадут на слизистые.
Но когда мы говорим о заболевании, то есть о проявлении типичных симптомов, это означает, что вирус размножился в достаточном количестве, чтобы, во-первых, вызвать масштабную реакцию иммунной системы, а во-вторых, начать вредить организму самостоятельно. И тут эффект различных вакцин оказывается очень разным — кроме того, вероятность заболеть, несмотря на прививку, зависит от ситуации с вирусом в стране и, в частности, от количества вакцинированных.
В случае с коронавирусом мРНК-вакцины дают лучшую защиту от новых высокозаразных штаммов — причем речь как о заражении, так и о заболевании. В недавно вышедшем препринте ученые из Англии, проанализировав 14 000 случаев диагностированной инфекции дельта-штаммом (он же индийский, он же В.1.617.2), подсчитали эффективность мРНК-вакцины от Pfizer/BioNTech и векторной вакцины от AstraZeneca в отношении этой вирусной разновидности и сравнили с данными по альфа-штамму (он же британский, он же B 1.1.7). Через две недели после введения второй дозы мРНК-препарата эффективность против проявления симптомов ковида составила 88% для дельта-штамма и 94% для альфа-штамма. После векторной вакцины эффективность составила 67% для дельта-штамма и 74% для альфа-штамма. В отношении попадания в больницу, то есть тяжелых симптомов, две дозы мРНК-вакцины эффективны на 96% для дельта и 95% для альфа-штамма, эффективность двух доз векторной вакцины составила 92% для дельта и 86% для альфа-штамма.
Иными словами, мРНК-вакцины лучше защищают от симптомов, особенно от тяжелых, но и векторные препараты дают защиту намного больше той, на которую большинство экспертов рассчитывали в начале эпидемии, когда создание вакцин только началось. То есть дельта-штамм с не очень большой вероятностью может заражать привитых, однако болезнь у них в подавляющем большинстве случаев будет протекать в легкой форме.
Надо ли перепрививаться и когда
Учитывая, что в России привито около 10% населения, вопрос о ревакцинации не является ни основным, ни критическим. Тем не менее мэр Москвы Собянин заявил, что перепривился спустя год после первой вакцинации (видимо, он получил вакцину одновременно с сотрудниками НИЦ Гамалеи, которые опробовали на себе будущий «Спутник» еще до начала официальных клинических исследований), а глава столичного депздрава Алексей Хрипун заявил, что повторную прививку необходимо делать спустя полгода, и обещал, что процедура будет разработана в ближайшее время. Чиновник уточнил, что «уровень антител никакого значения не имеет, он через шесть месяцев такой, который как раз требует ревакцинации».
Когда антитела перестают работать
Никаких исследований, которые бы показывали, какой уровень антител считается опасно низким, не существует. Как нет и единого стандарта измерений антител: разные лаборатории используют тест-системы различных производителей, и не создано никаких сводных таблиц, по которым можно было бы пересчитывать значение, полученное в одной лаборатории, для другой.
Чтобы понять, когда защитный эффект от вакцинации начинает ослабевать, производители продолжают следить за добровольцами, получившими препарат или плацебо в рамках третьей фазы клинических испытаний. Сравнивая количество заболевших в обеих группах, разработчики оценивают эффективность вакцин в долгосрочной перспективе. Для мРНК-вакцины от Pfizer/BioNTech эффективность по предотвращению симптомного заболевания спустя шесть месяцев составила 91,2% — не существенно меньше эффективности вскоре после введения второй дозы.
В исследованиях вакцины от компании Moderna показано, что спустя полгода уровень нейтрализующих (самых эффективных) антител у привитых добровольцев немного снизился, но уровень защиты в этой работе не определялся. Для других вакцин подобных данных пока не публиковалось.
Сколько действует вакцина
Ответ на этот вопрос совпадает с ответом на предыдущий. Массовая вакцинная кампания началась зимой 2020-го — весной 2021 года, и по крайней мере для мРНК-вакцины за этот период защитный эффект, видимо, не сильно упал. Тем не менее большинство экспертов полагают, что ревакцинация в том или ином виде понадобится, так как коронавирус, похоже, уже не уйдет из популяции, а вакцины вряд ли дадут пожизненный иммунитет.
Генеральный директор Pfizer Альберт Бурла оценил вероятный срок, когда привитым может понадобиться бустер (усиливающая прививка), в 8-12 месяцев.
Не опасно ли перепрививаться слишком часто
Понятие «слишком часто» в отношении вакцин лишено научного смысла. Необходимый интервал ревакцинации устанавливается по итогам наблюдения за заражениями среди привитых и оценки уровня антител, для разных заболеваний и вакцин он разный.
Более того, необходимость ревакцинации определяется эпидемиологической ситуацией и условиями, в которых живет человек. Скажем, людям из неблагополучных по энцефалиту районов рекомендуется делать бустерные прививки, а тем, кто лишь приезжал туда, а основную часть времени живет в регионах, где этой болезни нет, ревакцинация не показана.
В нескольких исследованиях ученые сравнивали количество заболеваний, не предотвращаемых вакцинами, у привитых и непривитых детей. Авторы обнаружили, что никакой разницы нет, то есть дети, получившие множество разных вакцин, столь же эффективно справляются с постоянно окружающими нас патогенами, как и дети, чей иммунитет не «отвлекался» на выработку защитных инструментов против тяжелых болезней.
Надо ли прививаться, если переболел ковидом и выработались антитела
Как уже упоминалось выше, сегодня ученые не знают, каким должен быть минимальный уровень антител, который обеспечивает приемлемую защиту от заболевания. Поэтому регуляторы в сфере здравоохранения разных стран просто рекомендуют переболевшим прививаться — либо не указывая сроков, как, например, американский CDC, либо советуют подождать 28 дней с момента начала симптомов, как британский NHS.
Сама по себе рекомендация обязательно прививаться связана с тем, что после болезни иммунный ответ очень отличается у разных людей. Обычно чем тяжелее протекало заболевание, тем выше как общий уровень антител, так и количество нейтрализующих. Вакцинация же дает намного более стабильный уровень антител, кроме того, после нее не образуются неэффективные антитела, нацеленные на другие белки коронавируса, которые неизбежно формируются после болезни.
Чем опасен индийский штамм, в чем его специфика
Индийский штамм сочетает в себе сразу два неприятных свойства: высокую скорость распространения и способность частично уходить из-под действия антител. По имеющимся оценкам, он распространяется в 1,5 раза быстрее предыдущего рекордсмена — британского штамма. Какие именно мутации дельта-штамма делают его таким — пока неясно, но как минимум одно изменение — L452R — увеличивает способность вируса связываться с клеточными рецепторами ACE2, а это необходимый шаг для проникновения в клетку. Впрочем, аналогичная мутация есть и у других коронавирусных вариантов, например калифорнийского, так что, скорее всего, новые способности дельта-штамма — результат взаимодействия нескольких мутаций.
Главный научный сотрудник ВОЗ Сумия Сваминатан заявила, что индийский штамм становится доминирующим по всему миру, вытесняя остальные варианты. Это очень опасно, так как штаммы, которые легче распространяются, в итоге приводят к большему количеству смертей, чем более патогенные, но медленные варианты, из-за того, что за одинаковое время заражают больше людей.
Кроме того, из-за способности уходить от части антител, выработанных у тех, кто уже встречался с вирусными антигенами, индийский штамм может заражать вакцинированных и переболевших. Однако вероятность заражения ниже, чем для неиммунных.
Поможет ли вакцинация остановить третью волну в России, вызванную индийским штаммом
Единственным действенным способом быстро остановить коронавирусную волну является локдаун. Когда количество вновь инфицированных быстро увеличивается, это означает, что вирус прямо сейчас активно распространяется в популяции. Затормозить процесс можно, только разорвав как можно больше потенциальных цепочек заражения. Чтобы добиться этого, необходимо до минимума сократить количество возможных контактов.
В Европе третью волну, вызванную британским штаммом, удалось сбить многомесячными карантинами, во время которых были закрыты все магазины, за исключением самых основных, рестораны, кафе, клубы, фитнес-студии, салоны и так далее. Не работали детские сады, школьники и студенты занимались удаленно, а значительная часть взрослых работала из дома. Параллельно в европейских странах разворачивалась прививочная кампания, но первые месяцы рост числа вакцинированных не мог оказать заметного влияния на эпидемию, так как иммунизация начиналась с очень пожилых людей, которые мало контактируют с кем-то еще. Ограничения начали снимать только тогда, когда цифры новых случаев ковида приблизились к тем, что были до начала волны, а существенный процент населения получил хотя бы одну дозу вакцины.
Вакцинация без ограничения контактов или локдаун без массовой вакцинации гораздо менее эффективны. Видимый защитный эффект наступает спустя две-три недели после введения второй дозы, до этого риск привитых заболеть самим и заразить кого-то еще остается почти таким же, как у неиммунных. Кроме того, в отсутствии ограничительных мер вирус продолжает распространяться в популяции, что быстро приводит к перегрузу больниц. Локдаун сам по себе способен быстро загасить волну, но так как большинство людей остаются неиммунными, после его ослабления вирус вновь начинает распространяться.
«Спутник V» — по-прежнему самая эффективная российская вакцина?
Эффективность вакцин (как и других медицинских препаратов) определяется по итогам клинических испытаний — масштабных многоступенчатых исследований. На доклинической стадии разработчики проверяют эффективность и безопасность исследуемого вещества на животных и определяют допустимые концентрации. На первой фазе клинических исследований на небольшой выборке здоровых людей оценивают, прежде всего, безопасность, но иногда и какие-то параметры эффективности препарата. На второй стадии препарат дают уже большему количеству людей, представляющих разные группы здоровья. Наконец, на третьей стадии медикамент — в данном случае, вакцину — получают десятки тысяч людей.
Одновременно сравнимое количество людей получают плацебо, причем ни сами добровольцы, ни ученые не знают, кому что досталось. Людей выпускают «в поля» и через определенное время подсчитывают, сколько народу заразилось в обеих группах. Если в группе вакцины заражений и тяжелого течения заметно меньше (для вакцин от коронавируса ВОЗ выбрала отсечку эффективности в 50%), препарат считают работающим. Результаты клинических испытаний публикуют в международных рецензируемых журналах, чтобы научное сообщество могло независимо оценить их.
Из российских вакцин всем этим критериям удовлетворяет только одна вакцина — «Спутник V». По итогам его клинических испытаний были опубликованы две статьи в престижном журнале The Lancet, хотя результаты и методика проведения испытаний подвергались критике. Разработчики двух других российских вакцин не предоставили данных, которые можно было бы проанализировать незаинтересованным специалистам.
Правда ли, что вакцины от Pfizer/BioNTech и Moderna эффективней, и есть ли смысл их ждать
Сравнивать результаты клинических испытаний разных вакцин напрямую нельзя: они проводятся по разным протоколам, с разными критериями включения людей в испытания, в странах с разной эпидемиологической ситуацией и так далее. Тем не менее грубо сопоставить итоги испытаний можно, и такое сопоставление показывает, что в отношении предыдущих вариантов коронавируса мРНК-вакцины и векторный «Спутник» дают сходную эффективность. Однако, как мы уже обсуждали выше, мРНК-вакцины более устойчивы к дельта-штамму. Прямых данных о том, насколько хорошо этот вариант «пробивает» защиту от «Спутника», нет, но можно предположить, что его эффективность будет снижаться по похожему с векторной вакциной от AstraZeneca паттерну.
В России иностранные вакцины могут появиться только после того, как пройдут регистрацию в российских надзорных органах в сфере здравоохранения. Пока ни для одной западной вакцины такая процедура не начата. В ноябре компания «Петровакс» сообщила, что в российские надзорные органы подана заявка на регистрацию китайской вакцины CanSino. «Петровакс» в партнерстве с CanSino проводит в России испытания этой вакцины и в случае регистрации обещала быстро наладить производство китайского препарата. Однако процесс затянулся, и вакцина CanSino до сих пор не одобрена на территории России.
Эксперты ответили на самые частые вопросы о вакцинации от COVID-19
Как готовиться к прививке?
Специальной подготовки вакцинация не требует. Желательно сдать общий анализ крови и минимальный биохимический комплекс, чтобы не пропустить очаг «дремлющего» воспаления. Если человек здоров, соответственно, прием узких специалистов не нужен, советует врач-инфекционист, главный врач клинико-диагностической «Инвитро-Сибирь» Андрей Поздняков.
Недавно я болел ОРВИ (гриппом и т.д.), когда можно прививаться?
Когда можно сделать прививку ребенку и пожилым родителям?
Дети в настоящий период также исключены из вакцинации, так как испытаний на данной категории пациентов не проводилось. То есть ограничение по возрасту 18+ все-таки имеется. Верхнего порогового значения для пожилых людей нет. В начале вакцинации пациенты 65+ исключались, но затем минздрав разрешил внести изменения в инструкцию по применению вакцины. Сейчас вакцинируют и после 65 при отсутствии медицинских противопоказаний.
Нужно ли прививаться человеку, который уже переболел и имеет антитела к COVID-19?
В случае если у человека имеются антитела любого класса и в любом титре, вакцинацию проводить не рекомендуется, говорит Андрей Поздняков.
После прививки поднялась температура: я заразен?
Поскольку вирус SARS-CoV-2 был идентифицирован только год назад, пока нет данных о наблюдении иммунитета длительное время (более года). Поэтому сейчас невозможно сказать, как долго будет длиться иммунитет после болезни либо после вакцинации, отметила эксперт.
При каком уровне антител нужно делать прививку, а при каком можно подождать?
Можно ли купить импортную вакцину и сделать прививку самостоятельно?
Так что на сегодняшний день в России нет ни одной импортной вакцины в легальном обороте. Ни одна из зарубежных компаний (Pfizer, Moderna, AstraZeneca и другие) нам свои вакцины не поставляет.
Говорят, что вакцинация добровольна и бесплатна. Почему тогда в частной клинике предлагают заплатить 2 тысячи рублей?
Говорят, коронавирус мутирует. Это опасно?
Что касается сообщений о 18 мутациях вируса SARS-CoV-2, обнаруженных российскими учеными у пациентки, которая болела COVID-19 полгода, а также переполошившем весь мир «британском» штамме, по мнению ученого, пока нет оснований для особых страхов и тем более паники. Да, «британский» штамм более заразен и может вызвать увеличение численности заразившихся. Но самое главное, тяжесть течения заболевания не усилилась.
Поэтому соблюдение всем известных мер защиты поможет уберечься от вирусов-мутантов.
Что касается вопроса, защитит ли от мутировавшего вируса вакцинация, большинство экспертов считает, что да, защитит. У мутантов наблюдается изменение лишь ничтожно малой части генома, поэтому иммунная система, научившись с помощью вакцины распознавать коронавирус, будет реагировать и на его разновидности, поясняют вирусологи.
Зачем нужна вакцина «Спутник Лайт»?
Иммунный ответ на коронавирус SARS-CoV‑2 у больных COVID‑19
Академик Российской академии наук, д.м. н., президент
ФБГУ «НМИЦ ДГОИ им. Дмитрия Рогачева» Минздрава России
В статье представлен анализ результатов исследований иммунного ответа и памяти к SARS-CoV‑2, включая все ветви адаптивного иммунитета, иммуноглобулины, В-клетки памяти, CD8+- и CD4+-T-клетки у больных в динамике в течение 6–8 месяцев после начала заболевания.
Гуморальное звено
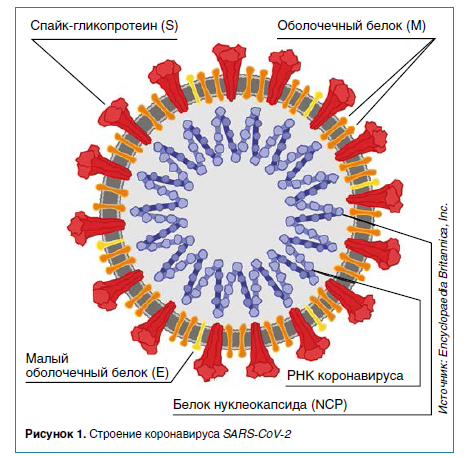
Факт первичного иммунного ответа слизистых на COVID‑19 необычен и требует объяснения. Обсуждаются две гипотезы.
Первая: вирусы контаминируют слизистые дыхательных путей и ЖКТ за 7–14 дней до появления системного ответа и клинических проявлений инфекции, поражая клетки микробиоты — используют их для репродукции вируса.
Вторая: кросс-реактивная продукция антител, предпосылкой которой являются Spike-реактивные CD4+-Т-клетки, обнаруженные у большинства пациентов с COVID‑19 и более чем у 34 % неинфицированных людей. Это подтверждает существование общих эпитопов эндемичных коронавирусов, вызывающих банальные ОРВИ и COVID‑19.
Важно, что изотипы иммуноглобулинов (либо IgG, либо IgA) конкурировали за нейтрализующую активность по отношению к SARS-CoV‑2 в зависимости от локализации. Сывороточные антитела IgG сильно коррелировали с величиной IgG-ответа и тяжестью заболевания. У пациентов, например, с IgA-назальным ответом определялась высокая активность нейтрализации вирусов. Инфекция у таких больных протекала бессимптомно.
Это, с одной стороны, предполагает возможность нейтрализации вируса с помощью IgA слизистых без системного ответа, что имеет отношение к исходам заболевания. А с другой стороны, из-за множества корреляций, наблюдаемых между типами антител и их активностью в разных анатомических участках, клиническая интерпретация гуморального ответа существенно затруднена.
Кроме того, эти данные имеют важное значение для нашего понимания защиты вакцинации, индуцирующей системный ответ на вакцинные гены или белки коронавируса по классическому пути и обеспечивающей иммунный ответ слизистых оболочек на 3–6‑й неделе после вакцинации. В идеале вакцина должна не только защитить реципиента от неизбежной болезни, но и предотвратить бессимптомное носительство, что закрыло бы проблему бессимптомных носителей в популяции.
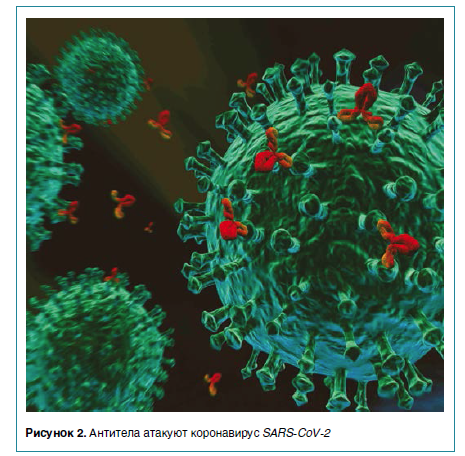
Титры Spike IgА и RBD IgА сохранялись на стабильном уровне на протяжении всего периода наблюдения t1/2— 210 дней, но у отдельных пациентов уровень специфических IgА-антител достоверно снижался через 90 дней.
Нельзя дать однозначный ответ в отношении серонегативных случаев COVID‑19. По-видимому, кроме протективного эффекта иммунитета слизистых, ответ напрямую связан с уровнем вирусной нагрузки SARS-CoV‑2. С одной стороны, высокие вирусные нагрузки связаны с более ранним ответом антител, в то время как у пациентов с низкой вирусной нагрузкой не может быть сероконверсии. С другой стороны, кинетика иммунного ответа может быть показателем скорости элиминации вируса у больного.
Идентификация специфичных В-клеток памяти к Spike, RBD и NCP с использованием флюоресцентно окрашенных зондов на IgD– и (или) CD27+ c последующей дифференцировкой по изотипам поверхностных IgM, IgG или IgA показала следующее. Количество специфических В-клеток увеличивалось в течение 120 дней после начала заболевания с последующим выходом на плато, в то время как Spike-специфические В-клетки памяти у людей, не заболевших COVID‑19, практически не встречались. RBD-специфические В-клетки появлялись на 16‑й день, и их количество увеличивалось в течение последующих 4–5 месяцев. Интересно, что только 10–30 % Spike-специфических В-клеток памяти было специфично для домена RBD через 6 месяцев после выздоровления больных.
NCP-специфичные В-клетки памяти также стабильно увеличивались в те же сроки и определялись спустя 5–6 месяцев после заболевания. Представленность изотипов иммуноглобулинов Spike-специфических В-клеток имела следующую динамику. В ранней фазе (20–60 дней) после заболевания IgM+ и IgG+ на В-клетках были представлены одинаково. В период после 60 дней до 240‑х суток преобладали IgG+ Spike-специфические В-клетки. Частота IgА+ Spike-специфических клеток составляла примерно 5 %, и они равномерно распределялись в течение всего периода наблюдения в 8 месяцев. Корреляция между сывороточным IgA и IgA слизистых оболочек не проводилась.
Сходная картина динамики наблюдалась и в случае IgG+, IgM+ и IgА+ к эпитопам RBD и NCP коронавируса. В то же время долгосрочное присутствие циркулирующих В-клеток памяти, направленных как против основных SARS-CoV‑2‑нейтрализующих таргетов (Spike и RBD), так и против не нейтрализующего таргета (NCP), свидетельствует о клеточной памяти, сохраняющейся после естественного воздействия вируса. Это может быть использовано для планирования ревакцинации. Тот факт, что почти все RBD- специфические IgG+-В-клетки памяти экспрессировали CD27, свидетельствует о долгосрочной иммунной памяти.
Анализ полученных данных говорит о том, что снижение нейтрализующих и других антител к SARS-CoV‑2 после клинического выздоровления вовсе мунитета. Просто с развитием и сохра- нением памяти В-клеток, способных активизироваться при встрече с новыми штаммами коронавируса, уровень антител в сыворотке снижается, в то время как IgА-ответ слизистых сохраняется на постоянном уровне в течении всего периода наблюдения.
Клеточный ответ
Процент больных с обнаруживаемыми циркулирующими CD8+-Т-клетками памяти через месяц после возникновения симптомов составил 70 %. К 6–9 месяцам клетки обнаруживались у 50 % выздоровевших пациентов. Фенотипические маркеры показали, что большинство SARS-CoV‑2‑специфичных CD8+-Т-клеток представлены терминально дифференцированными клетками памяти.
Циркулирующие SARS-CoV‑2‑специфичные CD4+-Т-клетки памяти через месяц после начала заболевания обнаруживались у 93 % пациентов. Через 6–9 месяцев уровень этих клеток был стабильным, а сами они выявлялись у более чем у 90 % пациентов, перенесших COVID‑19. Причем это касалось как Spike-специфичных, так и мембраноспецифичных CD4+-Т-клеток памяти.
Интересно, что при сравнении параметров иммунного ответа у больных с тяжелым и легким течением инфекции гуморальные показатели были более высокими у тяжелых больных, в то время как CD8+-Т-клетки были стабильными, а CD4+ — более низкими в тяжелых случаях заболевания. Объяснений этому феномену нет, важно, что слабый ответ Т-клеток наблюдается в острой фазе заболевания. Кроме того, важна и методология исследования клеточного им-мунитета.
Нарушения клеточного ответа проиллюстрированы дефицитом интерферонов I и II типов у пациентов с тяжелыми и среднетяжелыми формами COVID‑19 по сравнению с легкими и бессимптомными случаями заболевания. Это может быть связано с подавлением воспаления интерлейкином‑12 (IL‑12) и развитием вторичного дефекта клеточного иммунитета.
Иммунное взаимодействие
Большой интерес представляет изучение взаимодействия гуморального и клеточного ответа на SARS-Cov‑2. В исследованиях RBD-IgG, Spike IgА, RBD-В-клеток памяти, CD8+- и CD4+-Т-клеток в динамике у одних и тех же пациентов установлено, что у большинства из них (64 %) положительные показатели отмечались через 1–2 месяц после начала заболевания. Через 5–8 месяцев число реконвалесцентов, позитивных на пять тестов, снизилось до 43 %. В то же время как минимум три из пяти тестов были положительными спустя 6–9 месяцев. Важно отметить, что IgG на Spike дает на порядок больше положительных ответов, чем на RBD-антиген. Попытки связать гуморально- клеточные взаимодействия не привели к успеху из-за неоднородности участников исследования и методик оценки иммунного ответа.
Неопределенный результат
В метаанализе 22 исследований (4969 пациентов) установлены неблагоприятные признаки тяжелых форм болезни и летальных исходов, такие как лимфопения и нейтрофилез. Поскольку CD4+-Т-клетки необходимы для сбалансированного и эффективного иммунного ответа, неудивительно, что низкий уровень лимфоцитов может отражать гипервоспалительные процессы и способствовать более тяжелому течению заболевания и повышенной смертности.
Нейтрофилы как неотъемлемая часть врожденной защиты контролируют баланс микробиоты и элиминацию продуктов клеточной деструкции за счет производства активных форм кислорода и высвобождения нейтрофильных внеклеточных ловушек в венозном кровотоке. Лимфопения (менее 500 клеток в 1 мкл) указывает на повышение риска тяжелой формы заболевания и смертельных исходов при COVID‑19 в 3 раза. Стойкий нейтрофилез со сдвигом влево свидетельствует об истощении костномозгового резерва, а при сдвиге вправо отражает нарушения выхода клеток в ткани. Этот легко контролируемый анализом крови параметр указывает на более чем семикратное увеличение для пациента риска заболеть тяжело и погибнуть от COVID‑19.
Попытки выявить закономерности иммунного ответа на SARS-CoV‑2 оказались пока безуспешными.
Во-первых, можно сделать вывод, что переболевшие коронавирусной инфекцией сохраняют иммунную память в последующие 6–9 месяцев. Дальнейшие динамические исследования покажут, в какие сроки наступает снижение иммунного ответа, требующее профилактической вакцинации и (или) ревакцинации.
Во-вторых, и это очень интересно, каждый изученный компонент иммунного ответа и иммунной памяти демонстрирует различную кинетику. Это связано с индивидуальным ответом на инфекцию, наличием преморбида и частого превращения моноинфекции в смешанные инфекции SARS-CoV‑2 с активизировавшейся микробиотой больного.
В-третьих, неоднородность ответа может быть центральным признаком, характеризующим иммунную память к SARSCoV‑2. Биологические специфические IgG имеют 21 день периода полураспада, уровень антител с течением времени отражает продукцию короткоживущих, а потом и долгоживущих плазматических клеток. С точки зрения исчезновения возбудителя в течение нескольких дней после появления клиники, процесс наработки антител должен быть снижен к 6 месяцам, но, если SARS-CoV‑2 Spike и RBD IgG сохраняются дольше 8 месяцев, это означает, что вирус персистирует в организме хозяина или его микробиоте. Нельзя исключать и связь с пролонгированным иммунным ответом естественной реиммунизации циркулирующими эпидемическими альфа-коронавирусами, поддерживающими иммунный ответ.
В-четвертых, выявление и анализ SARSCoV‑2‑специфических В-клеток памяти потенциально могут применяться в качестве маркера гуморального ответа при вакцинации. Сейчас исследования поствакцинального иммунного ответа проводятся с использованием иммунофлуоресцентного анализа с оценкой IgM- и IgG-антител в качестве маркеров эффективности вакцины (рис. 3). Методы ИФА-диагностики, к сожалению, не стандартизованы едиными белками S, RBD, NCP, качество которых зависит от очистки антигена. Поскольку количество В-клеток памяти стабильно с течением времени, они могут представлять собой более надежный маркер продолжительности гуморальных иммунных реакций, чем иммуноглобулины сыворотки крови.
Таким образом, из результатов исследований иммунного ответа у больных COVID‑19 невозможно сделать какие-либо выводы о защитном иммунитете при новой коронавирусной инфекции. Ведь изучение антител и клеток памяти при этом заболевании пока еще не завершено. А значит, обсуждаемые механизмы защитного иммунитета против SARS-CoV‑2 у людей окончательно не определены.
Источник: Газета «Педиатрия сегодня» №6, 2021

