Тяжелый вариант течения ревматоидного артрита
Ревматоидный артрит (РА) считается одним из самых тяжелых хронических заболеваний человека. Заболевание характеризуется выраженным воспалением с пролиферацией синовиальной оболочки суставов, поражением внутренних органов и систем, мног

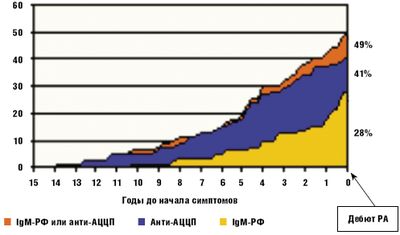
Течение РА весьма вариабельно. Это связано со многими причинами. Больной может оказаться резистентным к лечению, либо терапия оказывается не переносимой. Задержка с назначением терапии базисными противовоспалительными препаратами (БПВП) также ухудшает прогноз при РА. Кроме того, известно, что воспаление в синовиальной оболочке может начать развиваться задолго до появления первых клинических симптомов заболевания. Известно, что в крови больных РА за несколько лет до дебюта артрита (вплоть до 10 лет) выявляются серологические тесты, такие как ревматоидный фактор (РФ) и/или антитела к циклическому цитрулинированному пептиду (АЦЦП) [4] (рис. 1).
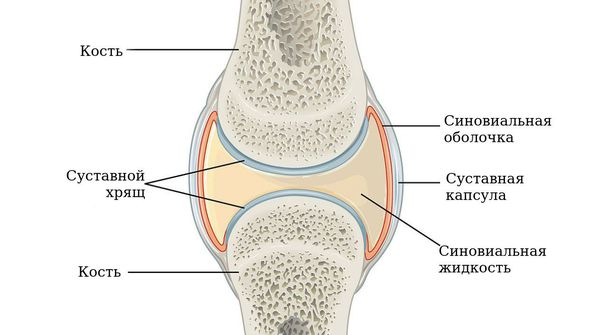
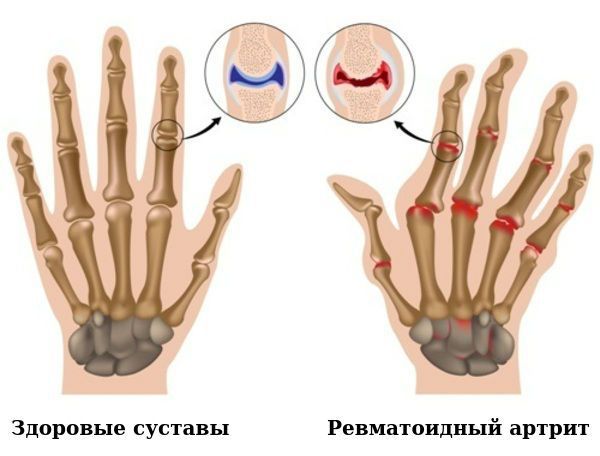
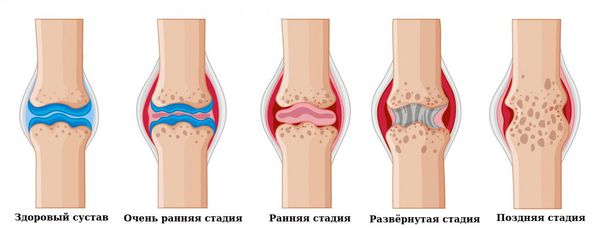
Морфологическое исследование синовиальной оболочки, полученной у больных в первые месяцы дебюта артрита, показало, что не у всех больных выявляются признаки острого ревматоидного воспаления, у части больных уже в первом биоптате отмечаются отчетливые признаки хронического синовита [5]. Именно у этих больных отмечался далее более торпидный вариант РА с плохим ответом на терапию БПВП. Тяжесть состояния больного РА на каждом этапе зависит от уровня воспалительной активности, что определяет выраженность болей в суставах, скованности, функциональных нарушений. При адекватно проводимой терапии и подавлении активности до развития необратимых анатомических изменений в суставах (деструкция, деформация) функция суставов восстанавливается (рис. 2). Тяжелый вариант течения болезни формируется при неадекватно проводимой или не эффективной терапии и определяется степенью стойкой утраты функциональной способности больного не только к профессиональному труду, но и к самообслуживанию. Поэтому как можно более раннее начало противовоспалительной терапии имеет при РА принципиальное значение.
В последнее десятилетие в практику ревматолога внедрены критерии раннего РА [6] для своевременного направления больного к ревматологу и раннего начала терапии. Идеальным должно считаться начало терапии БПВП сразу после появления первых симптомов воспаления в синовиальной оболочке: утренней скованности, боли в суставах и припухлости. На практике больной с дебютом РА проходит подчас длинный путь консультаций, диагностических мероприятий до встречи с ревматологом. Кроме того, начало болезни может быть клинически слабо выражено и симптомы болезни медленно нарастают, что затрудняет установление диагноза РА. По данным зарубежных авторов [7] и по нашим данным [8] при остром дебюте РА отдаленный исход болезни лучше, чем при постепенном начале заболевания. Вероятно, острое начало болезни заставляет пациента быстрее обращаться за врачебной помощью и позволяет врачу быстрее определиться с диагнозом и начать терапию. Наши данные свидетельствуют о лучшем исходе РА, оцененном через 15 лет болезни по степени сохранности функции опорно-двигательного аппарата, выраженности деструкции в суставах, частоте многолетних ремиссий и по выживаемости больных, при назначении БПВП в первые 6 месяцев от дебюта симптомов артрита [9]. Задержка с назначением БПВП приводит к более плохому ответу на эти препараты, что было показано в контролируемых исследованиях [10]. Препаратами первой линии считаются метотрексат и лефлуномид. Оба препарата способны подавлять активность и прогрессирование РА у большинства больных, особенно при назначении их в первые месяцы болезни. Но и начало терапии в очень ранний период болезни (1–2 месяца) не во всех случаях позволяет добиться выраженного эффекта (клинической ремиссии или поддержания субклинической активности РА). Во-первых, больной может не ответить на базисный препарат; во-вторых, у многих больных эффективность БПВП уменьшается через 1–2 года терапии, у части больных происходит последовательная смена базисных препаратов из-за симптомов непереносимости. При неэффективности и/или непереносимости последовательно назначаемых БПВП и формируется тяжелый вариант РА. Наиболее значимыми параметрами для определения тяжести РА являются выраженность деструктивных изменений в суставах и степень стойкой утраты функциональной способности суставов вплоть до утраты больным способности к самообслуживанию.
Большое количество рандомизированных клинических исследований (РКИ) было посвящено выявлению наиболее эффективных терапевтических стратегий в лечении больных РА: сравнивались результаты лечения при последовательной монотерапии БПВП, при их комбинации как в дебюте болезни (стратегия step-down), так и присоединение второго, третьего препаратов при неэффективности первого средства (стратегия step-up).
Оценка в сравнительном аспекте эффективности монотерапии метотрексатом, сульфасалазином, антималярийными препаратами, циклоспорином А, лефлуномидом и их комбинаций [11, 12, 13, 14, 15, 16, 17, 18] не показала однозначного преимущества комбинированной терапии БПВП перед их применением в виде монотерапии. В ряде исследований было показано, что через 6, 12 и 24 месяца клинический эффект был более выражен при использовании комбинации БПВП (либо при step-up, либо при step-down стратегии) [14, 16, 19, 20, 21, 22, 23], по данным других авторов [24, 25] не отмечено достоверных отличий во влиянии на показатели активности монотерапии или комбинации БПВП. При продлении срока исследований (до 5 лет) преимущества во влиянии на активность РА комбинации БПВП перед монотерапией не отмечено [11, 23, 24]. Оценка рентгенологических изменений в суставах через 1–2 года не показала преимуществ комбинированного лечения в исследовании MASCOT [16], а комбинация циклоспорина А и метотрексата в двух исследованиях через 6 [26] и 12 [27] месяцев в большей степени подавляла прогрессирование деструкции, чем монотерапия метотрексатом. В исследовании FIN-RACo изменение счета Ларсена было достоверно меньше при использовании комбинации БПВП через 2 года [14], но через 5 лет достоверных различий между комбинированной терапией и монотерапией уже не отмечалось [15].
Весьма интересны данные, полученные в результате исследования TICORA [12, 28], которое сравнило результаты 18-месячного лечения двух групп больных РА: в 1-й группе лечение проводилось со строгим ежемесячным контролем изменения активности РА по DAS (tight-контроль) и в соответствии с динамикой DAS корригировалась терапия («интенсивная» группа). Во 2-й группе лечение проводилось «рутинным способом» без такого жесткого контроля. К концу исследования ремиссия была достигнута у 65% больных 1-й группы и только у 16% больных 2-й группы. Увеличение числа эрозий было меньше в 1-й группе. Контролируемое лечение («интенсивная» группа) сопровождалась более частой коррекцией терапевтической тактики (использование комбинации БПВП, эскалация их дозы, использование внутрисуставных введений глюкокортикоидов). Авторы при анализе этих результатов пришли к выводу, что контроль за лечением обеспечивает наилучшие результаты вне зависимости от выбора БПВП. Такой же вывод сделан Albers J. M. и соавт. [29] при оценке результатов четырех различных режимов использования БПВП: жесткий контроль за успешностью лечения обеспечивает сходные результаты терапии различными БПВП. При оценке лечения метотрексатом пациентов с ранним РА (длительность болезни
Н. В. Чичасова, доктор медицинских наук, профессор Г. Р. Имаметдинова, кандидат медицинских наук Е. В. Иголкина С. А. Владимиров ММА им. И. М. Сеченова, Москва
Продолжительность жизни при ревматоидном артрите
Могут. Это так называемый серонегативный ревматоидный артрит.
Зачем и как часто надо делать общий и биохимический анализ крови?
Анализы крови выполняются для оценки активности ревматоидного артрита, а также позволяют выявить побочные эффекты проводимого лечения при их развитии. Если лечение базисными препаратами (метотрексатом, лефлуномидом, сульфасалазином, гидроксихлорохином) назначено впервые, анализы крови надо сделать в течение 2-3 недель, а далее ежемесячно в течение первых трех месяцев, затем 1 раз в 2 месяца в течение полугода и далее 1 раз в 3 месяца еще в течение 6-9 месяцев. Если терапия не меняется и нет признаков обострения болезни можно делать анализы крови 1 раз в 6 месяцев.
Лечение ревматоидного артрита Когда нужно начинать лечение ревматоидного артрита?
Лечение ревматоидного артрита необходимо начинать сразу же после установления диагноза, оптимально в первые 3 месяца от появления первых симптомов.
Кто назначает лечение ревматоидного артрита?
Лечение ревматоидного артрита назначается и контролируется ревматологом, который владеет полной информацией о болезни и ее рисках, методах оценки заболевания, терапевтической цели и возможных средствах ее достижения, разработке плана лечения и соотношении польза/риск для индивидуальной терапии.
Какова цель лечения ревматоидного артрита?
Лечение ревматоидного артрита направлено на достижение и поддержание ремиссии или низкой активности заболевания у каждого пациента.
Как часто нужно ходить к ревматологу, чтобы оценить эффективность лечения?
В первый год лечения требуется частый мониторинг (каждые 1-3 месяца). Ревматологом будет проведена коррекция лечения, если нет улучшения в течение 3 месяцев или цель лечения не достигнута через б месяцев после его начала.
Что такое базисная терапия?
Базисная терапия — основа медикаментозного лечения ревматоидного артрита. Она влияет на саму суть болезни, предотвращает прогрессирование заболевания и инвалидизацию. В настоящее время без применения базисных лекарственных средств лечение ревматоидного артрита невозможно.
Какие лекарственные средства используются для базисной терапии?
Золотым стандартом базисной терапии при ревматоидном артрите является метотрексат. При его непереносимости назначают лефлуномид, сульфасалазин, гидроксихлорохин. Это так называемые средства синтетической базисной терапии. Базисную терапию назначает и контролирует ревматолог.
На что надо обратить внимание при лечении базисными лекарственными средствами?
При назначении базисных лекарственных средств необходимо проводить клинический и лабораторный мониторинг каждого пациента для раннего выявления признаков реализации побочных эффектов проводимого лечения. Женщинам репродуктивного возраста на фоне приема базисных препаратов необходима контрацепция.
Что такое биологическая терапия?
Биологические лекарственные средства способны действовать избирательно на определенные компоненты воспалительного процесса. В большинстве случаев эти лекарственные средства представляют собой моноклональные антитела к провоспалительным цитокинам (веществам, вызывающим воспаление), таким какФНОа, интерлейкин-6.
Когда назначается биологическая терапия?
Показания к назначению биологической терапии определяет ревматолог, например, биологическая терапия назначается при недостаточной эффективности синтетической базисной терапии.
Какие лекарственные средства биологической терапии у нас есть? Как давно они применяются?
Биологические лекарственные средства начали применяться в ревматологии в 1998 году. С тех пор накоплен значительный опыт лечения данными препаратами. В настоящее время у нас зарегистрированы для лечения ревматоидного артрита: инфликсимаб, адали- мумаб, этанерцепт, ритуксимаб и тоцилизумаб. Эти лекарственные средства назначаются ревматологом и вводятся в специализированных отделениях, где врачи имеют соответствующий опыт.
Является ли биологическая терапия эффективной?
Биологическая терапия высоко эффективна. Большинство пациентов отмечают значительное улучшение самочувствия. Кроме сим- птом-модифицирующего действия, биологическая терапия обладает патогенетическим (базисным) действием, существенно улучшает прогноз заболевания.
Надо ли принимать метотрексат, если про-водится лечение биологическими лекар-ственными средствами?
Обычно синтетическая базисная терапия сохраняется. Чаще всего нет необходимости в приеме нестероидных противовоспалительных средств. Также на фоне биологической терапии вероятно снижение дозы глюкокортикоидов или их полная отмена.
При использовании тоцилизумаба допускается отказ от синтетических базисных препаратов (метотрексата, сульфасалазина и др.).
Какое значение имеют нестероидные про-тивовоспалительные средства в лечении ревматоидного артрита?
НПВС являются симптом-модифицирующими препаратами, они не влияют на процессы формирования и прогрессирования костно-хрящевой деструкции (разрушения кости и хряща). Их основное назначение — устранение субъективных болезненных ощущений, связанных с воспалением.
Как часто надо принимать нестероидные противовоспалительные средства и можно ли их вообще не использовать?
При ревматоидном артрите нестероидные противовоспалительные препараты (НПВС) принимают «по требованию», это значит, при болях. Чем реже пациент принимает эти лекарственные средства, тем меньше активность заболевания и, вероятно, базисная терапия подобрана верно. В случае постоянного болевого синдрома и необходимости принимать нестероидные противовоспалительные средства практически ежедневно необходимо обратиться к ревматологу для коррекции базисной терапии.
Как и для чего назначаются глюкокортикоиды?
Можно ли отменять гормоны самостоятельно при улучшении самочувствия?
Самостоятельно изменять дозировки глюкокортикоидов и режим приема препаратов нельзя. Действительно, при достижении эффекта, обычно начинают снижать дозу глюкокортикоидов, иногда до полной отмены. Но схему снижения должен предложить врач. Следует знать, что чем меньше доза и чем длительнее время приема глюкокортикоидов, тем медленнее необходимо снижать дозировку. Нельзя пропускать прием препарата.
Для чего вводить глюкокортикоиды в сустав?
Глюкокортикоиды могут вводиться внутрисуставно или периартикулярно (в ткани, окружающие сустав). Преимущество этой терапии состоит во введении препаратов непосредственно в очаг воспаления. Показанием для локальной терапии является необходимость быстро подавить активный воспалительный процесс в суставах в начале заболевания или при выраженном обострении.
Однако вводить глюкокортикоиды в один и тот же сустав можно не чаще 3 раз в год. Также не вводят препараты в сустав, в котором нет воспаления (отсутствует повышение температуры над суставом, припухлость). Если возникает потребность в более частых введениях глко- кортикоидов в сустав, необходимо пересмотреть базисную терапию. Необходимо помнить, что локальная терапия ни в коем случае не является эквивалентом базисного лечения, а назначается и проводится ревматологом в качестве дополнения к системной базисной и противовоспалительной терапии по строгим показаниям.
Какой диеты следует придерживаться при ревматоидном артрите?
Необходимо придерживаться сбалансированной диеты с включением в пищу полинена- сыщенных жирных кислот, фруктов и овощей, а также достаточного количества белка и кальция (мясо, рыба, молочные продукты). При ожирении надо придерживаться гипокалорий- ной диеты. Целесообразно отказаться от приема алкоголя и курения.
Полезно ли движение при ревматоидном артрите?
Движение в рамках повседневной жизни, лечебной физкультуры и активного досуга является залогом хорошего функционального прогноза, предотвращает анкилоз суставов, а также потерю мышечной и костной ткани.
Полезна ли физиотерапия при ревматоидном артрите?
Физиотерапевтические процедуры не влияют на прогрессирование болезни, а являются лишь дополнением к медикаментозному лечению. В период обострения заболевания физиотерапия не рекомендуется, а тепловые процедуры (озокерит, парафинолечение и др.) могут вызвать обострение ревматоидного артрита.
Совместима ли синтетическая базисная терапия с беременностью?
Планирование беременности при ревматоидном артрите должно согласовываться с ревматологом и гинекологом. Оптимально планировать беременность при достижении ремиссии или низкой активности заболевания. Зачатие возможно через 12 месяцев после отмены метотрексата, через 24 месяца после отмены лефлуномида. Допускается прием сульфасалазина до и во время беременности.
Совместима ли беременность с лечением биологическими препаратами?
Во время лечения и мужчинам, и женщинам необходимо соблюдать контрацепцию. Зачатие возможно через б месяцев после отмены биологической терапии.
Что такое ревматоидный артрит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Семизаровой И. В., ревматолога со стажем в 33 года.
Определение болезни. Причины заболевания
Ревматоидный артрит — это хроническое воспалительное заболевание соединительной ткани, которое характеризуется повреждением суставов и системным поражением внутренних органов.
Краткое содержание статьи — в видео:
Чаще всего заболевание поражает именно суставы, но может также затрагивать другие системы (лёгкие, сердце и нервную систему). Повреждение суставов происходит вследствие хронического воспаления синовиальной оболочки — внутреннего слоя, выстилающего суставную сумку.
По мере прогрессирования болезни происходит эрозия кости и деформация суставов. Заболевание имеет аутоиммунный характер, это означает, что в организме образуются антитела против собственных тканей. В результате длительного воздействия этих антител происходит разрушение и воспаление тканей.
Причины развития ревматоидного артрита неизвестны.
Предрасполагающие факторы:
Симптомы ревматоидного артрита
Дебют ревматоидного артрита может клинически проявляться различными вариантами:
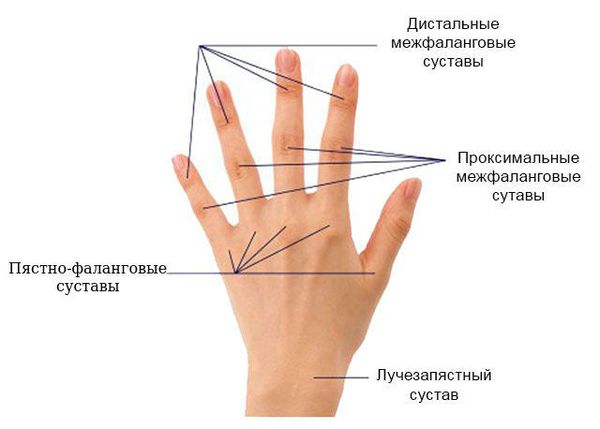
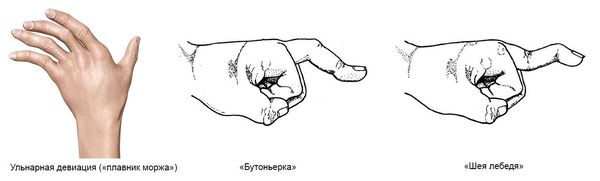
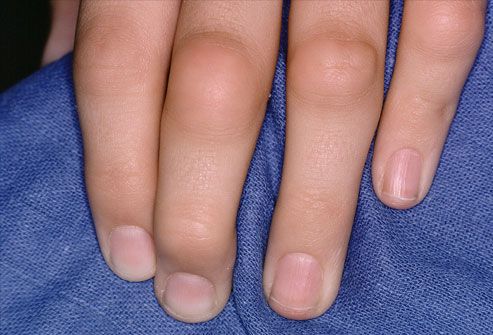
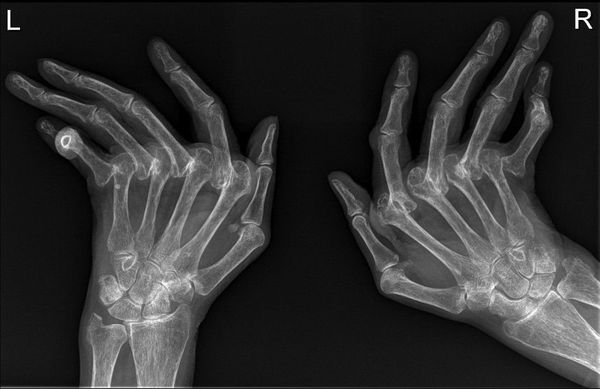
Для ранней стадии РА характерно поражение второго и третьего проксимальных межфаланговых и пястно-фаланговых суставов, а также положительный симптом сжатия кисти или стопы (при сжатии кисти или стопы возникает резкая боль) на уровне пястно-фаланговых и плюснефаланговых суставов. Типичным симптомом РА является веретенообразная дефигурация (изменение формы сустава, например в виде лебединой шеи или пуговичной петли) проксимальных межфланговых суставов кистей.
Одним из наиболее ранних и характерных симптомов является утренняя скованность (пациент не может согнуть и разогнуть суставы, как будто руки в тугих перчатках). Выраженность скованности чётко взаимосвязана с воспалительной активностью. При высокой активности воспалительного процесса она длится на протяжении многих часов, однако по утрам особенно выражена и всегда снижается после двигательной активности.
В развёрнутой и финальной стадиях заболевания появляются типичные для РА деструкции, деформации и анкилозы (заращение сустава, отсутствие движений в нём).
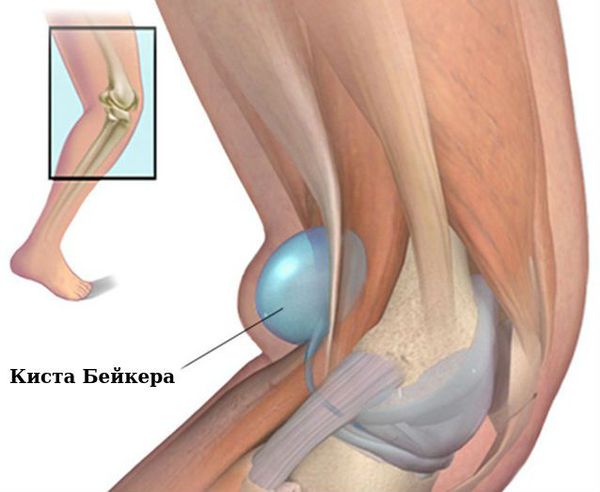
Коленные суставы: сгибательная и вальгусная (колени сводятся внутрь) деформация, киста Бейкера (подколенная или коленная киста).
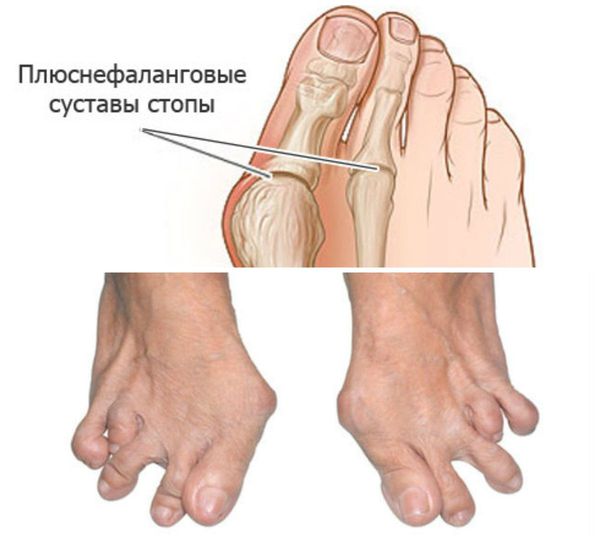
Стопы: подвывихи головок плюснефаланговых суставов, латеральная девиация (отклонение большого пальца к другим пальцам стопы), деформация большого пальца.
Шейный отдел позвоночника: подвывихи в области атлантоаксиального сустава, иногда осложняющиеся сдавлением спинного мозга или позвоночной артерии.
Перстневидно-черпаловидный сустав: огрубение голоса, одышка, дисфагия (пациент не может глотать), рецидивирующий бронхит.
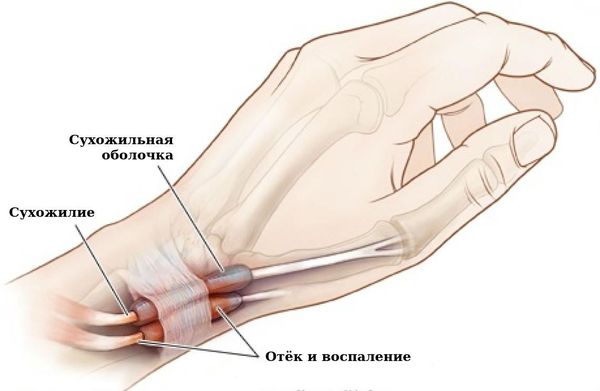
Связочный аппарат и синовиальные сумки: теносиновит (воспаление оболочек сухожилия) в области кисти и лучезапястного сустава; бурсит (воспаление в синовиальной сумке), чаще в области локтевого сустава; синовиальная киста на задней стороне коленного сустава (киста Бейкера).
Для РА характерны разнообразные внесуставные и системные проявления.
Конституциональные симптомы: генерализованная слабость, недомогание, похудение вплоть до истощения (вес меньше 40 кг), субфебрильная лихорадка.
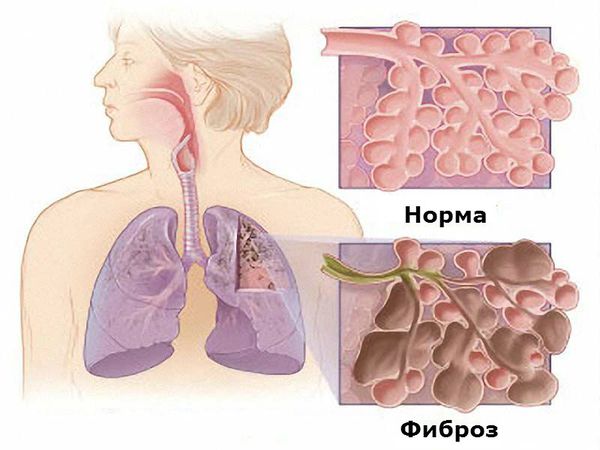
При РА нередко встречается поражение лёгких. Оно проявляется:
Кожный синдром имеет множество проявлений. Типичным внесуставным признаком являются ревматоидные узелки (костные образования на суставах размером с горошину или грецкий орех), которые располагаются под кожей чаще всего на разгибательной поверхности локтевых суставов, при атипичном расположении могут появляться на ахилловом сухожилии, роговице, в сухожилиях.
Кожными проявлениями ревматоидного артрита считают и развитие различных патологий:
Поражения периферической нервной системы объясняются сдавлением нервных стволов или их сосудистым поражением. Для ревматоидного артрита характерны компрессионные нейропатии: синдром запястного канала (длительная боль, онемение пальцев кисти), тарзального канала (боль в области голеностопного сустава, чувство ползания мурашек по руке) и т. д. Компрессия нервных стволов проявляется болями, чувством ползания мурашек, онемением, регионарной атрофией мышц. Возможно и поражение периферических нервов, которое проявляется чувствительными или чувствительно-двигательными нарушениями.
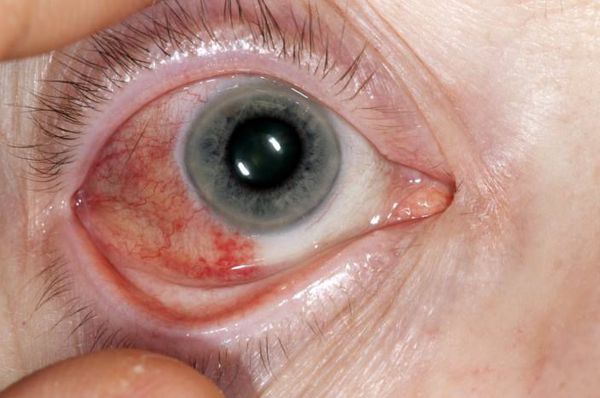
Патология глаз является одним из характерных проявлений ревматоидного артрита. Часто возникает эписклерит (воспаление тканей глаза), который очень редко сопровождается тяжёлым течением или исходом в перфорирующую склеромаляцию (размягчение ткани) с образованием отверстий в роговице и энуклеацией (удалением ядра).
При склерите (воспалении склеры глаза) и склерокератите (воспалении склеры и роговицы глаза) появляется выраженная боль и покраснение склеры. Характерен для этого заболевания и синдром сухого глаза, который является следствием скопления лимфоцитов в слёзных железах и обычно рассматривается в рамках синдрома Шегрена.
Патология почек проявляется диффузным гломерулонефритом (поражением клубочкового аппарата почек), распространённым амилоидозом (скоплением белка амилоида) с преимущественным поражением почек или лекарственной нефропатией (повреждением ткани и клубочкового аппарата почек). Последняя обусловлена приёмом нестероидных противовоспалительных средств (НПВС), например диклофенака, или комбинированных анальгетиков с фенацетином, что приводит к развитию интерстициального нефрита (воспаления в межуточной ткани почек).
Система крови реагирует на аутоиммунный воспалительный процесс развитием анемии, тромбоцитоза (увеличения содержания в крови тромбоцитов), нейтропении (снижения количества нейтрофилов). Возможны также вторичные, лекарственно обусловленные осложнения:
Поражение желудочно-кишечного тракта (ЖКТ) может быть представлено вторичным амилоидозом, аутоиммунным гепатитом, но наиболее часто выявляется эрозивное поражение вследствие приёма НПВС или глюкокортикостероидов.
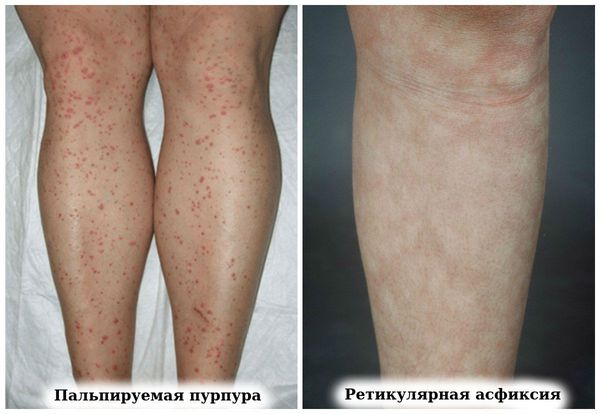
У пациентов с высокой активностью ревматоидного артрита может развиваться васкулит:
Эндокринные проявления — в связи с аутоиммунным характером заболевания одновременно могут развиваться аутоиммунный тиреоидит (хроническое заболевание щитовидной железы, при котором происходит постепенное разрушение клеток), синдром Шегрена.
Выделяют также редкие особые клинические формы течения ревматоидного артрита:
Синдром Фелти характеризуется таким симптомокомплексом: нейтропения, спленомегалия, гепатомегалия, тяжёлое поражение суставов, внесуставные проявления (васкулит, нейропатия, лёгочный фиброз, синдром Шегрена), гиперпигментация кожи нижних конечностей, высокий риск инфекционных осложнений. Этот синдром развивается у больных с длительным течением РА.
Патогенез ревматоидного артрита
В норме синовиальная оболочка имеет толщину всего несколько клеток, она вырабатывает синовиальную жидкость, которая смазывает и питает сустав. Механизм развития ревматоидного артрита можно представить следующим образом.
Классификация и стадии развития ревматоидного артрита
Классификация МКБ-Х
Рабочая классификация ревматоидного артрита (проект 2002)
Серопозитивный ревматоидный артрит (М 05).
Серонегативный ревматоидный артрит (М 06.0).
В течение длительного времени для установления достоверного диагноза РА использовались критерии 1987 года.
Пересмотренные диагностические критерии РА (ARA 1987):
Достоверный диагноз РА устанавливают при наличии четырёх из семи вышеперечисленных критериев, причём первые четыре должны существовать не менее шести недель.
Наличие 6 из 10 баллов указывает на определённый РА.
В 2007 году Ассоциации ревматологов России приняла новую классификацию РА, включающую несколько разделов.
Основной диагноз:
Клиническая стадия:
Активность болезни:
Внесуставные (системные) проявления:
Инструментальная характеристика:
Дополнительная иммунологическая характеристика — антитела к циклическому цитрулинированному пептиду (АЦЦП). Цитруллинированный пептид — это белок, который вырабатывается в результате обменных процессов в организме. В норме цитруллин полностью выводится из организма. При развитии РА концентрация ЦЦП повышается, иммунная система воспринимает его как чужеродный и начинает вырабатывать к нему антитела.
Функциональный класс:
Осложнения ревматоидного артрита
Диагностика ревматоидного артрита
Лабораторные исследования, рекомендуемые для обследования пациентов с подозрением на ревматоидный артрит [2] :
Ранняя диагностика подразумевает исследование уровня АЦЦП:
Инструментальные методы диагностики, рекомендуемые для обследования пациентов с подозрением на ревматоидный артрит:
Дифференциальный диагноз следует проводить со следующими заболеваниями: остеоартроз, системная красная волчанка, подагра, псориатический артрит, анкилозирующий спондилит, реактивный артрит, бактериальный эндокардит, септический артрит, вирусные артриты, системная склеродермия, идиопатические воспалительные миопатии, смешанное заболевание соединительной ткани, болезнь Лайма, амилоидоз, саркоидоз, рецидивирующий полихондрит, фибромиалгия.
Лечение ревматоидного артрита
Treat to Target (T2T) — лечение до достижения цели (рекомендации EULAR)
Общие рекомендации:
Медикаментозное лечение
Базисная терапия ревматоидного артрита
Метотрексат — один из основных препаратов терапии РА. Цитотоксический препарат из группы антиметаболитов. По структуре аналог фолиевой кислоты. Каждому пациенту с РА при отсутствии явных противопоказаний должна быть назначена терапия метотрексатом.
Метотрексат является препаратом выбора при активном ревматоидном артрите, как на ранней, так и в развёрнутой и поздней стадиях. Этот препарат обладает значительной терапевтической широтой и возможностью индивидуального подбора дозировок, эффективные дозы находятся в диапазоне 15-30 мг/нед, в среднем — 20 мг/нед.
Основные нежелательные явления: М-эрозивный стоматит, эрозивный гастрит, диспепсия, геморрагический энтероколит, гепатоцеллюлярный синдром, нефротоксичность, обструктивная мочекислая нефропатия.
Лефлуномид («Арава») — антивоспалительное, иммуномодулирующее, антипролиферативное действие. Специально был разработан для лечения РА.
Биологическая терапия РА
Введение ГИБП (генно-инженерных биологических препаратов) стало главным прорывом в лечении ревматических заболеваний. ГИПБ представляют собой искусственные антитела (белки из группы иммуноглобулинов). С появлением биологических препаратов появилась возможность достичь длительной и стойкой ремиссии у больных с ревматоидным артритом. В настоящее время ГИБП разделены на группы по их механизму действия:
Побочные эффекты. Биологические препараты помимо положительных свойств обладают и отрицательными:
Класс малых молекул
Симптоматическая терапия
НПВП — нестероидные противовоспалительные препараты. Их особенность — быстрое наступление терапевтического эффекта, активное подавление боли и воспаления (диклофенак, «Нимесил», «Найз», «Аркоксия» и др.)
ГКС — глюкокортикостероиды. Применяются в следующих случаях:
Локальная терапия ГКС — внутрисуставно и периартикулярно: бетаметазона дипропионат-дипроспан; триамцинолона ацетонид («Кеналог»); гидрокортизон ацетат.
Немедикаментозное лечение
Лечебная физкультура и трудотерапия (специальные упражнения, имитирующие движения в процессе самообслуживания, направленные на восстановление моторики) полезны больным РА.
Прогноз. Профилактика
Прогноз
Показатели смертности у больных РА увеличиваются: средняя продолжительность жизни снижается на 8-15 лет. Около 40 % пациентов в течение трёх лет становятся нетрудоспособными. Примерно у 80 % в течение 20 лет развивается нетрудоспособность средней и тяжёлой степени и в 25 % случаев требуется обширное протезирование суставов.
Факторы неблагоприятного прогноза: женский пол, положительный РФ, поражение плюснефаланговых суставов в начале заболевания.