pica chlorotica это что
Сидеропенический синдром
Сидеропенический синдром (синдром гипосидероза) обусловлен тканевым дефицитом железа, что приводит к снижению активности многих ферментов (цитохромоксидаза, пероксидаза, сукцинат-дегидрогеназа и др.). Сидеропенический синдром проявляется многочисленными симптомами:
• пристрастие к острой, соленой, кислой, пряной пище;
• выраженная мышечная слабость и утомляемость, атрофия мышц и снижение мышечной силы в связи с дефицитом миоглобина и ферментов тканевого дыхания;
• дистрофические изменения кожи и ее придатков (сухость, шелушение, склонность к быстрому образованию на коже трещин; тусклость, ломкость, выпадение, раннее поседение волос; истончение, ломкость, поперечная исчерченность, тусклость ногтей; симптом койлонихии — ложкообразная вогнутость ногтей);
• ангулярный стоматит — трещины, «заеды» в углах рта (встречаются у 10-15% больных);
• глоссит (у 10% больных) — характеризуется ощущением боли и распирания в области языка, покраснением его кончика, а в дальнейшем атрофией сосочков («лакированный» язык); часто наблюдается склонность к пародонтозу и кариесу;
• атрофические изменения слизистой оболочки желудочно-кишечного тракта — это проявляется сухостью слизистой оболочки пищевода и затруднениями, а иногда болями при глотании пищи, особенно сухой (сидеропеническая дисфагия или симптом Пламмера-Винсона); развитием атрофического гастрита и энтерита;
• симптом «синих склер» характеризуется синеватой окраской или выраженной голубизной склер. Это объясняется тем, что при дефиците железа нарушается гидроксилирование пролина и лизина, а затем синтез коллагена в склере, она истончается и через нее просвечивает сосудистая оболочка глаза.
• императивные позывы на мочеиспускание, невозможность удержать мочу при смехе, кашле, чихании, возможно даже ночное недержание мочи, что обусловлено слабостью сфинктеров мочевого пузыря;
• «Сидеропенический субфебрилитет» — характеризуется длительным повышением температуры до субфебрильных величин, происхождение этого симптома объяснить трудно; выраженная предрасположенность к острым респираторно-вирусным и другим инфекционно-воспалительным процессам, хронизации инфекций, что обусловлено нарушением фагоцитарной функции лейкоцитов и ослаблением системы иммунитета;
• снижение репаративных процессов в коже, слизистых оболочках.
Дата добавления: 2016-07-18 ; просмотров: 30388 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Извращение пищевых пристрастий (пикацизм, аллотриофагия) — это неконтролируемое пациентом желание поедать землю, глину, мел, древесину, пластмассу, тесто, сырое мясо, другие малосъедобные или несъедобные вещества и предметы. Расстройство выявляется при беременности, дефицитных состояниях, стрессе, психических болезнях. Для установления причины аллотриофагии рекомендованы лабораторные методы исследований, психологическое консультирование, осмотр психиатра. В лечении используют витаминно-минеральные препараты, седативные и психотропные средства.
Причины извращения пищевых пристрастий
Расстройство встречается у 1% взрослых, преимущественно женщин детородного возраста, у 10-15% детей и подростков. Чаще нарушением пристрастий к пище страдают жители экономически неразвитых регионов с низким социальным статусом. К извращениям пищевых предпочтений не относят случаи поедания несъедобных предметов детьми из любопытства, регулярное употребление малосъедобных веществ в экстремальных условиях и специфические традиции национальных кухонь.
Беременность
У взрослых женщин извращения вкусовых предпочтений чаще всего выявляются в гестационном периоде. Обычно сначала у беременной на фоне гормональной перестройки меняются пищевые привычки: она ощущает желание есть острую и солёную еду, сладости, смешивать между собой несовместимые продукты. По мере роста ребенка и активного потребления им основных питательных веществ у будущей матери формируются различные дефицитные состояния.
Именно недостаточное содержание в организме нужных микроэлементов вызывает у беременной стремление к поеданию земли, мела, мыла, льда, свежего теста, иногда — сырого мяса или рыбы. Особенность извращения пищевых пристрастий при гестации — сохранение женщиной сознательного контроля над поведением. Из-за боязни причинить вред ребёнку беременные воздерживаются от употребления потенциально опасных компонентов, несмотря на сильную тягу.
Дефицитные состояния
Частая причина расстройства — недостаточное поступление или усвоение организмом отдельных витаминов и микроэлементов. При дефицитных состояниях пищевые извращения сочетаются с другими признаками витаминно-минеральной недостаточности — общим недомоганием, специфическими изменениями кожи, снижением иммунитета, реже служат единственным симптомом заболевания. Тяга к несъедобным веществам встречается при таких патологиях, как:
Ранний (ювенильный) хлороз
Извращения пищевых привычек как один из ведущих признаков болезни появляются у девушек пубертатного возраста. Им предшествуют неспецифические симптомы в виде усталости, вялости, постоянной сонливости, сердцебиений, шума в ушах. По мере развития ювенильного хлороза проявляется pica chlorotica — неконтролируемая тяга есть землю. Симптому сопутствуют извращения обоняния, специфическая «алебастровая» бледность кожи, диспепсия, олиго- и аменорея.
Психологические причины
У взрослых нарушение вкусовых пристрастий может стать следствием острого и хронического стресса. Поеданию несъедобного способствует рост энергозатрат и расход питательных веществ, необходимых для поддержания стрессового метаболизма. Человек испытывает неукротимый голод, кроме обычной пищи начинает есть мел, зубную пасту, землю. У части больных развивается обсессивно-компульсивное расстройство с обкусыванием и поеданием волос, ногтей, кусочков кожи.
В детском возрасте ключевые причины извращения вкусовых привычек — недостаточное внимание родителей, буллинг со стороны сверстников, чрезмерные физические или интеллектуальные нагрузки, переезд семьи на новое место. Ребенок становится угрюмым, замкнутым, плаксивым или раздражительным. Чтобы успокоиться или привлечь внимание взрослых, такие дети начинают жевать и проглатывать бумагу, песок, камни, мел, мыло.
Психические расстройства
Вкусовые извращения у людей с нарушенной психикой свидетельствуют о тяжелом течении заболевания, плохом прогнозе, глубокой дезадаптации. Зачастую поедание несъедобных ингредиентов и предметов является стойким, постоянным и крайне сложно поддающимся коррекции. Нередко попытки окружающих воспрепятствовать нарушенному пищевому поведению вызывают агрессию со стороны больного. Распространенные психиатрические причины пикацизма:
Редкие причины
Диагностика
С учетом возраста первичным обследованием пациентов с выявленным изменением вкусовых пристрастий без признаков психических расстройств занимаются врачи-терапевты или педиатры. При наличии явной психопатологии диагностический поиск проводит психиатр. Для уточнения причины извращения пищевого поведения используют следующие методы обследования:
Лечение
Помощь до постановки диагноза
Беременным женщинам с легкой минеральной недостаточностью и незначительным изменением пищевых привычек достаточно откорректировать рацион. Рекомендуется есть продукты, содержащие железо, кальций, цинк, — мясо, творог, твёрдые сыры, пшеничные отруби, кедровые орехи. Обычно после родов у таких пациенток проявления пикацизма прекращаются самостоятельно.
До установления причины расстройства при стойком нарушении пристрастий к еде, особенно – поедании потенциально токсичных предметов и химических соединений важно обеспечить присмотр за больным и по возможности пресекать его попытки употреблять несъедобное. Если речь идёт о ребенке, следует максимально очистить пространство в доме от опасных компонентов. В любом случае необходимо срочно обратиться за врачебной помощью.
Консервативная терапия
Ведущим методом лечения пациентов, у которых извращения пищевых пристрастий связаны с психологическими проблемами и сверхценностями, является рациональная, поведенческая и семейная психотерапия. Больным с дефицитными состояниями, обусловленными целиакией, пожизненно назначается жесткая безглютеновая диета. При выборе препарата для медикаментозной коррекции учитывают причины, спровоцировавшие расстройство. В схему лечения могут включать:
Другие нарушения пищевого поведения
Извращение вкуса.
При извращении вкуса человек в течение долгого времени, месяца или больше, употребляет в пищу то, что несъедобно и способно вызвать серьезные проблемы со здоровьем, такие как отравление свинцом, анемия, повреждение зубов и других органов.
Извращение вкуса распространено среди людей, находящихся в сложном экономическом положении, среди людей с нарушениями развития, а также среди детей 2–6 лет и беременных женщин.
Извращение вкуса бывает трех основных видов:
При данном расстройстве больной может считать съедобными:
Причины извращения вкуса:
Последствия извращения вкуса:
Одним из успешных методов лечения является закрепление ассоциации данного отклонения с неприятными последствиями или наказанием (легкая терапия отвращением), после чего, если в пищу употребляются правильные вещества, предлагается позитивное подкрепление.
Прегорексия.
Прегорексия – расстройство пищевого поведения у беременных. Название образовано из слов “pregnancy” и “anorexia”. Прегорексия не является собственно заболеванием и встречается относительно редко. Она может проявиться во время беременности у женщин, которые очень боятся набрать вес и недостаточно кормят себя и развивающегося ребенка.
Сопровождаться отклонение может чрезмерными занятиями спортом во время беременности. У женщин с прегорексией в 0,2 % случаев на ранней стадии беременности отмечалась булимия и в 4,8 % случаев – компульсивное переедание. Все нарушения пищевого поведения во время беременности представляют опасность для матери и ребенка.
Дранкорексия.
Дранкорексия не является медицинским термином, скорее, это слово из разговорного лексикона. Это расстройство пищевого поведения, характеризующееся переходом человека на так называемую алкогольную диету, когда приём пищи заменяется приёмом алкоголя с целью преднамеренного снижения веса или контроля над ним. Часто сопровождается патологическим страхом набора веса и депрессией. Не является на данный момент официально признанным психическим расстройством.
Согласно публикации в «The Times of India», Виктория Осборн, профессор в сфере социальных проблем и здравоохранения, изучила связь между чрезмерным употреблением алкоголя и расстройством питания, включая ограничение калорий и «очистку», и пришла к заключению, что «16 % подростков ограничивают употребление калорий, чтобы «сохранить» место для выпивки. Среди девушек такой тип поведения встречается в три раза чаще, чем среди юношей, а основная мотивация — экономия денег на еде, чтобы остались средства на алкоголь».
Среди участников исследования данное поведенческое расстройство было присуще в большей степени женщинам, чем мужчинам. Особое распространение расстройство получило среди девушек-подростков. Основным мотивом для дранкорексии служит стремление не набрать лишний вес, быстрее опьянеть и сэкономить деньги, выделенные на еду, чтобы купить ещё спиртное. Около трети 18–23-летних женщин голодали для того, чтобы быть в состоянии употребить больше алкоголя.
В экстремальных случаях дранкорексия может быть связана с булимией или анорексией, когда алкоголь употребляется для того, чтобы вызвать рвоту или заглушить связанное с едой чувство беспокойства.
Неспецифическое нарушение пищевого поведения.
Бывает так, что у человека, который нормально ест и занимается спортом, присутствует зацикленность на питании, которая мешает ему в повседневной жизни. Причем, со стороны кажется, что никакого нарушения пищевого поведения нет. Это иногда принимают за «здоровый образ жизни».
Неспецифическое нарушение пищевого поведения включает в себя множество различных состояний. Часто речь идет о комбинации нескольких расстройств. Нарушения пищевого поведения выявляются все сложнее и их симптому нередко указывают одновременно на несколько различных состояний. Поэтому чаще всего диагностируется неспецифическое, т.е. невыясненное нарушение пищевого поведения. Но именно неспецифические нарушения заслуживают наибольшего внимания.
Ещё больше полезной информации и индивидуальные рекомендации вы сможете получить в поликлинике по месту жительства во время прохождения диспансеризации (или периодического медосмотра) или в ближайшем центре здоровья.
Pica chlorotica это что
Термин «пикацизм» происходит от латинского слова Pica — птица сорока. Традиционно (хотя неправильно) считается, что у этой птицы непомерный аппетит и она ворует и ест практически все. Пикацизмом, или извращенным аппетитом, в медицине называют тягу человека к поеданию глины, стирального крахмала, пепла, песка, кофейной гуши, раковин моллюсков, спичек, льда, газет, окурков и т. п..
Этот феномен встречается у половины пациентов, страдающих от недостаточности железа. Обычно люди с пикацизмом скрывают его от врача. Пероральный прием содержащих железо препаратов может привести к ремиссии извращенного аппетита. Особенно он распространен в Африке, Австралии (среди аборигенов) и на юге США.
Относительно причинно-следственной связи пикацизма с дефицитом в организме железа и цинка существуют разногласия. Некоторые факторы, предрасполагающие к извращенному аппетиту, приведены в таблице ниже. Особую разновидность пикацизма представляет тяга к необычной для данного индивида или нездоровой пище, например, во время беременности.
Факторы, предрасполагающие к извращенному аппетиту:
— Семейные неурядицы
— Неполноценное питание (включая недостаточность железа)
— Бедность
— Этнографические особенности
— Умственная отсталость
а) Пищевой пикацизм. Пищевой пикацизм — один из распространенных симптомов недостаточности железа. Пациент компульсивно ест определенный тип пищи, например сельдерей, хрустящий картофель, морковь, арахисовое масло, подсолнечное семя, петрушку, крекеры на соде, маринованные огурцы, шоколадное мороженое, латук, претцели, пьет апельсиновый сок, глотает жевательную резинку. Потребляемый продукт редко служит хорошим источником железа, но часто хрустит на зубах. Пищевой пикацизм может привести к летальному исходу.
б) Хартофагия. Хартофагия, т. е. тяга к поеданию бумаги, встречается не так уж редко, особенно у умственно отсталых, и может привести к непроходимости кишечника, его прободению и отравлению свинцом. Лощеная бумага покрыта слоем лака, обычно этил целлюлозного, и ее прием внутрь чреват образованием бумажного безоара.
Соединения ртути, вводимые в целлюлозную массу для производства бумаги в качестве противогрибковых агентов, могут вызвать ртутное отравление (например, при поедании пачек из-под сигарет или книг в мягкой обложке).
в) Геофагия. Геофагия — одна из форм пикацизма, выражающегося в потреблении земли и «напоминающих ее» продуктов. К последним относятся, например, крахмал, лед, засохшая краска, окурки и горелые спички. Геофагия широко распространена в животном мире и обычна среди приматов, включая шимпанзе. У человека ее считают как причиной, так и результатом особых типов алиментарного дефицита.
Геофагия как форма отклоняющегося поведения встречается по всеми миру, но особенно распространена в развивающихся странах, среди чернокожей бедноты, беременных женщин и детей, не будучи ограничена низшими слоями общества. Австралийские аборигены едят глину как средство от желудочного дискомфорта и диареи. Рентгенография брюшной полости может показывать у них соответствующие скоплениям почвы контрастные участки.
Дети женщин, потребляющих глину или крахмал, едят грязь, бумагу, отслоившуюся краску или штукатурку или вообще все, что попадет им в руки.
г) Лечение пикацизма. Геофагия или пагофагия (поедание льда) у некоторых пациентов быстро проходит после курса железотерапии. Парентеральное введение препаратов железа в ряде случаев устраняет пагофагию и пищевой пикацизм в течение 1 нед, а пероральный их прием — за 2 нед.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Железодефицитная анемия: современное состояние проблемы
В.Ю. Сельчук, С.С. Чистяков, Б.О. Толокнов, Л.В. Манзюк, мгмсу М.П. Никулин, Т.В. Юрьева, П.В. Кононец, Г.В. Титова
МГМСУ
Всасывание железа осуществляется преимущественно в двенадцатиперстной кишке и верхних отделах тощей кишки. Степень всасывания железа зависит от потребности организма в нем. При выраженном дефиците железа всасывание его может происходить и в остальных отделах тонкого кишечника. При уменьшении потребности организма в железе происходит снижение скорости поступления его в плазму крови и увеличивается отложение в энтероцитах в виде ферритина, который элиминируется при физиологическом слущивании эпителиальных клеток кишечника. В крови железо циркулирует в комплексе с плазменным трансферрином. Этот белок синтезируется преимущественно в печени. Трансферрин захватывает железо из энтероцитов, а также из депо в печени и селезенке и переносит его к рецепторам на эритрокариоцитах костного мозга. В норме трансферрин насыщен железом приблизительно на 30%. Комплекс трансферрин-железо взаимодействует со специфическими рецепторами на мембране эритрокариоцитов и ретикулоцитов костного мозга, после чего путем эндоцитоза проникает в клетки, и железо переносится в их митохондрии, где включается в протопорфирин и таким образом участвует в образовании гема. Освободившийся от железа трансферрин неоднократно участвует в переносе железа. Количество железа, которое расходуется на эритропоэз, составляет 25 мг/сут., что значительно превышает возможности всасывания железа в кишечнике. В связи с этим для гемопоэза постоянно используется железо, освобождающееся при распаде эритроцитов в селезенке. Хранение (депонирование) железа осуществляется в депо в составе белков ферритина и гемосидерина.
Хотя среди взрослого населения анемия чаще всего развивалась у женщин во время беременности, тем не менее в популяции основную долю пациентов с анемией составляли небеременные женщины репродуктивного возраста (468 млн человек). По крайней мере в половине случаев причиной анемии служит дефицит железа [WHO, 2001], который может быть следствием хронической кровопотери (менструации, оккультные кровотечения при опухолях желудочно-кишечного тракта (ЖКТ), неспецифические и специфические воспалительные заболевания тонкой и толстой кишки, другие причины), недостаточного поступления железа с пищей или нарушения его усвояемости (например, при хроническом алкоголизме), повышенной потребности (детский и подростковый возраст, беременность, послеродовый период), нарушения всасывания.
В соответствии с Международной классификацией болезней 10-го пересмотра (МКБ-10) учитывают следующие формы анемий, связанных с абсолютным и относительным дефицитом железа:
Классификация, клиника и диагностика ЖДА
Общепризнанной классификации ЖДА не существует. Имеются клиническая классификация ЖДА и классификация по стадиям и тяжести протекания анемии.
Клиническая классификация ЖДА:
ЖДА также классифицируют по стадиям и тяжести протекания.
По степени тяжести:
Анемический синдром обусловлен снижением содержания гемоглобина и уменьшением количества эритроцитов, недостаточным обеспечением тканей кислородом и представлен неспецифическими симптомами. Больные жалуются на общую слабость, повышенную утомляемость, снижение работоспособности, головокружение, шум в ушах, мелькание мушек перед глазами, сердцебиения, одышку при физической нагрузке, появление обморочных состояний. Может появляться снижение умственной работоспособности, ухудшение памяти, сонливость. Субъективные проявления анемического синдрома вначале беспокоят больных при физической нагрузке, а затем и в покое (по мере развития анемии).
Сидеропенический синдром (синдром гипосидероза) обусловлен тканевым дефицитом железа, что приводит к снижению активности многих ферментов (цитохромоксидаза, пероксидаза, сукцинат-дегидрогеназа и др.). Сидеропенический синдром проявляется многочисленными симптомами, такими как:
Лабораторные данные
Диагностика латентного дефицита железа
Латентный дефицит железа диагностируется на основании следующих признаков:
Диагностика ЖДА
При снижении содержания гемоглобинового железа появляются характерные для ЖДА изменения общего анализа крови:
Наиболее часто используемыми в практике критериями ЖДА являются:
— низкий цветовой показатель;
— гипохромия эритроцитов, микроцитоз;
— снижение уровня сывороточного железа;
— повышение ОЖСС;
— снижение содержания ферритина в сыворотке.
При биохимическом исследовании крови, кроме снижения уровня сывороточного железа и ферритина, выявляются также изменения, обусловленные основным онкологическим или другим заболеванием.
Лечение
В настоящее время существует следующие этапы лечения ЖДА:
Не так давно гемотрансфузия являлась одним из самых распространенных способов коррекции анемии даже легкой степени у больных после операционной кровопотери и кровопотери при других клинических ситуациях (роды, маточные кровотечения, геморрой, опухоли ЖКТ и др.). Считалось, что надо остановить кровотечение и перелить донорскую кровь или эритроцитную массу. Необходимое для переливания количество эритроцитов определяли исходя из объема кровопотери и уровня гемоглобина. Однако ориентация на достижение нормального уровня гемоглобина иногда приводила к переливанию значительных количеств (до 5-6 л) донорской крови, что сопровождалось развитием синдрома массивной трансфузии, рецидивом кровотечения, появлением признаков полиорганной недостаточности с высокой смертностью.
Лечебная программа при ЖДА включает:
При выявлении причины развития ЖДА основное лечение должно быть направлено на ее устранение (оперативное лечение опухоли желудка, кишечника, лечение энтерита, коррекция алиментарной недостаточности и др.). В целом ряде случаев радикальное устранение причины ЖДА не представляется возможным, например, при продолжающихся меноррагиях, наследственных геморрагических диатезах, проявляющихся носовыми кровотечениями, у беременных и в некоторых других ситуациях. В таких случаях основное значение приобретает патогенетическая терапия железосодержащими лекарственными препаратами.
Путь введения препарата больному ЖДА определяется конкретной клинической ситуацией. При проведении купирующей терапии применяются пероральное и парентеральное введение препаратов железа (ПЖ) больному.
Основными принципами лечения ПЖ для приема внутрь являются следующие:
— назначение ПЖ с достаточным содержанием трехвалентного железа;
— нецелесообразность одновременного назначения витаминов группы В (в том числе В12), фолиевой кислоты без специальных показаний;
— избегание назначения ПЖ внутрь при наличии признаков нарушения всасывания в кишечнике;
— достаточная продолжительность насыщающего курса терапии (не менее 3-5 мес.);
— необходимость проведения поддерживающей терапии ПЖ после нормализации показателей гемоглобина в соответствующих ситуациях.
Для адекватного прироста показателей гемоглобина у больных необходимо назначать от 100 до 300 мг трехвалентного железа в сутки. Применение более высоких доз не имеет смысла, поскольку всасывание железа при этом не увеличивается. Индивидуальные колебания в количестве необходимого железа обусловлены степенью его дефицита в организме, истощения запасов, скоростью эритропоэза, всасываемостью, переносимостью и некоторыми другими факторами. С учетом этого при выборе лекарственного ПЖ следует ориентироваться не только на содержание в нем общего количества, но и, главным образом, на количество трехвалентного железа, которое только и всасывается в кишечнике.
Причины неэффективности терапии ПЖ для приема внутрь:
— отсутствие дефицита железа (неправильная трактовка природы гипохромной анемии и ошибочное назначение ПЖ);
— недостаточная дозировка ПЖ (недоучет количества трехвалентного железа в препарате);
— недостаточная длительность лечения ПЖ;
— нарушение всасывания ПЖ, назначаемых внутрь больным с соответствующей патологией;
— одновременный прием препаратов, нарушающих всасывание железа;
— наличие хронических (оккультных) кровопотерь, чаще всего из органов ЖКТ;
— сочетание ЖДА с другими анемическими синдромами (В12-дефицитной, фолиеводефицитной).
— нарушение всасывания при патологии кишечника (энтериты, синдром недостаточности всасывания, резекция тонкого кишечника, резекция желудка по методу Бильрот II с выключением двенадцатиперстной кишки);
— обострение язвенной болезни желудка или двенадцатиперстной кишки;
— непереносимость ПЖ для приема внутрь, не позволяющая дальнейшее продолжение лечения;
— необходимость более быстрого насыщения организма железом, например, у больных ЖДА, которым предстоят оперативные вмешательства (миома матки, геморрой и др.).
В отличие от ПЖ для приема внутрь в инъекционных препаратах железо всегда находится в трехвалентной форме. Лечение больных с ЖДА имеет свои особенности в зависимости от конкретной клинической ситуации с учетом многих факторов, в том числе характера основного заболевания и сопутствующей патологии, возраста больных (дети, пожилые люди), выраженности анемического синдрома, дефицита железа, переносимости ПЖ и др. Общая ориентировочная доза ПЖ для внутримышечного введения, необходимая для коррекции дефицита железа и анемии, может быть рассчитана по формуле:
При парентеральном введении ПЖ возможны развитие флебитов, инфильтратов, потемнение кожи в местах инъекций, аллергических реакций, в том числе тяжелых (анафилактический шок). Внутримышечные инъекции болезненны, в некоторых случаях они ассоциировались с развитием саркомы ягодичной мышцы [Grasso P, 1973; Greenberg G., 1976]. По мнению некоторых авторов [Auerbach M. et al., 2007], от внутримышечного введения ПЖ следует отказаться.
В последнее время особенно большой интерес вызывают ПЖ для внутривенного введения с целью терапии постгеморрагических анемий. В нескольких работах показано, что внутривенное введение ПЖ более эффективно при сравнении с приемом железа внутрь при тех же показаниях. Помимо этого, внутривенная терапия позволяет избежать возникновения как побочных эффектов со стороны ЖКТ, наблюдающихся при приеме ПЖ внутрь, так и некоторых осложнений, вызываемых при внутримышечном введении ПЖ, однако требует определенного уровня реанимационной службы учреждения, в котором вводятся препараты.
ПЖ для внутривенного введения
Для внутривенного введения в России применяют карбоксимальтозат железа (Феринжект®), сахарат железа (Венофер), глюконат железа и декстран железа, которые представляют собой сферические железоуглеводные коллоиды. Углеводная оболочка придает комплексу стабильность, замедляет высвобождение железа и поддерживает образующиеся формы в коллоидной суспензии.
Внутривенное введение декстрана железа вызывает большое число анафилактических реакций, сопровождающихся летальностью в 13,5% случаев [Faich G. еt Strobos J., 1999], и в настоящее время применяется ограниченно. Применение натриевого комплекса глюконата железа в сукрозе вызывает значительно меньше осложнений и, как правило, не сопровождается смертельными исходами. Однако токсические эффекты, связанные с поступлением свободного железа в организм, существенно ограничивают применение препарата в ежедневной практике терапии ЖДА.
Сахарат железа (III) (Венофер®) является популярным препаратом для лечения синдрома ЖДА. Это связано с безопасностью и высокой переносимостью комплекса трехвалентного железа с сахаратом в отличие от декстрана железа и глюконата железа. Данный препарат одобрен для применения, в том числе и в период беременности. Венофер следует вводить только в учреждениях, располагающих оборудованием для сердечно-легочной реанимации, так как часто могут отмечаться сердечно-сосудистые осложнения в виде гипотонии. Максимальная разовая парентеральная доза сахарата железа (III) составляет 500 мг, предпочтительно развести препарат в 100 мл 0,9% раствора NaCl для введения в форме инфузии. Продолжительность инфузии составляет приблизительно 4,5 ч с использованием внутривенного доступа (следует помнить, что высокая скорость инфузии связана с риском развития гипотензивной реакции). В зависимости от исходных значений уровня гемоглобина внутривенное введение повторяют 1-3 раза/нед. до повышения уровня гемоглобина >105 г/л. Затем пациента можно перевести на прием пероральных ПЖ для поддерживающей терапии. Оснований ожидать возможной передозировки железом не имеется.
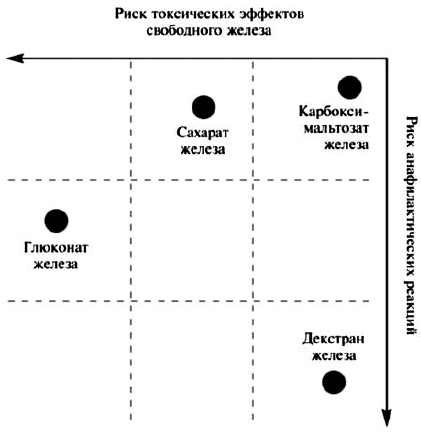
Эффективность и безопасность внутривенного введения ПЖ зависят от их молекулярной массы, стабильности и состава. Комплексы с низкой молекулярной массой, такие как глюконат железа, менее стабильны и быстрее высвобождают в плазму железо, которое в свободном виде может катализировать образование реактивных форм кислорода, вызывающих перекисное окисление липидов и повреждение тканей. Значительная часть дозы подобных препаратов выводится через почки в первые 4 ч после приема и не используется для эритропоэза. Хотя декстран железа обладает высокими молекулярной массой и стабильностью, его недостатком является повышенный риск развития аллергических реакций. Карбоксимальтозат железа сочетает в себе положительные свойства высокомолекулярных комплексов железа, но не вызывает реакции гиперчувствительности, наблюдающиеся при применении препаратов, содержащих декстран, и, в отличие от сахарата и глюконата железа, может вводиться в более высокой дозе [Geisser P., 2009]. Схема оценки риска токсических эффектов и анафилактических реакций препаратов свободного железа для внутривенного введения представлена на рисунке 1 [С.В. Моисеев, 2012].
Рис. 1. Риск токсических эффектов и анафилактических реакций при применении внутривенных препаратов железа
Применение карбоксимальтозата железа позволяет вводить за 1 инфузию до 1000 мг железа (внутривенно капельно в течение 15 мин.), в то время как максимальная доза железа в виде сахарата составляет 500 мг и вводится в течение 4,5 ч, а длительность инфузии декстрана железа достигает 6 ч. Причем в двух последних случаях перед началом инфузии необходимо ввести тестовую дозу препарата. Введение большой дозы железа позволяет сократить необходимое число инфузий и затраты на лечение. Карбоксимальтозат железа отличается не только удобством применения, но и низкой токсичностью, а также отсутствием оксидативного стресса, которые определяются медленным и физиологичным высвобождением железа из стабильного комплекса с углеводом, по структуре сходного с ферритином.