o rads 1 что значит в гинекологии
Новая система стандарта ультразвуковых исследований яичниковых образований для прогнозирования риска злокачественности опухоли
ФГБУ ДПО «Центральная государственная медицинская академия» Управления делами Президента РФ, Москва, Россия
В статье приведен обзор по новой мировой системе описания и обработки ультразвуковых исследований (УЗИ) яичниковых образований ORADS (Ovarian-Adnexal Imaging-Reporting-Data System), обеспечивающей единую диагностическую платформу, на которой могут работать как клиницисты, так и специалисты визуальной диагностики. Эта уникальная система представляет собой совокупность лексикона международного анализа опухолей яичников (IOTA) для оценки различных неоплазий и инкорпорированную модель IOTA-Adnex для прогнозирования риска злокачественности, которая успешно прошла проспективную и внешнюю валидацию. Приведен единый лексикон описания УЗ-данных при образованиях яичников и его трактовка, а также категоризация образований по степени риска малигнизации ORADS. В задачи этой классификации входят повышение качества УЗИ и улучшение ранней диагностики опухолей яичников, оптимизация работы врача-гинеколога- онколога в случаях подозрений на злокачественные новообразования яичников, улучшение клиническо- го ведения и предоперационной сортировки пациентов.
Заключение. Скорейшее внедрение этой классификации в клиническую практику является актуальной задачей для врачей всех специальностей, включенных в алгоритм профилактики, диагностики и лечения в акушерстве и гинекологии.
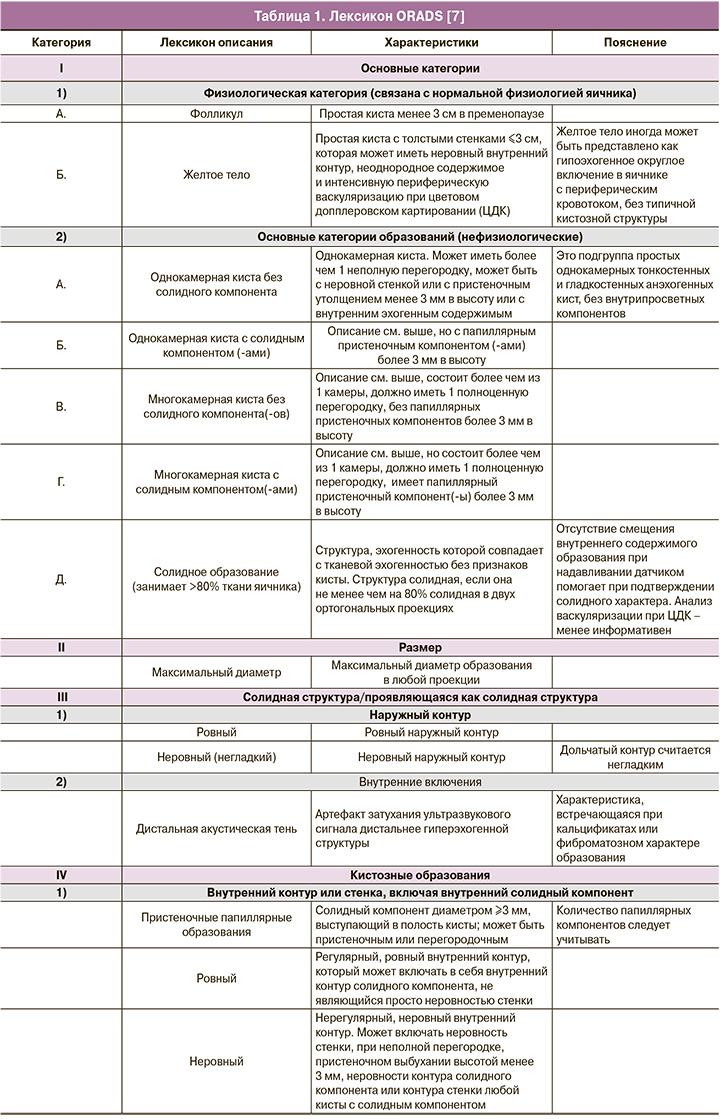
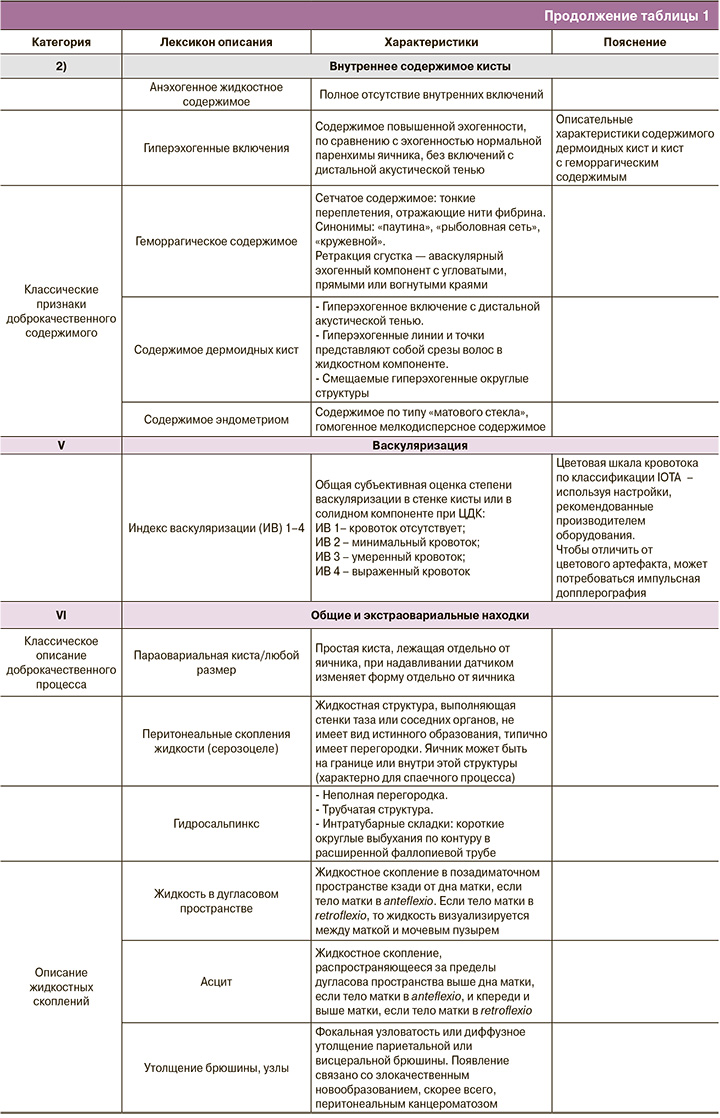
Рак яичников – серьезная проблема среди женщин всех возрастных групп, занимающая 7-е место по распространенности и 3-е место после рака тела и шейки матки среди всех злокачественных опухолей у женщин [1]. При этом рак яичников является лидирующим в структуре смертности от онкогинекологических заболеваний – половина больных не переживут 5-летний рубеж [2]. В России в 2019 г. зарегистрировано 14 318 больных раком яичников, при этом смертность составила 7616 [3]. Кроме истинных опухолей, в яичнике могут быть и опухолевидные образования, которые являются доброкачественными [4]. Частота ложноположительных диагнозов, основанных на данных визуальной диагностики при доброкачественных опухолях и опухолевидных образованиях яичников, остается высокой и достигает 30% [5], поэтому совершенствование алгоритмов визуальной диагностики с целью определения риска злокачественности представляет большой научный и практический интерес [6]. Оптимизация протоколов, создание единого стандарта терминологии и унификация категорий образований яичников с учетом риска их малигнизации позволит повысить качество исследований и улучшить раннюю диагностику опухолей яичников. В ноябре 2018 г. под руководством Американского общества радиологов совместно с международной группой экспертов по визуализации в гинекологии и лечению новообразований яичников был опубликован лексикон новой классификации образований яичников ORADS (Ovarian-Adnexal Imaging Reporting and Data System) [7]. ORADS – система описания и обработки данных ультразвуковых исследований (УЗИ) яичников. Этот стандартный лексикон описания ультразвуковых данных представлен в таблице 1 [7]. Балльная система ORADS колеблется от 1 до 5 с различными процентами риска того, что образование яичника является злокачественным (табл. 2). Опухолевые маркеры не играют никакой роли в оценке риска злокачественности в этой системе, и это пока первая гинекологическая ультразвуковая классификация, которая предложила варианты наблюдения, тактики ведения в каждой группе риска [8].
В последнем издании ORADS в 2020 г. уже рассматривается стандартизация в интерпретации образований яичников и их категоризация в отношении риска злокачественности, что должно значительно уменьшить двусмысленность в протоколах УЗИ, повысить вероятность постановки правильного диагноза и, соответственно, улучшить маршрутизацию [8]. Правильная интерпретация данных УЗИ в случае образований яичников, ведущая к постановке правильного диагноза, является ключом к точности в определении риска злокачественности новообразований и, наконец, оптимальному ведению пациентки.
Стоит упомянуть, что классификация ORADS включила в себя ранее изданные классификации IOTA (Международная группа по анализу опухолей яичников) и GI-RADS (Gynecologic Imaging Reporting and Data System), значительно дополнила их тактикой наблюдения и ведения, особенно для доброкачественных кист. Согласно новой классификации ORADS, алгоритм стратификации рисков делится на шесть основных категорий (ORADS 0–5), причем категории рисков разрабатывались комитетом на основе данных IOTA, и расчет риска проводился с учетом и соответствием риска злокачественности по IOTA-ADNEX модели.
ORADS 0
ORADS 0 является неполной оценкой из-за технических факторов, таких как газ кишечника, большой размер поражения, невозможный для оценки при УЗИ, или невозможность проведения трансвагинального УЗИ по причине болезненности.
ORADS 1
ОRADS 1 – физиологическая категория, которая актуальна только у пациенток в пременопаузе, включает фолликул и желтое тело. В заключении рекомендуется их описывать, как фолликул и желтое тело, а не как кисту.
ORADS 2
ORADS 2 – однозначно доброкачественная категория (риск злокачественности 1%); в нее вошло большинство однокамерных кист менее 10 см: простые кисты; несложные однокамерные с гладкими внутренними стенками и кисты, которые могут быть описаны с помощью классических доброкачественных поражений и их дескрипторов, если их максимальный диаметр составляет менее 10 см. К ним относятся: типичная геморрагическая киста, дермоидная киста, эндометриома, параовариальная киста, серозоцеле и гидросальпинкс (рис. 1). Хотя анализ васкуляризации не включен в оценку поражений в категории ORADS 2, он проводится в обязательном порядке, особенно при наличии.
Стратификация рисков злокачественности образований яичников. Интеграция МРТ в систему O-RADS
1) ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова» Министерства здравоохранения Российской Федерации, Москва, Россия;
2) ФГАОУ ВО «Первый Московский государственный медицинский университет имени И.М. Сеченова» Министерства здравоохранения Российской Федерации (Сеченовский Университет), Москва, Россия;
3) Московский научно-исследовательский онкологический институт имени П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Министерства здравоохранения Российской Федерации, Москва, Россия
В данном обзоре проведен анализ современных литературных данных, посвященных лучевой диагностике образований яичников (ОЯ), проблемам скрининга рака яичника (РЯ), современным методам классификации с учетом основных характеристик и рисков малигнизации ОЯ. На сегодняшний день первым этапом визуализационной диагностики является ультразвуковое исследование (УЗИ). Разработано множество различных систем оценок характеристик ОЯ, основанных на ультразвуковых показателях. Одна из современных перспективных систем – стандартизированная шкала оценки результатов УЗИ O-RADS (Ovarian-Adnexal Reporting and Data System), целью которой является улучшение междисциплинарных взаимодействий специалистов и повышение точности диагностики. На основании существующей системы O-RADS в 2020 г. был представлен алгоритм оценки результатов и стратификации рисков злокачественности ОЯ, выявляемых при МРТ, – O-RADS MRI (Ovarian-Adnexal Reporting and Data System Magnetic Resonance Imaging). Данный алгоритм дает возможность стратифицировать риск злокачественности новообразований яичников, оценивая МР-картину на основании пяти сформулированных категорий.
Заключение. Согласно проведенным исследованиям, в т.ч. внешней валидации, O-RADS MRI демонстрирует не только точность балльной системы и высокую эффективность, но и простоту в использовании, что дает возможность рекомендовать шкалу O-RADS MRI в качестве рутинной системы оценки МР-изображений для дифференциации и стратификации рисков малигнизации ОЯ, при неопределенной степени злокачественности по данным УЗИ
Образования яичников (ОЯ) представляют собой гетерогенную группу заболеваний с полиморфной гистологической структурой. Рак яичников (РЯ) занимает 7-е место в структуре всех злокачественных новообразований и 3-е место среди гинекологических новообразований [1]. ОЯ диагностируются у 1 из 10 женщин, при этом около 2% ОЯ являются злокачественными или пограничными [2, 3]. Злокачественные ОЯ имеют наиболее высокие показатели летальности среди всех гинекологических злокачественных новообразований. По данным American Cancer Society (ACS), рак яичников занимает 5-е место в структуре смертности от всех злокачественных новообразований у женщин [4]. Высокие показатели смертности от РЯ обусловлены выявлением заболевания на поздних стадиях (III–IV), что связано с трудностями ранней диагностики и отсутствием патогномоничного симптомокомплекса на ранних этапах развития болезни [5, 6]. Зачастую жалобы пациенток при РЯ неспецифичны и обусловлены распространенностью опухолевого процесса. Среди жалоб наиболее частыми являются: повышенная утомляемость, слабость, боль и ощущения вздутия в животе, увеличение его в объемах, запоры, нарушения мочеиспускания, боли в спине [6, 7].
У большинства пациенток (≤75%) РЯ диагностируется на III–IV стадиях [8], когда имеется выраженное распространение опухолевого процесса (преимущественно по брюшине) и отдаленное метастазирование. В 70% случаев летальность и рецидив приходятся на первые 5 лет жизни после установления диагноза. Таким образом, лишь в 30% и менее диагноз устанавливают на ранних стадиях, когда потенциально может быть положительный прогноз, что позволяет повысить выживаемость среди больных РЯ [5]. Раннее выявление РЯ позволяет увеличить процент пятилетней выживаемости до 93%, однако до настоящего времени эффективных скрининговых программ не разработано [9].
Согласно исследованию Freddie Br. и соавт., в 2018 г. в мире было диагностировано 295 414 новых случаев РЯ и зафиксировано 184 799 летальных случаев в течение первого года от момента установки диагноза [10]. В структуре онкологической заболеваемости РЯ занимает лидирующие позиции среди причин смертности у женщин во всем мире.
В России на 2019 г. заболеваемость РЯ составила 78,7 случаев на 100 000 женщин, при этом летальность в течение первого года после установления диагноза достигала 19,4%. Высокие показатели смертности при РЯ обусловлены поздней диагностикой. Так, удельный вес РЯ, диагностированного на III и IV cтадиях, из числа впервые выявленных злокачественных новообразований в России в 2019 г. составил 38,4% и 20,0% соответственно [11].
Несмотря на активное развитие диагностических возможностей, проблема раннего выявления ОЯ и дифференциальной диагностики является крайне актуальной. Отсутствие детальной характеристики структуры, распространенности процесса, в ряде случаев – корректной органопринадлежности образования на этапе неинвазивной диагностики ограничивает возможности и эффективность лечения. Определяющим фактором при выборе тактики ведения пациенток является комплекс уточняющей диагностики выявленных изменений яичников. Выбор консервативного подхода в случае функциональных и доброкачественных изменений, малоинвазивной хирургии с функциональным и органосохраняющим подходом у женщин репродуктивного возраста при доброкачественных и пограничных опухолях, максимально радикальный объем в объеме экстирпации матки с придатками и резекцией большого сальника основываются на данных дифференциальной диагностики [7, 12].
Учитывая тенденцию к «омоложению» РЯ и повышение частоты пограничных опухолей у молодых пациенток активного репродуктивного возраста, требуется четкая стратификация рисков при определении или исключении признаков злокачественности, определяющая возможность проведения органосохраняющего лечения либо необходимость комбинированного лечения в сочетании неоадъювантной и/или адъювантной химиотерапии с дополнительными возможностями криоконсервации ткани яичника при необходимости [6, 7].
Что означает на маммографии BI-RADS
Что означает BI-RADS
Классификация BI-RAD
Классификация BI-RADS имеет 6 категорий. Они распределены по уровню опасности. Чем выше число тем больше шанс того, что у пациентки развивается рак молочной железы:
Категория BI-RADS 0 после маммографии означает недостаточность исследования. Врач не может сделать вывод, необходима дополнительная диагностика. Среди методов — МРТ (магнитно-резонансная томография), КТ (компьютерная томография, УЗИ (ультразвуковое исследование).
Ситуация возможна при травматизации груди, а также при наличии / повреждении имплантов молочных желез. Проходить маммографию с имплантами необходимо только на цифровых аппаратах — рентгенографическое оборудование не дает необходимой точности результата.
Категория BI-RADS 1 в маммографии означает, что патологии не обнаружены. У пациентки отсутствуют:
Категория BI-RADS 2 означает, что признаки злокачественных новообразований не обнаружены, но присутствуют доброкачественные изменения. Они не требуют дополнительного обследования. К ним относят:
Категории BI-RADS 3 означает, что обнаружена доброкачественная патология. Вероятность этого — 98 процентов. При этом имеется 2% риск злокачественных изменений. К таким патологиям относят:
Категории BI-RADS 4 при маммографии означает подозрение на злокачественность новообразований в молочной железе. Врач назначает биопсию — забор биоматериала и его морфологическое исследование. Это позволит подтвердить качественность заболевания.
BI-RADS 4 разделяют на уровни подозрения:
Врач направляет пациентку на следующие исследования:
Прогноз: риск рака молочной железы при разных значениях BI-RADS
Основной процент профилактических маммограмм получает результат 1 или 2 по классификации BI-RADS. В остальных случаях шанс злокачественности:
В маммологическом центре L7 ведут прием опытные маммологи-онкологи. Диагностика происходит на современном оборудовании, которое гарантирует 95% точность. Чтобы записаться на консультацию специалиста в клинике L7:
Мой опыт составляет более 160 лапароскопических операций при раке матки с позитивными результатами, который обобщен в монографиях и научных трудах. Ежегодно я провожу мастер-классы для гинекологов и онкологов по проблемам хирургического лечения рака матки.
Посмотреть видео операций в моем исполнении Вы можете на сайте «Видео операций лучших хирургов мира».
Актуальность проблемы рака тела матки (рака эндометрия).
Рак тела матки (синоним: рака эндометрия) – злокачественная опухоль матки, исходящая из слизистого слоя (эндометрия). Рак тела матки занимает 3-е место по частоте после рака шейки матки и молочной железы среди женщин в возрасте до 54 лет и 2-е место среди женщин старше 55 лет. Ежегодно в России регистрируется более 21000 больных раком тела матки.
В структуре заболеваемости злокачественными опухолями тела матки до 75% составляют женщины в пре- и постменопаузе (старше 50 лет), но в последние годы заметна тенденция омоложения контингента больных. По данным МНИОИ им. Герцена П.А. аденокарцинома эндометрия диагностируется у 10% женщин моложе 40 лет.
Факторы риска развития рака тела матки
У пациентки, находящейся в операционной телевизионной клиники программы «Здоровье», самая злокачественная форма рака матки. Бригада врачей-эндоскопистов под руководством профессора К.В. Пучкова виртуозно провела бескровную операцию по удалению рака матки
Международная классификация болезней Х пересмотра
С54.0 – рак перешейка матки (нижнего сегмента матки)
C54.1 – рак эндометрия
C54.2 – рак миометрия
C54.3 – рак дна матки
C54.9 – рак тела матки неуточненной локализации
Клиническая картина рака тела матки
В 80% случаев рак тела матки диагностируется на I-II стадиях ввиду наличия характерных симптома – кровяные выделения их половых путей. В репродуктивном периоде эти выделения носят ациклический характер (не связаны с менструацией), в постменопаузе само наличие кровяных выделений из половых путей позволяет заподозрить злокачественные изменения в матке. В ряде случаев рак эндометрия может протекать бессимптомно.
Также могут отмечаться такие симптомы, как тянущие боли в нижних отделах живота, водянистые выделения из половых путей с неприятным запахом, диспареуния (боли и дискомфорт во время полового акта).
Диагностика рака тела матки
Эндометрий – гормонально чувствительная ткань. В течение всего менструального цикла он претерпевает изменения: постепенно утолщается и меняет структуру, готовясь к имплантации эмбриона, если же беременность не наступает – происходит его отторжение, проявляющееся в виде менструации, и цикл роста слизистой в полости матки начинается заново.
Чаще всего образованию рака эндометрия предшествует доброкачественный процесс – гиперплазия эндометрия – чрезмерное разрастание клеток слизистой полости матки, за счет чего увеличивается ее объем и толщина. При длительном существовании, отсутствии лечения и наличии факторов риска гиперплазия эндометрия может трансформироваться в рак, в связи с чем гиперплазию относят к предраковым заболеваниям матки. Особую настороженность при гиперплазии эндометрия вызывают 2 фактора: атипическая гиперплазия эндометрия по гистологическому строению и рецидивы заболевания (повторное образование гиперплазии в течение 2-х лет после проведенного лечения) – это наиболее частые ситуации, предшествующие образованию рака эндометрия.
Поставить диагноз гиперпластического процесса и рака эндометрия можно только на основании гистологического исследования, поэтому во всех случаях, когда по данным УЗИ органов малого таза возникают подозрения на наличие патологии эндометрия первым этапом проводится гистероскопия с раздельным диагностическим выскабливанием слизистой шейки и полости матки. Целью данной операции является удаление патологически измененной ткани и определение ее гистологической структуры для определения дальнейшей тактики лечения.
При подтверждении рака эндометрия по данным гистологии для определения распространенности процесса проводится следующее дообследование:
Типы рака тела матки (рака эндометрия)
Для определения стадии заболевания при раке эндометрия и степени поражения соседних органов, а также выбора правильной тактики хирургического лечения необходимо прислать мне на личный электронный адрес puchkovkv@mail.ru puchkovkv@mail.ru копировать описание УЗИ органов малого таза и брюшной полости, данные МРТ малого таза с контрастом, результаты гистероскопии и гистологии, указать возраст и основные жалобы. Тогда я смогу дать более точный ответ по вашей ситуации.
| Признаки | 1 патогенетический вариант (гормонозависимый) | 2 патогенетический вариант (гормононезависимый, автономный) |
| Гормональный фон | Хроническая гиперэстрогения | Гипоэстрогения (в менопаузе) |
| Менструальная функция | В анамнезе ановуляторные маточные кровотечения | Не нарушена |
| Детородная функция | Нередко бесплодие | Не нарушена |
| Время наступления менопаузы | Часто после 50 лет | Обычно до 50 лет |
| Тип кольпоцитологической реакции в менопаузе | Эстрогенный | Атрофический |
| Состояние яичников | Гиперплазия тека-ткани Синдром Штейна-Левенталя Феминизирующие опухоли | Фиброз |
| Фон эндометрия или произведенные ранее соскобы | Гиперпластические процессы | Атрофия |
| Состояние миометрия | Фибромиома, внутренний эндометриоз | Без особенностей |
| Нарушение жирового обмена | Есть | Нет |
| Сахарный диабет | Есть | Нет |
| Гипертоническая болезнь | Сочетается с ожирением и/или сахарный диабетом | Отсутствует или не сочетается с ожирением и сахарным диабетом |
| Т-система иммунитета | Без существенных изменений у 60-70% больных | Иммунодепрессия у 30-40% больных |
В результате комплексных исследований была выдвинута и обоснована концепция о двух основных патогенетических вариантах РТМ ( Бохман Я.В., 1985):
| Особенности течения | 1 вариант | 2 вариант |
| Продолжительность симптомов | Обычно длительная | Обычно короткая |
| Степень дифференцировки опухоли | Высокая (чаще 1 или 2 степень) | Снижена (чаще 3 или 4 степень) |
| Глубина инвазии в миометрий | Чаще поверхностная | Чаще глубокая |
| Потенции к лимфогенному метастазированию | Невысокие | Высокие |
| Чувствительность к Прогестагенам | Высокая | Невысокая |
| Первично множественные опухоли | Не характерны | |
| Прогноз | Благоприятный | Сомнительный |
| 5-летняя выживаемость | 85,6% | 58,8% |
Для того чтобы отнести каждое конкретное наблюдение к первому патогенетическому варианту рака тела матки, необходимы 2 условия: соответствие более, чем половине его признаков и сочетание симптомов гиперэстрогении с обменными нарушениями.
В практической работе возможен упрощенный вариант определения патогенетического варианта в постменопаузе: сочетание ожирения и эстрогенного типа кольпоцитологической реакции позволяет отнести данное наблюдение к 1 варианту (Бохман Я.В., 1985).
Определение у каждой больной 1 или 2 патогенетического варианта РТМ поможет лечащему врачу более внимательно оценить особенности организма и выбрать рациональный план лечения.
Особенности опухоли матки и ее клинического течения в зависимости от патогенетического варианта:
У больных РТМ установлена достоверная корреляция патогенетического варианта со степенью дифференцировки опухоли.
В 80-90% случаев РТМ представляет собой аденокарциному. Выделяют 3 степени дифференцировки аденокарциономы:
Остальные наблюдения распределяются между имеющими несколько худший прогноз светлоклеточной мезонефроидной аденокарциномой и диморфным железисто-плоскоклеточным раком.
Светлоклеточный (мезонефроидный) рак матки составляет менее 5% от всех случаев рака тела матки. Чаще наблюдается у пожилых больных, отличается чрезвычайно агрессивным течением и плохим прогнозом. Пятилетняя выживаемость при светлоклеточном раке матки колеблется от 33 до 64% и зависит от глубины инвазии в миометрий и наличия раковых эмболов (Козаченко В.П., 2005).
Международная классификация стадий рака тела матки
Недостаточно данных для оценки первичной опухоли
Первичная опухоль не определяется
Преинвазивная карцинома (carcinoma in situ)
Опухоль ограничена телом матки
Опухоль в пределах эндометрия
Инвазия в миометрий менее 1/2 его толщины
Инвазия в миометрий более 1/2 его толщины
Опухоль распространяется на шейку, но не выходит за пределы матки
Опухоль распространяется на канал шейки матки в пределах эндоцервикальных желез
Опухоль распространяется на строму шейки матки
Местное и/или регионарное распространение опухоли
Прорастание серозной оболочки матки и/или
в придатки матки (прямое распространение или метастазы) и/или наличие опухолевых клеток в асците или смывах из брюшной полости
Опухоль распространяется на влагалище (прямое распространение или метастазы)
Метастазы в тазовых и/или поясничных лимфатических узлах
Метастазы в тазовых лимфатических узлах
Метастазы в поясничных лимфатических узлах
Прорастание слизистой оболочки мочевого пузыря и/или прямой кишки (наличие буллезного отека недостаточно для отнесения опухоли к Т4)


Благодаря накоплению клинического опыта, показания к лимфаденэктомии у больных РТМ претерпели значительную эволюцию, где определяющими являются 2 аспекта: целесообразность расширения объема операции с точки зрения особенностей лимфогенного метастазирования и возможность ее осуществления у пожилых людей, нередко страдающих выраженными эндокринно-обменными нарушениями.
Показаниями к забрюшинной лимфаденэктомии при раке эндометрия (раке тела матки) являются наличие одного или нескольких неблагоприятных факторов прогноза (Козаченко В.П., 2005):
Этапы лимфогенного метастазирования:
1 этап – наружные и внутренние подвздошные, запирательные л/у;
2 этап – поясничные и общие подвздошные л/у;
3 этап – латеральные крестцовые, паховые, нижние и верхние ягодичные л/у.
При 1 клинической стадии рака матки метастазы в лимфатических узлах диагностируются:
ЛЕЧЕНИЕ РАКА ТЕЛА МАТКИ
При отсутствии прямых противопоказаний (генерализация заболевания, тяжелые сопутствующие заболевания) хирургическое лечение является основным или первым этапом в лечении больных злокачественными опухолями тела матки.
Основной путь метастазирования РТМ лимфогенный. Клинический опыт многих тысяч операций показывает, что удаление опухоли до формирования регионарных и отдаленных метастазов обеспечивает стойкое излечение большинства больных.
Доказано, что у 38% больных первой клинической стадии во время операции обнаруживается большее распространение опухоли, чем предполагалось до вмешательства, а метастазы в лимфатических узлах таза выявляются в 16% случаев (Я.В. Бохман, 2002г).
При образовании метастазов рака тела матки в регионарных лимфатических узлах, их барьерная иммунологическая функция на какое-то время задерживает наступление широкой диссеминации опухоли, поэтому в тех случаях, когда процесс не вышел за пределы органа и регионарных лимфатических узлов 1 порядка, применение расширенных оперативных вмешательств может обеспечить длительное излечение больных со злокачественными опухолями матки.
При значительном местном и регионарном распространении злокачественной опухоли матки повышается вероятность возникновения ортоградных и ретроградных лимфогенных метастазов в отдаленные лимфатические узлы, а также гематогенных метастазов. Естественно, что при этом хирургические воздействия, направленные на первичную опухоль и ее регионарные лимфатические коллекторы, не решают основных проблем лечения. Однако удаление основной массы опухоли, несомненно, способствует реализации эффекта лекарственного лечения, направленного на диссеминированные опухолевые клетки (Бохман Я.В., 2002).
Нельзя недооценивать важность клинического стадирования рака матки на этапе предоперационного обследования, во многом предопределяющего объем оперативного вмешательства. Необходимо уточнить локализацию опухоли, ее гистологическую структуру и степень дифференцировки, вероятность регионарных метастазов.
Особенности хирургического лечения рака тела матки
При каждой стадии заболевания выбор тактики определяется для каждого пациента консилиумом 3 врачей: хирурга-онколога, химиотерапевта и радиолога с учетом индивидуальных особенностей, таких как возраст, общее состояние, наличие сопутствующей патологии.
Я всегда выполняю операцию лапароскопическим доступом. Для максимального и при этом бережного удаления окружающей органы клетчатки, несущей в себе лимфатические узлы и сосуды, я использую аппарат Thunderbeat (Olympus, Япония), сочетающий в себе ультразвуковую и биполярную энергии, за счет чего удается добиться абсолютно сухого поля. Во время операции я использую и другие электрохирургические аппараты, например, LigaSure (Covidien, Швейцария). Выбор инструмента зависит от ткани, на которой происходит работа в данный момент, и поставленных задач. Благодаря лапароскопическому доступу и использованию самого современного оборудования мне удается добиться максимальной эффективности, безопасности и быстроты выполнения вмешательства, отсутствует потребность в установке дренажей, в результате техника операции получается максимально щадящей. Это позволяет пациентке максимально быстро активизироваться, ускоряет сроки реабилитации и значительно приближает сроки адъювантного лечения (при его необходимости).
Техника лапароскопической операции при раке тела матки (эндометрия):
Латеральными границами являются мочеточники, которые окружены фасциальным листком (этот фасциальный футляр образован двумя листками околопочечной фасции). Таким образом, дальнейшую лимфодиссекцию осуществляют по ходу внутрибрюшной фасции, оттесняя забрюшинную фасцию с проходящими в ней мочеточниками латерально. Дорсальной границей лимфодиссекции на этом этапе операции является поясничная мышца. Сигмовидную кишку зажимом Бебкокка отводят медиально, делая окно в области корня брыжейки. Выполняют лимфодиссекцию в области бифуркации аорты и нижней полой вены, вдоль подвздошных сосудов.
Следуя вдоль внутрибрюшной фасции и ориентируясь на надкостницу крестца в области мыса, отсепаровывают париетальную фасцию таза. Начинают удаление париетальной фасции с задней полуокружности с последующим переходом на боковые стенки. Тазовую лимфодиссекцию начинают с отсепаровки париетальной фасции от крестца.
Самым сложным этапом тазовой лимфодиссекции является латеральная лимфаденэктомия. На данном этапе следует быть максимально осторожным, чтобы не повредить расположенный латеральнее наружной подвздошной артерии бедренно-половой нерв и проходящую кнутри подвздошную вену. Последняя обычно находится в спавшемся состоянии вследствие повышенного внутрибрюшного давления, обусловленного пневмоперитонеумом. Лимфодиссекцию из запирательного пространства осуществляют следующим образом. Мочеточник выделяют и отводят медиально. Захватив жестким зажимом края рассеченной брюшины, вдоль наружной подвздошной артерии латеральнее мочеточника посредством острой и тупой отсепаровки удаляют клетчатку по направлению к наружной подвздошной вене.
С помощью эндоскопического ретрактора наружные подвздошные сосуды отводят латерально и вверх, открывая доступ к запирательным областям. При этом кзади и медиально обнаруживается запирательный нерв с сопровождающими его сосудами и внутренняя запирательная мышца, которая является ориентиром глубины лимфодиссекции. Постоянно осуществляя тракцию вверх и в стороны, удаляют клетчатку, расположенную под наружными подвздошными сосудами в запирательной области единым блоком с сохранением запирательного нерва.
Длительность операции в руках опытного хирурга составляет около 1,5 часов. Количество осложнений не превышает 1,7 %.
После тщательного гистологического исследования удаленного препарата проводится окончательное стадирование процесса и выбор тактики дальнейшего лечения совместно с химиотерапевтом и врачом лучевой диагностики.
Диспансерное наблюдение
Пятилетняя выживаемость
Прогнозы выживаемости сильно варьируют в зависимости от гистологического строения опухоли и степени дифференцировки клеток. Усредненные показатели представлены ниже.