неорганические соединения в жизни человека
Применение изученных неорганических и органических веществ
Содержание:
Известные науке химические элементы образуют примерно 1 млн. неорганических и более 20 млн. органических веществ. В лабораториях синтезируется 200–250 тыс. новых соединений. Все они нашли широкое применение в различных сферах деятельности человека, начиная от медицины и заканчивая машиностроением, оборонным комплексом.
Применение неорганических веществ
К неорганическим относят соединения, которые не содержат углерод, а также углеродосодержащие вещества, традиционно относящиеся к неорганическим (карбиды, оксиды и др.).
Применение данных соединений достаточно распространено в повседневной деятельности человека, и без них невозможно полноценное ведение хозяйства, лечение, производство и т.п.
Гидрокарбонат натрия (NaHCO3 ) – представляет собой мелкий порошок белого цвета, без запаха, растворимый в воде. Используется преимущественно в кулинарии, для выпечки. Это обусловлено тем, что во время нагревания сода легко разлагается с выделением углекислого газа.
Кроме этого гидрокарбонат натрия используется для придания пышности омлету, смягчения мяса, усиления аромата чая или кофе, добавления сладости плодам фруктов, очищения продуктов от нитратов и т.д.
Na2CO3 — применяется для бытовых нужд:
Для использования необходимо развести раствор от 10 до 100 °С.
Поваренная соль (NaCl) – незаменимая приправа при приготовлении первых, вторых блюд, консервации и даже выпечки. Суточная норма натрия для организма человека составляет 1 г, но употребление значительно превышает эту норму (4-6 г). Осторожнее к потреблению данного продукта следует относиться людям, страдающим повышенным давлением, склонным к появлению отеков.
Сильная двуосновная кислота (H2SO4) представляет собой бесцветную тяжелую маслянистую жидкость, не обладающую запахом. Широко распространено использование средства в различных отраслях промышленности:
Так же соединения серы используется в качестве электролита в свинцовых аккумуляторах.
Цинковые белила (ZnO) – представляет собой белый порошок, меняющий цвет при нагревании. Применение продукта известно в медицине, химической промышленности в качестве наполнителя или пигмента:
Данное соединение обладает фотокаталитической активностью, что нашло свое применение при изготовлении самоочищающихся поверхностей, бактерицидных покрытий для помещений больниц и подобных учреждений.
Сульфат меди II (CuSO4) – бесцветное кристаллическое соединение, растворимое в воде. При реакции с воздухом или водой образуется голубой пентагидрат.
основные соли азотной кислоты : нитрат натрия, нитрат магния, нитрат аммония
Азотсодержащие удобрения (селитры).
Соли фосфорной кислоты: Фосфат кальция
Гидрофосфат кальция
Суперфосфат
Прокаленный песок: Оксид кремния (IV)
Производство керамических изделий.
Твердые и жидкие соли карбоновых кислот: Пальмитат натрия/калия
Стеарат натрия/калия
Мыла
Натриевые соли высших карбоновых кислот – твердые мыла, а калиевые соли высших карбоновых кислот – жидкие мыла.
Используется при производстве резины. Для этого серу нагревают (вулканизируют) с каучуком.
Кислые соли натрия, например: Гидрокарбонат натрия.
Твердое вещество, использующееся в качестве разрыхлителя теста, а также в качестве чистящего средства.
Соединения аммония например: Карбонат аммония
Используется как разрыхлитель теста благодаря тому, что при нагревании образует газообразные продукты разложения в соответствии с уравнением:
(NH4)2CO3 => 2NH3 + CO2 + H2O
Карбоновые кислоты : Этановая (уксусная) кислота
Используется для консервирования овощей. Концентрированные растворы вызывают ожоги.
Твердый Активированный уголь
Твердое вещество черного цвета используется в качестве поглотителя (адсорбента) в фильтрах, а также как лекарственное средство при различных видах отравлений.
Раствор пищевого спирта: Этанол (этиловый спирт).
C2H5OH
Основной компонент алкогольных напитков, может быть использован в качестве топлива. Жидкость со специфическим запахом.
Жидкие трехатомные спирты: Глицерин
Используется в парфюмерии и пищевой промышленности.
Изомерные соединения алканов: Тетрахлорид углерода CCl4
Сырье для получения удобрений (нитратов калия, натрия, аммония).
Сырье для получения азотной кислоты.
Используется как компонент стеклоочистительных жидкостей, жидкость с резким запахом.
В аптечке – нашатырный спирт, применяется для приведения в чувство человека, потерявшего сознание.
Аллотропное соединение кислорода: Озон O3
Дезинфекция (очистка) воды.
Дезинфекция (очистка) воды.
Используется для сварки и резки металла благодаря тому, что при горении ацетилена развивается крайне высокая температура – около 3000 о С
Основной компонент природного газа. Горючее для газовых плит.
Раствор Лимонной кислоты
Используется для удаления накипи с внутренней поверхности чайника.
Используется в качестве антисептика (дезинфицирующего средства) при обработке небольших ран и порезов.
Изомерные соединения алкенов и их производных: Хлоропрен (2-хлорбутадиен-1,3)
Изопрен (2-метилбутадиен-1,3)
Бутадиен (дивинил)
Сырье для производства каучука.
Спиртовой раствор Йода
Спиртовой раствор данного вещества используется для дезинфекции мелких порезов и царапин.
Применение органических веществ
Органические вещества – это класс химических соединений, объединяющий все вещества, в состав которых входит углерод.
Широко распространено применение данной группы органических соединений в химической промышленности (для производства пластмасс, синтетических волокон и т.д.) и медицине.
Соединения служат исходными веществами для получения ряда готовых продуктов:
Этилен (Н2С=С Н2) используется для получения, тефлона, этилового спирта, уксусного альдегида, галогенопроизводных и многих других органических соединений.
Алкены применяются и для ускорения процесс созревания фруктов.
Алкины (ацетиленовые углеводороды)
Ацетилен – необходим в качестве исходного продукта в органическом синтезе при производстве:
Температура пламени вещества достигает 3150°С, что нашло свое применение при резке металла и в сварке.
Алкоголи – производные углеводородов, в которых один или несколько атомов водорода замещены на гидроксильную группу ОН.
Метанол (СН3ОН) –применяется в производстве муравьиной кислоты и формальдегида. Рассматривается как вариант для применения в качестве моторного топлива.
Этанол (С2Н5ОН)- востребован в виде исходного соединения для получения уксусной кислоты, сложных эфиров, карбоновых кислот. Вещество служит основой производства спиртосодержащей продукции и антисептических средств.
Этиленгликоль – компонент необходимый в производстве пластмасс, антифризов, органическом синтезе.
Глицерин – незаменим в разных отраслях промышленности, в том числе текстильной, пищевой, фармакологии.
Основное использование соединений приходится на химическую промышленность, медицину (производство синтетических смол, красителей, антисептиков, взрывчатых веществ и т.д.).
Метаналь – используется при получении фенолформальдегидных и карбамидных смол, синтезе лекарственных средств, как дезинфицирующее средство.
Соединения, карбоксильной группы –СООН.
Бензойная кислота (С6Н5СООН) – незаменима в фармацевтике для синтеза душистых веществ и красителей, а также в качестве консерванта для пищевых продуктов.
Применяются в пищевой и парфюмерной отраслях в качестве отдушек. А также обеспечивают эластичность и пластичность пластмасс и резины.
Также широко распространено в пищевой промышленности, медицине применение глюкозы, аминов, аминокислот. Целлюлоза основной компонент при изготовлении бумаги, пленок, искусственных волокон и т.д.
Много соединений еще не изучено до конца, и возможно, благодаря науке человек сможет заменить натуральные продукты на искусственные, органических соединений природного происхождения применяется все меньше.
Неорганические и органические вещества клетки
Большинство реакций, которые протекают в клетке, идут в растворе (водной среде). Полярность молекулы воды позволяет ей быть отличным растворителем для других гидрофильных (полярных) веществ.
Вода может поглощать теплоту при минимальном изменении температуры. Это настоящее «спасение» для клеток: чуть только температура меняется, вода начинает поглощать избыток тепла, защищая клетку от перегревания. Выделяясь на поверхность кожи с потом, вода испаряется, поверхность кожи при этом охлаждается.
Питательные вещества, газы перемещаются по организму с током крови. Вода составляет 90-92% плазмы крови, является ее основным компонентом. С помощью воды происходит не только доставка веществ к клеткам, но и удаление из организма побочных продуктов обмена веществ.
Если же клетка окажется в гипотоническом растворе, то вода извне устремится внутрь клетки (опять-таки в сторону большей концентрации солей), приводя при этом к разбуханию (и возможному разрыву) клетки.
Элементы
Процентное содержание элемента не коррелирует с его важностью и биологической значимостью. Так, к примеру, микроэлемент I играет важную роль в синтезе гормонов щитовидной железы: тироксина, трийодтиронина. За нормальные рост и развитие организмов отвечают Zn, Mn, Cu.
Благоприятно влияют на сперматозоиды Zn, Ca, Mg, защищая их от оксидативного стресса (окисления). Невозможным становится нормальное образование эритроцитов без должного уровня Fe и Cu.
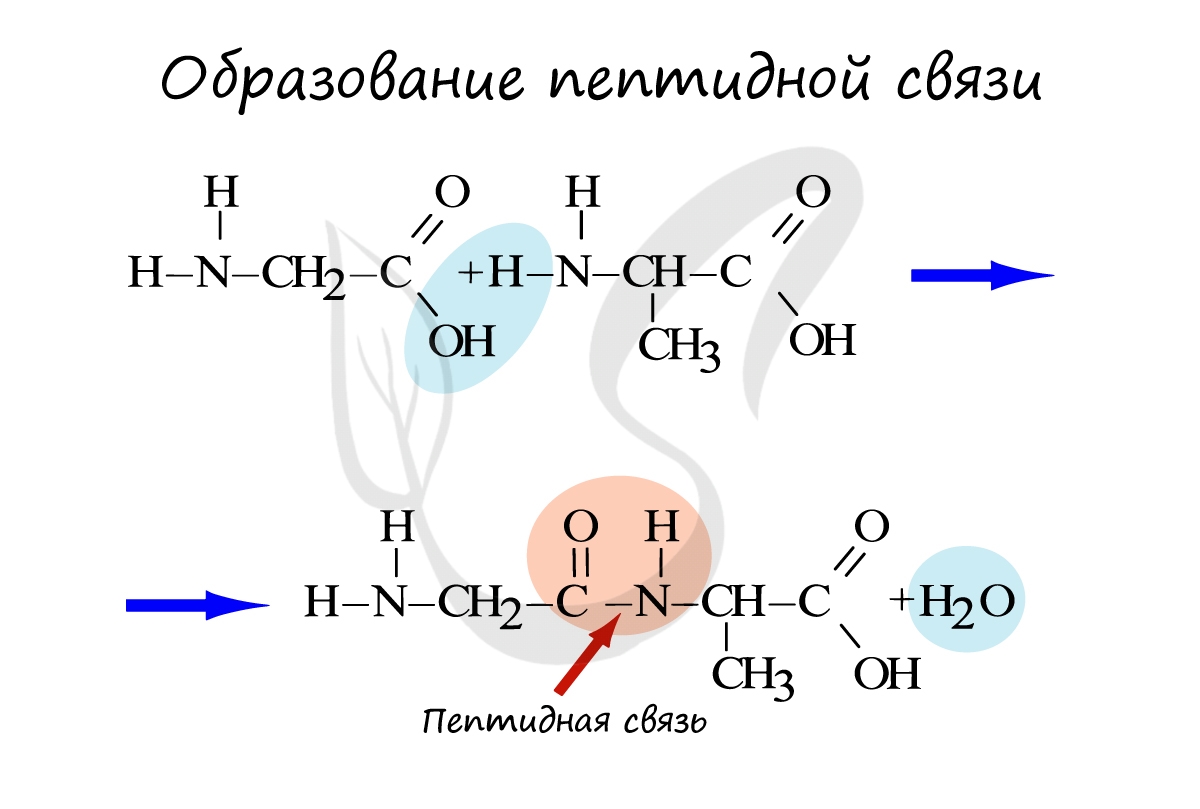
Мы переходим к органическим компонентам клетки, к которым относятся: жиры, углеводы, белки и нуклеиновые кислоты.
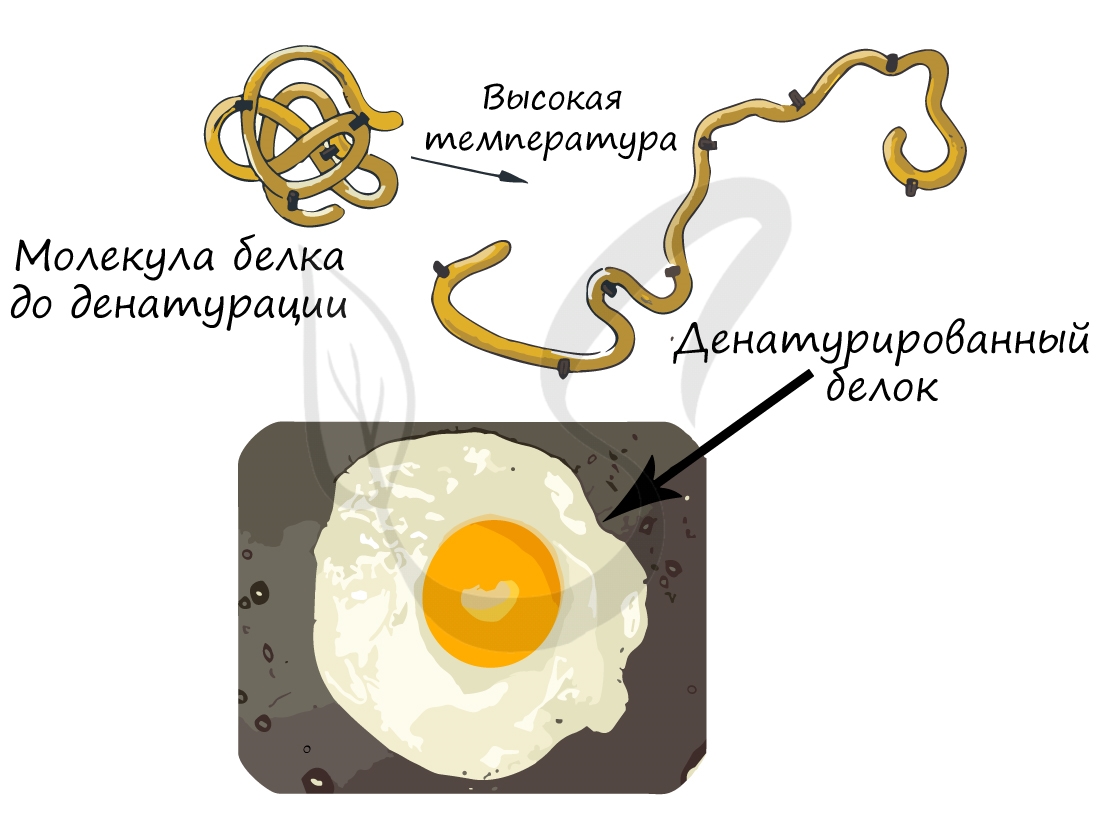
При резком изменении оптимальных для белка условий он подвергается денатурации: при этом происходит переход от высших структур организации к низшим, или «раскручивание белка». Важно заметить, что аминокислотная последовательность (первичная структура белка) при этом не меняется, однако свойства белка меняются кардинально (теряется его гидрофильность).
Некоторые гормоны, регулирующие обменные процессы в организме, имеют белковое происхождение: инсулин, глюкагон, адренокортикотропный гормон (АКТГ).
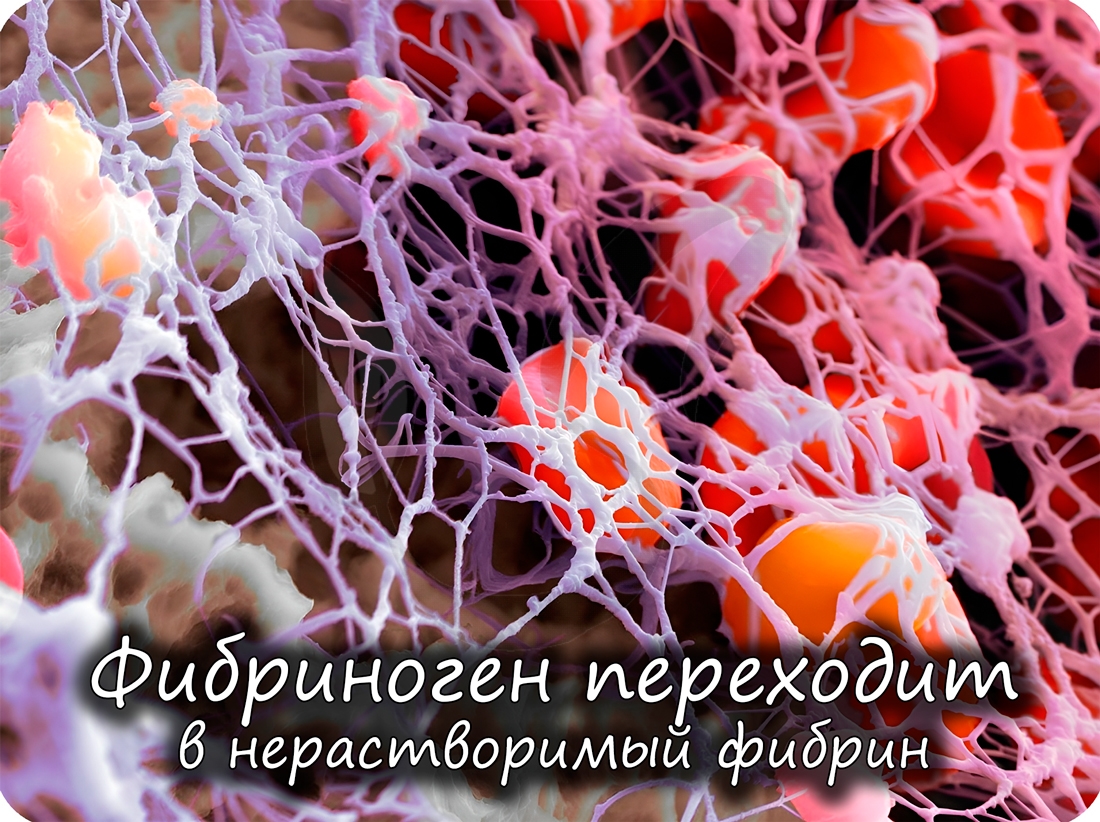
Помимо антител, защитную функцию выполняют также белки свертывающей системы крови (тромбин и фибриноген): они предохраняют организм от кровопотери.
При недостаточном питании в организме начинают окисляться молекулы белков. При расщеплении 1 г белков выделяется 17,6 кДж энергии.
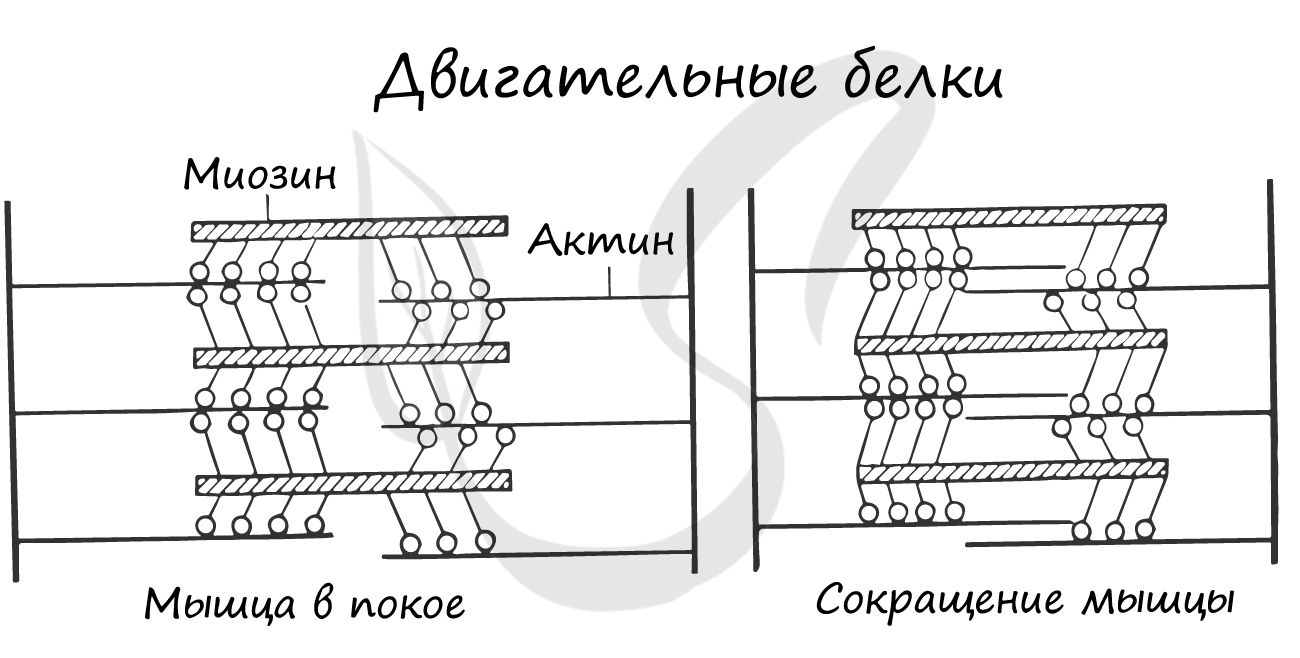
Двигательные белки, актин и миозин, на уровне саркомера обеспечивают сокращение мышц. При возбуждении мышечной ткани тонкие нити актина начинают тереться о толстые нити миозина, приводя к сокращению.
На поверхности мембраны белки образуют многочисленные рецепторы, которые, соединяясь с гормонами, приводят к изменению обмена веществ в клетке. Таким образом, гормоны реализуют воздействие на клетки органов-мишеней.
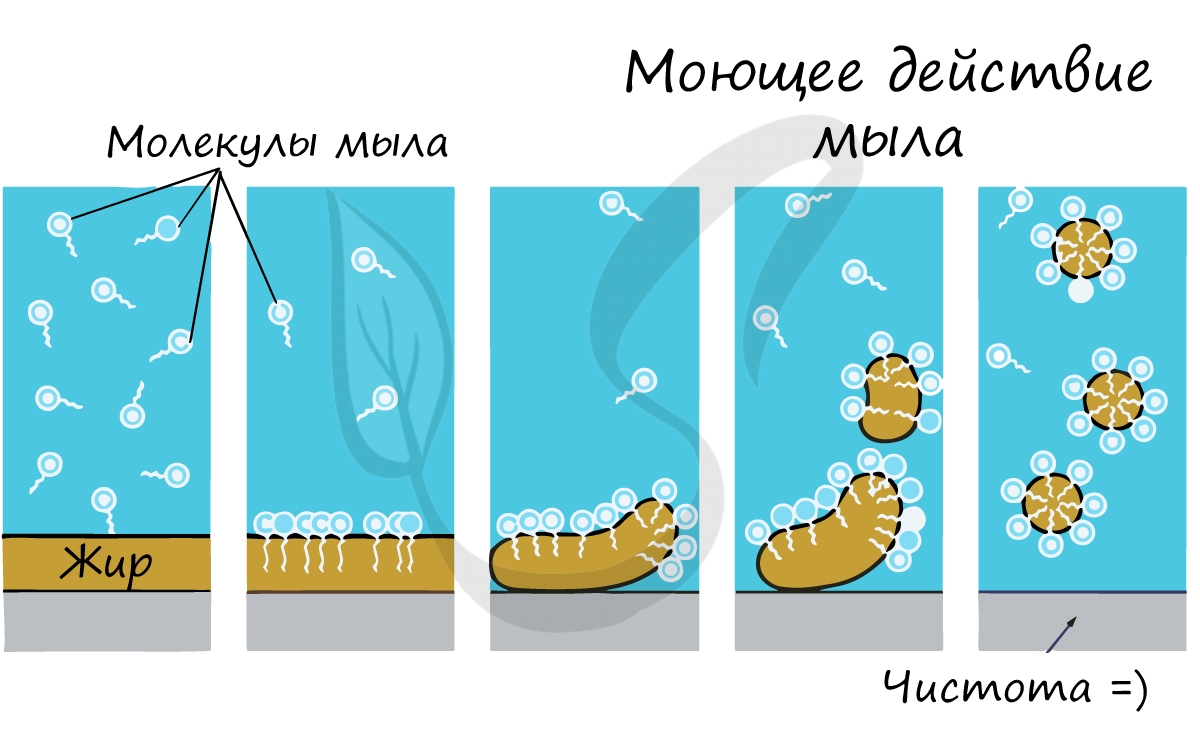
С химической точки зрения жиры являются сложными эфирами, образованными трехатомным спиртом глицерином и высшими карбоновыми кислотами (жирными кислотами). Среди их свойств надо выделить то, что они практически нерастворимы в воде. Вспомните, как тяжело смыть жир с рук водой.
Почему именно мыло смывает жир с рук? Дело в том, что молекула мыла повторяет свойства жира: одна часть ее гидрофобна, а другая гидрофильна. Мыло соединяется с молекулой жира гидрофобной частью, и вместе они легко смываются водой.
Жиры имеют способность накапливаться в клетках, расположенных в подкожно-жировой клетчатке, внутренних органах. Эти запасы являются резервом организма на случай голодания или при недостаточном питании.
В жирах также запасается вода: в 100 г жира содержится 107 мл воды. Многим пустынным животным (верблюдам) жировые запасы помогают длительное время обходиться без воды.
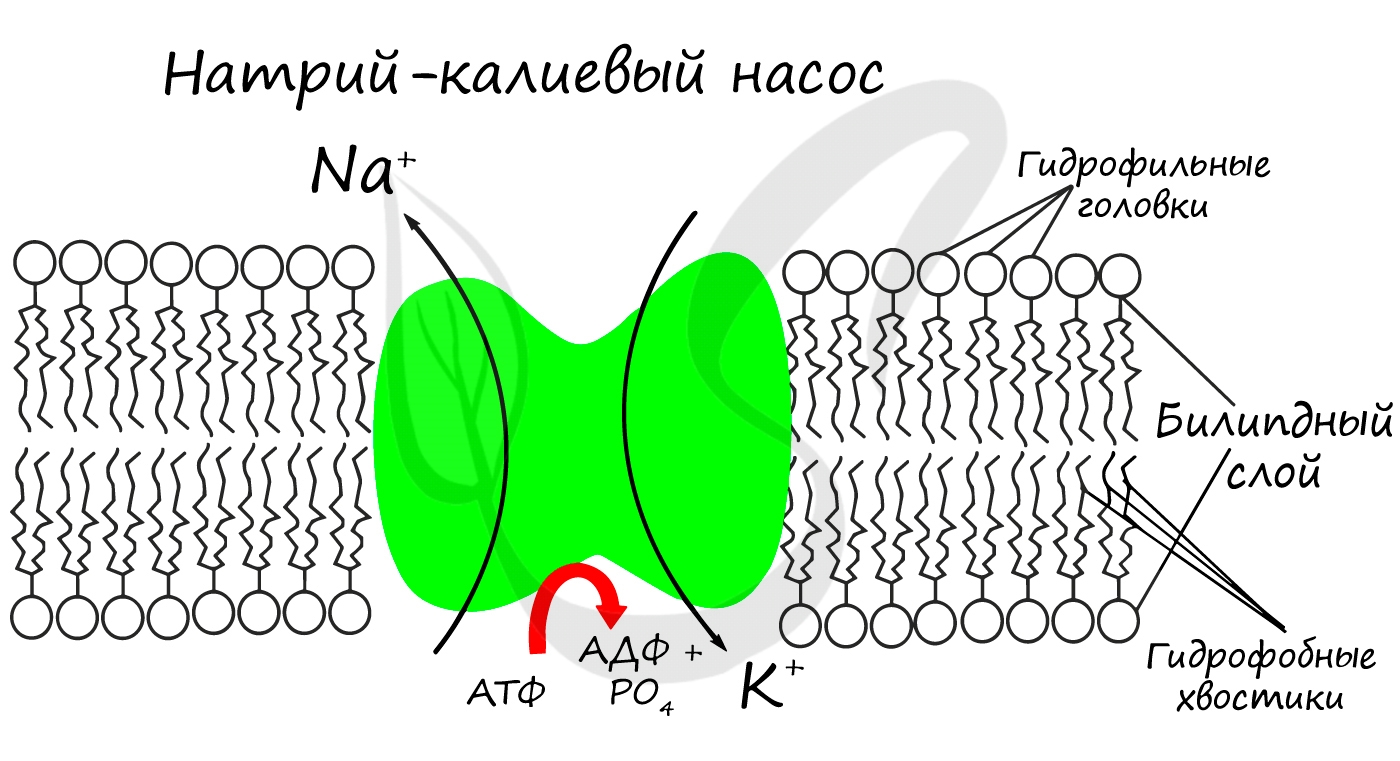
Жиры входят в состав биологических мембран клеток человека вместе с белками. Из фосфолипидов построены мембраны всех клеток органов и тканей!
Жиры обладают плохой теплопроводностью. Располагаясь в подкожно-жировой клетчатке, они образуют термоизолирующий слой. Особенно хорошо он развит у ластоногих (моржи и тюлени), китов, защищает их от переохлаждения.
Углеводы
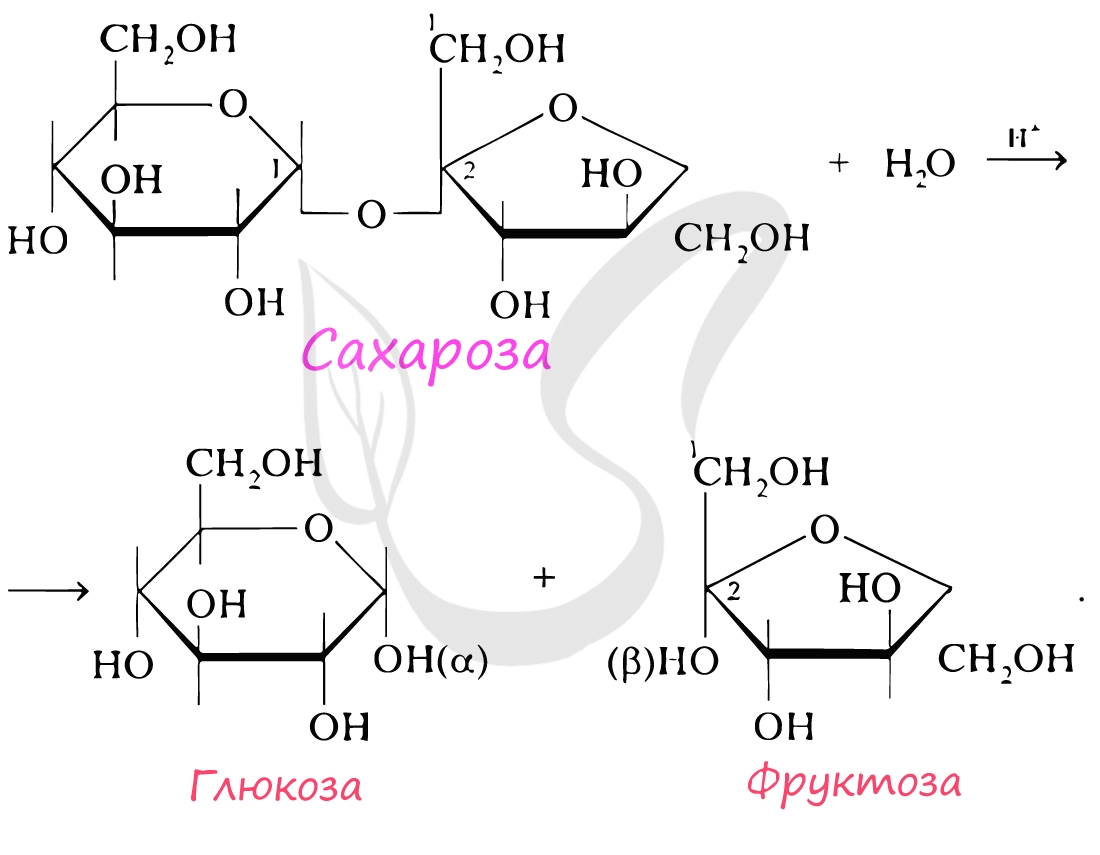
При гидролизе олигосахариды распадаются на моносахариды. В состав олигосахаридов может входить от 2 до 10 моносахаридных остатков. Если в состав олигосахарида входят 2 остатка моносахарида, то его называют дисахарид. К дисахаридам относятся сахароза, лактоза, мальтоза. При гидролизе сахароза распадается на глюкозу и фруктозу.
Это биополимеры, в состав которых входят сотни тысяч моносахаридов. Они обладают высокой молекулярной массой, нерастворимы в воде, на вкус несладкие.
В результате расщепления 1 г углеводов высвобождается 17,6 кДж энергии.
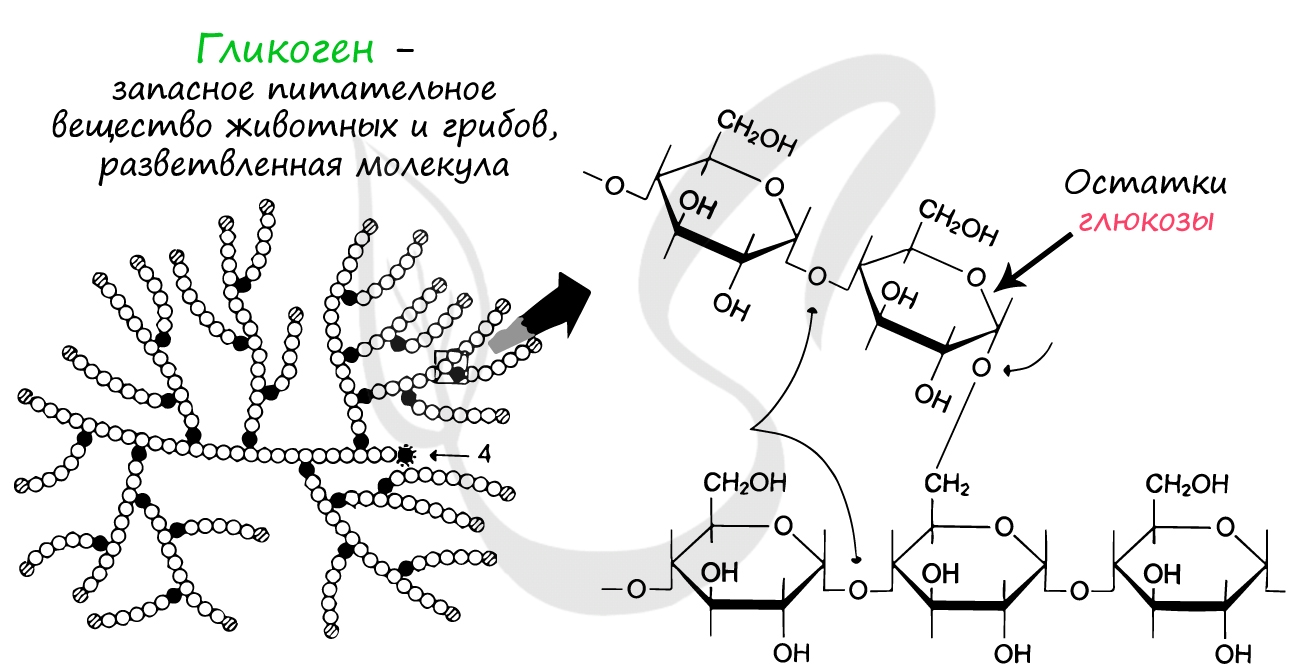
Запасным питательным веществом растений и животных соответственно являются крахмал и гликоген. Расщепление гликогена позволяет нам оставаться в сознании и быть активными между приемами пищи.
Гликоген представляет собой разветвленную молекулу, состоящую из остатков глюкозы. За счет больших размеров такая молекула хорошо удерживается в клетке, а ее разветвленность позволяет ферментам быстро отщеплять множество молекул глюкозы одновременно.
Существуют заболевания, при которых распад гликогена нарушается: в результате нейроны не получают глюкозы (источника энергии, соответственно не синтезируются и молекулы АТФ). Из-за этого становятся возможны частые потери сознания.
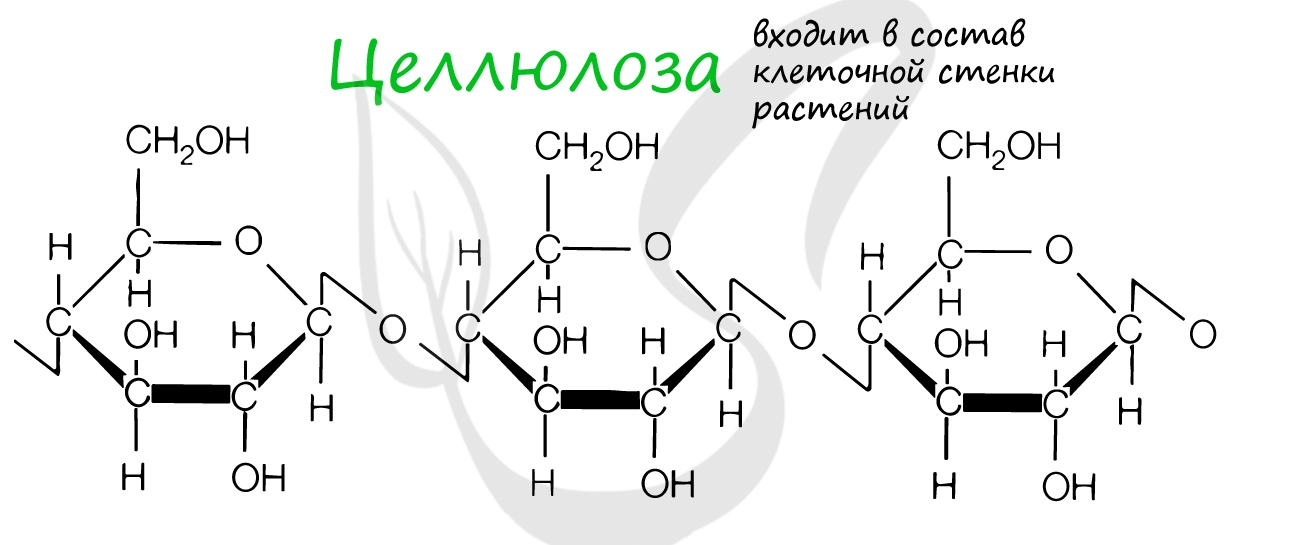
Целлюлоза входит в состав клеточных стенок растений, придавая им необходимую твердость. Хитин образует клеточную стенку грибов и наружный скелет членистоногих.
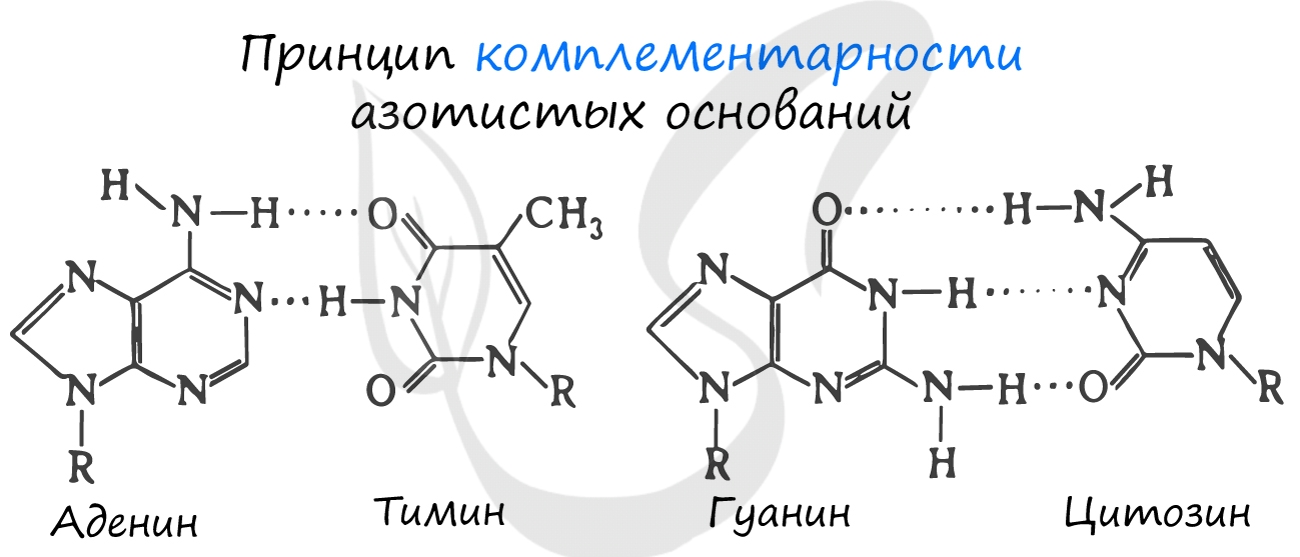
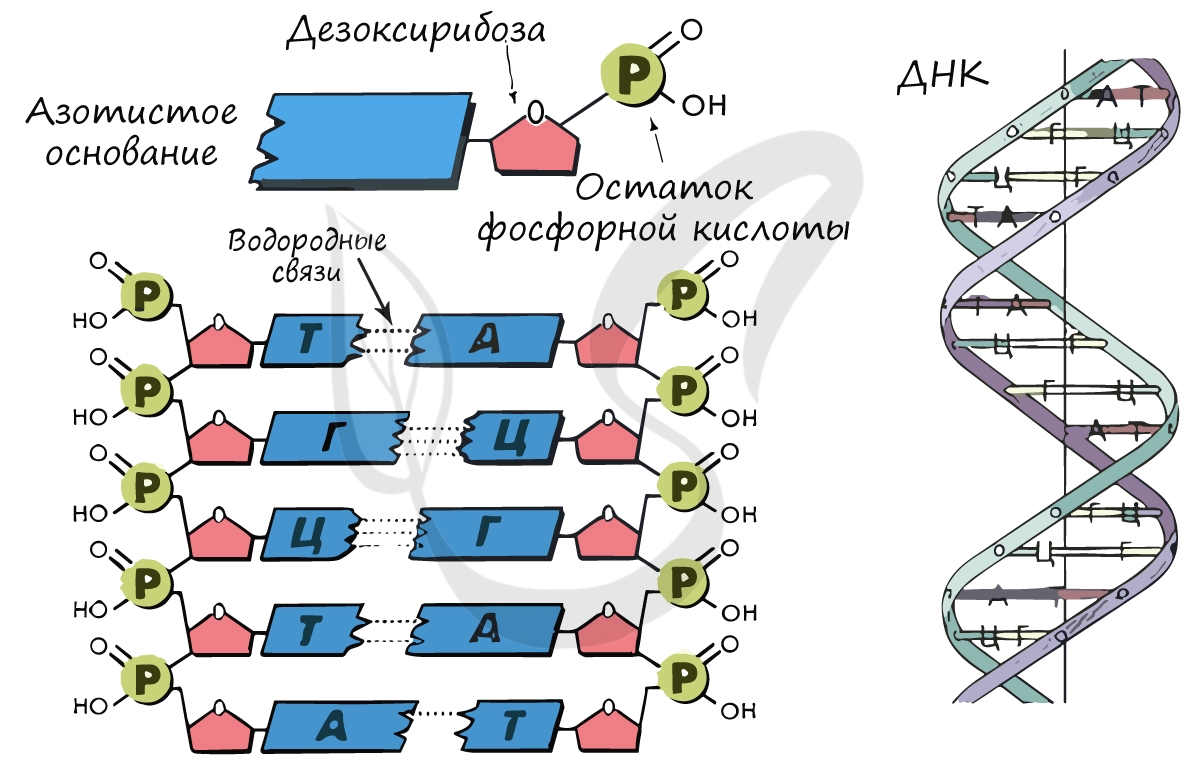
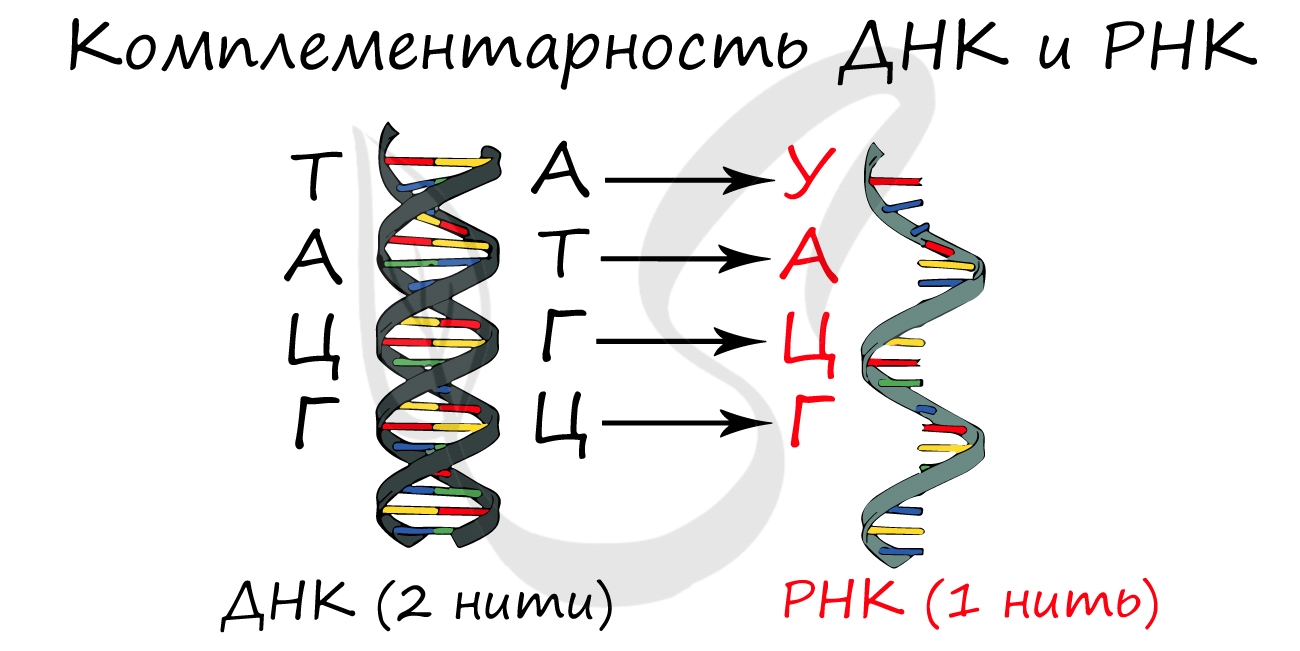
Нуклеиновые кислоты (от лат. nucleus — ядро)
Синтезируется в ядрышке. рРНК входит в состав малых и больших субъединиц рибосом. В процентном отношении рРНК составляет 80-90% всей РНК клетки.
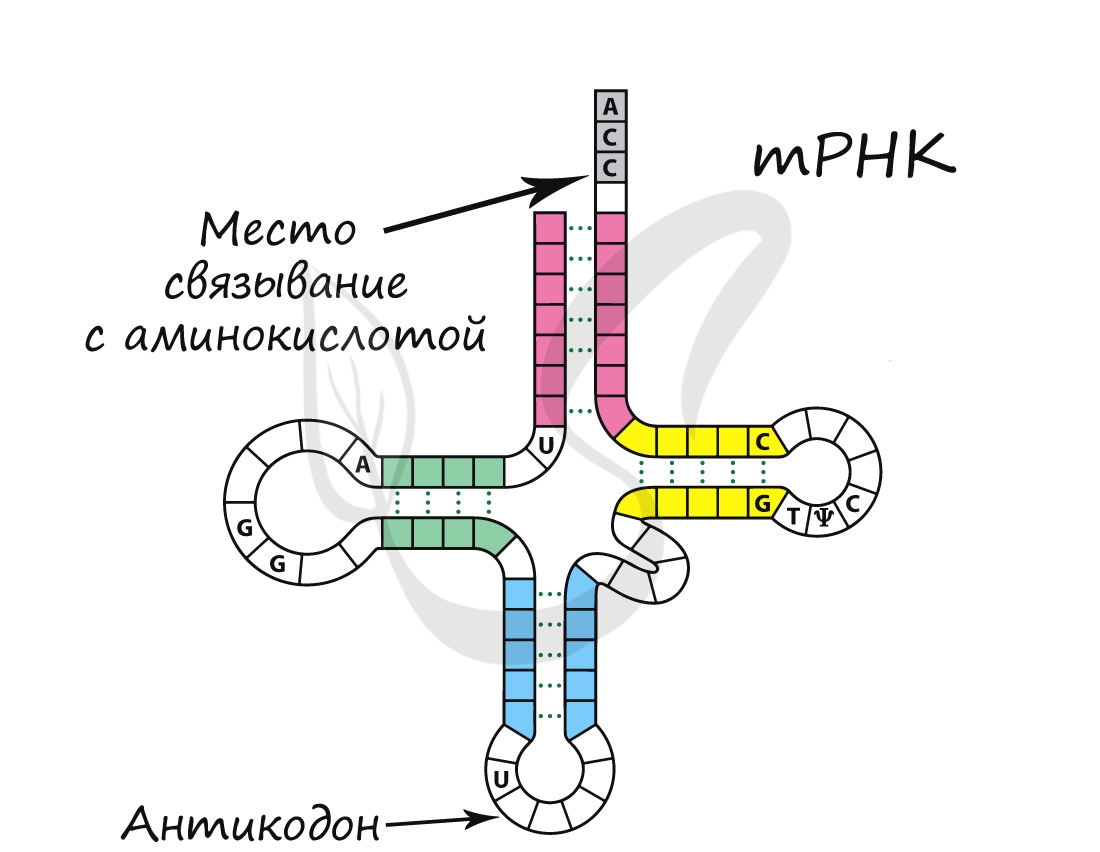
Обеспечивает транспорт аминокислоты к рибосоме во время синтеза белка. Благодаря этому становится возможным соединение аминокислот друг с другом, образуется белок. тРНК имеет характерную форму клеверного листа.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Химико-биологическое значение неорганических веществ
Дата публикации: 31.03.2018 2018-03-31
Статья просмотрена: 2113 раз
Библиографическое описание:
Майская, В. Д. Химико-биологическое значение неорганических веществ / В. Д. Майская, А. К. Абрамян, Л. В. Давыденко. — Текст : непосредственный // Юный ученый. — 2018. — № 2 (16). — С. 108-110. — URL: https://moluch.ru/young/archive/16/1205/ (дата обращения: 11.10.2021).
Химические элементы в организме человека и их роль
Вещества, необходимые для нормальной жизнедеятельности организма человека в больших количествах называются макроэлементами. Они составляют примерно 98 % всех минеральных веществ клетки. К макроэлементам относятся магний, алюминий, калий, кальций, натрий, железо, кислород, углерод, азот, водород, сера и фосфор. От 0,1 % до 2 % всех минеральных веществ клетки составляют микроэлементы. Микроэлементы: медь, цинк, молибден, кобальт, ванадий, хлор, бор, йод. Ультрамикроэлементы составляют около 0,01 % минеральных веществ клетки. Цезий, радий, бериллий, серебро, золото и ртуть относятся к ультрамикроэлементам.
Ионы натрия и калия обеспечивают проницаемость клеточных мембран для различных веществ, образование электрического заряда на мембранах нервных клеток, т. е. способность нервных клеток проводить импульс. Также эти ионы регулируют кровяное давление организма. При недостатке калия наблюдается повышенная кислотность желудка, аритмия сердечных сокращений. При дефиците натрия нарушается усвоение углеводов, возникает повышенное тромбообразование.
Катионы кальция обеспечивают нормальную свёртываемость крови, устойчивость организма к внешним неблагоприятным факторам, участвуют в передаче нервно-мышечного импульса. Кальций является основным элементом строения костей и зубов, регулирует состояние кожи, волос и ногтей, снимает спазмы сосудов. При дефиците кальция происходит замедление роста скелета, развитие атеросклероза, артрозов, остеохондрозов, гипертонии.
Катионы магния участвуют в процессах образования фибрина, то есть обеспечивают нормальную свёртываемость крови. Также магний нормализует работу мочевого пузыря и репродуктивных органов. Достаточное количество магния в организме предупреждает развитие сахарного диабета.
Функции цинка в организме: поддержание иммунитета, гормональная регуляция, участие в делении и росте клеток, обмене веществ. Также цинк необходим для нормального хода беременности и развития плода. При его недостатке возрастает риск выкидыша или рождения недоношенного ребёнка, ребенок может родиться с патологиями.
Железо входит в состав белка гемоглобина. Медь входит в состав окислительных ферментов, стимулирует кроветворение. Кобальт входит в состав витамина В12.
Золото нейтрализует различные виды болезнетворных бактерий, улучшает сердечно-сосудистую деятельность и стабилизирует иммунные процессы. Серебро уничтожает различные бактерии, снижает воспаление и ускоряет заживление ран.
Ртуть при попадании в микродозах в организм человека стимулирует выработку иммуноглобулинов, поддерживает на необходимом уровне содержание в организме Т-лимфоцитов, способных убивать раковые клетки. Но в больших дозах ртуть смертельно опасна для человека.
Сера является одним из главных химических элементов для живого организма, важнейшей составной частью белка, компонентом некоторых аминокислот. При её недостатке кожа значительно ухудшается и начинается раннее старение организма, волосы начинают выпадать и ломаться. Сера участвует в росте хрящевой и костной тканей, нейтрализует токсичные вещества.
Основная биологическая роль фосфора заключается в укреплении зубов и костной ткани. Также фосфор способствует делению клеток и участвует в регуляции нервной системы, значительно улучшает метаболизм, является источником энергии и регулирует кислотно-щелочной баланс.
Йод служит компонентом гормонов щитовидной железы и необходим для их синтеза. Также йод принимает участие в нервно-психическом развитии, регулирует белковый и жировой обмен, обмен энергии. Аналогично сере, при недостатке йода, начинается выпадение волос, снижается работоспособность человека.
Бром оказывает влияние на центральную нервную систему, эндокринную систему, участвует в работе желудочно-кишечного тракта. Также бром оказывает влияние на функции половых желез. При недостатке брома у людей начинаются серьезные проблемы со здоровьем: анемия, замедление роста, депрессия, снижение аппетита.
Углерод — основа жизни на Земле. Углерод участвует во всех процессах в организме и проявляется во всем живом. Служит для организма человека источником энергии. Углекислый газ (CO2) или углекислота участвует регуляция дыхания. При недостатке углерода становится труднее дышать, появляется тошнота, снижается активность, повышается утомляемость.
Применение неорганических веществ в медицине
В медицине популярны методы металлотерапии. Золото и серебро обладают антибактериальными и противовоспалительными свойствами. Препараты с добавлением железа употребляют при анемии. Аристотель называл медь прекрасным средством от отёчности, синяков и ушибов. Магний применяют в лечении язвы желудка. Соли лития применяют для лечения заболеваний, связанных с отложением солей в организме(подагры). Сульфат цинка (ZnSO4) применяют как вяжущее и антисептическое средство. 0,9 % раствор NaCl (более известный как физраствор) применяют для ингаляций, промываний слизистых оболочек, растворения медикаментозных препаратов, а также для восстановления водно-солевого баланса организма. Гипс (CaSO4×2H2O) применяют в травматологии. Металлы применяют для изготовления медицинских инструментов, приборов. Также металлы используются в протезировании. Например, из титана изготавливаются искусственные суставы, различные фиксаторы и даже клапаны сердца.
Неметаллы нашли широкое применение в медицинских препаратах. Соли серы (MgSO4, Na2SO4) применяются, как слабительные средства. Водород используют для приготовления перекиси водорода (H2O2) в виде трехпроцентного раствора. Углерод используют для изготовления различных имплантов и для получения «Активированного угля». При обморочных состояниях используют нашатырный спирт (NH4OH). Соединения брома используют в качестве успокоительного средства. Йод широко применяют для обработки ран. Фосфор используют для лечения заболеваний печени, сердца, желудка, применяют в стоматологии. Также неметаллы входят в состав многих витаминов.
Таким образом, неорганические вещества играют огромную роль для здоровой и полноценной жизни человека. Недостаток одних веществ и избыток других ведет к заболеваниям. Для предотвращения недостатка необходимых для организма элементов необходимо принимать витаминные комплексы, назначенные врачом.
Значение химических элементов для организма человека
» data-image-caption=»» data-medium-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2019/03/tablitsa-mendeleeva.png?fit=450%2C300&ssl=1″ data-large-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2019/03/tablitsa-mendeleeva.png?fit=829%2C550&ssl=1″ />
Наш организм, как известно, состоит из клеток, которые в свою очередь включают в себя органические и неорганические соединения, выполняющие разные функции. Неорганические химические элементы важны для слаженной работы всего организма, поэтому дефицит или избыток каждого из них может привести к образованию болезней.
В человеческом теле насчитывается 81 неорганических элементов. Все они обеспечивают функции жизнедеятельности:
Избыток, дефицит или дисбаланс микро- и макроэлементов соответственно обуславливает различного рода болезни, депрессию, усталость. Причинами этого являются – экологические проблемы, негативное влияние окружающей среды, вредная работа, плохой образ жизни, неполноценное питание.
Это заболевание называется микроэлементоз, ему подвергаются, в первую очередь дети и подростки, люди с хроническими болезнями эндокринной системы и ЖКТ, кормящие грудным молоком женщины.
Все химические элементы поделены на две группы: микроэлементы и макроэлементы. Вторые называют еще основными, которых в организм взрослого человека с массой 55 – 65 кг должно поступать около 100 мг в сутки.
К данной группе причисляют: хлор, углерод, кислород, водород, фосфор, натрий, магний, калий, кальций, сера, азот. Дневная норма потребления всех микроэлементов составляет приблизительно 70 мг. Это – железо, марганец, йод, цинк, бром, селен, медь, фтор, хром, кобальт, молибден.
Нужные вещества человек получает из пищи. Но их содержание в воде и продуктах питания замкнуто в цикл: почва – растения – животные – человек. Если грунт беден на некоторые элементы, значит и поступать в организм человека будет меньше нормы (даже если продукты качественные и натуральные). В этом случае требуется дополнительное потребление пищевых добавок.
Различные лекарственные формы поливитаминных комплексов включают в себя все виды витаминов и химических элементов, но имеют свои недостатки. Встречаются они в виде таблеток или капсул, а также в форме порошка, сиропа или шипучек.
Первая группа зачастую имеет неприятный запах и может раздражать слизистую желудка. Вторая в таком виде не всегда нравится взрослым, но хорошо давать детям. Покупая поливитамины, следует обращать внимание на состояние упаковки, потому что добавки, созданные на основе сульфатов, селенитов, карбонатов имеют плохую растворимость и усвояемость.
Лучше выбирать, содержащие биоорганические соли, например лактат магния, ведь в таком виде минералы включаются в обмен веществ. Также стоит обратить внимание, что чем больше вмещает в себя пищевая добавка элементов, тем сильнее будут одни вещества вытеснять другие:
Также, кроме необходимых элементов, в человеческий организм могут поступать и опасные для здоровья минералы.
Алюминий (Al). Он опасен тем, что его избыток поражает нервную систему, снижает память и способность к вниманию. Его дозы проникают через кожу с присыпками, тальком, кремами, дезодорантами, стойкой губной помадой. Значительно получаем Аl вместе с пищей, приготовленной в алюминиевой посуде.
Барий (Ba). Избыток этого элемента приводит к появлению слабости, одышки, выпадения волос, аритмии, гипертонии, рините, повреждению глазных век. Получают его люди, работающие в промышленности, а также те, кто часто проходил рентгеновское обследование с использованием барий сульфата.
Свинец (Pb). Это опасный тяжелый метал, который поражает кости, мышцы, мозг и почки. Из-за длительного воздействия страдает нервная система, у детей это проявляется гиперактивностью и потери ориентации в пространстве.