Что значит патогенность вируса
Патогенность вирусов
Смотреть что такое «Патогенность вирусов» в других словарях:
Иммунологи́ческие ме́тоды иссле́дования — диагностические методы исследования, основанные на специфическом взаимодействии антигенов и антител. Широко используются для лабораторной диагностики инфекционных и паразитарных болезней, определения групп крови, тканевых и опухолевых антигенов,… … Медицинская энциклопедия
Ви́рус — ( ы) (лат. virus яд) неклеточные формы жизни, обладающие геномом (ДНК или РНК), но лишенные собственного синтезирующего аппарата и способные к воспроизведению лишь в клетках более высокоорганизованных существ. ECHO вирусы (англ. enteric… … Медицинская энциклопедия
онкогенные вирусы — (опухолеродные вирусы), возбудители некоторых естественно возникающих, а также многих экспериментальных опухолей животных. К онкогенным вирусам относятся представители различных таксономических групп вирусов (например, аденовирусы), различающиеся … Энциклопедический словарь
Ви́русы — (лат. virus яд) мельчайшие микроорганизмы, не имеющие клеточного строения, белоксинтезирующей системы и способные к воспроизведению лишь в клетках высокоорганизованных форм жизни. Они широко распространены в природе, поражают животных, растения и … Медицинская энциклопедия
Инфекция — I Инфекция (позднелат. intectio заражение) сложный патофизиологический процесс взаимодействия макро и микроорганизма, имеющий широкий диапазон проявлений от бессимптомного носительства до тяжелых форм инфекционной болезни. Термин «инфекция»… … Медицинская энциклопедия
Ме́дленные ви́русные инфе́кции — группа вирусных заболеваний человека и животных, характеризующихся продолжительным инкубационным периодом, своеобразием поражений органов и тканей, медленным течением со смертельным исходом. Учение о М.в.и. основано на многолетних исследованиях… … Медицинская энциклопедия
Т-лимфотропный вирус человека — Т лимфотропный вирус человека … Википедия
ОНКОГЕННЫЕ ВИРУСЫ — (опухолеродные вирусы) возбудители некоторых естественно возникающих, а также многих экспериментальных опухолей животных. К онкогенным вирусам относятся представители различных таксономических групп вирусов (напр., аденовирусы), различающиеся по… … Большой Энциклопедический словарь
Генетическая инженерия — I Генетическая инженерия направление исследований в молекулярной биологии и генетике, конечной целью которых является получение с помощью лабораторных приемов организмов с новыми, в т.ч. не встречающимися в природе, комбинациями наследственных… … Медицинская энциклопедия
Тамифлю — Действующее вещество ›› Осельтамивир* (Oseltamyvir*) Латинское название Tamiflu АТХ: ›› J05AH02 Оcельтамивир Фармакологическая группа: Противовирусные средства Нозологическая классификация (МКБ 10) ›› J10 Грипп, вызванный идентифицированным… … Словарь медицинских препаратов
Что значит патогенность вируса
Вирусы являются внутриклеточными инфекционными агентами. Весь репликативный цикл вируса осуществляется с исполь зованием метаболических и генетических ресурсов клеток. Поэтому патогенез вирусных инфекций, в первую очередь, следует рассматривать на молекулярном и клеточном уровнях (В.И. Покровский, О.И. Киселев, 2002). Вместе с тем, инфекционный процесс, вызванный вирусами, развивается в пределах того или иного органа или ткани, так как большинство вирусов обладают достаточно высокой органной или тканевой тропностью. Поэтому характер развития внутритканевых процес сов при вирусных инфекциях, с одной стороны, определяется, как правило, цитопатическим действием вируса на клетки данной ткани и органа, а с другой стороны, реакцией внутритканевых и органных систем защиты от вирусной инфекции. Последние не редко носят деструктивный характер и усугубляют течение забо левания и его последствия. Поэтому понимание патогенеза вирусных инфекций представляется исключительно важным для создания рациональных схем лечения, основанных на гармоничном сочетании симптоматического лечения и противовирусной химиотерапии.
В клинической практике важное значение имеют процессы, вызванные вирусной инфекцией, виремией – (степень «вирусной нагрузки» прямо коррелирует с явлениями общего токсикоза, тяжестью состояния пациента, лихорадкой; тесным взаимодействием с иммунной системой), реакция которой в значительной степени определяет характер течения инфекционного процесса и его исход; присоединением бактериальной инфекции и развитием осложнений. Смешанные инфекции представляют собой опасный путь развития процесса.
Стадии репликативного цикла вируса гриппа представлены на рис. 1. Такой же репликативный цикл свойствен большинству РНК- и ДНК-содержащих вирусов, кроме тех, кото рые обладают особыми механизмами хронизации процесса, латенции и способностью к интеграции в клеточный геном (например, ВИЧ, гепатит С, вирус папилломы и.т.). Ключевыми стадиями репликативного цикла вируса являются проникновение в клетки, декапсидация, активация процессов транскрипции и трансляции, собственно репликация вирусного генома и созревание зрелых вирусных частиц с выходом нового потомства инфекционного вируса.
Для проникновения вируса в клетку, необходимо: высокое сродство к вирусоспецифическому рецептору; множественность рецепторов; эффективность слияния вируса с клетками при инфицировании; способность к образованию синцития, к образованию гигантских синпластов, состоящих из множества слившихся клеток, в которых вирусный нуклеопротеид без эндоцитоза беспрепятственно переходит от одной зараженной клетки к множеству других через цитоплазму.
Такими свойствами из респираторных вирусов обладает респираторно-синцитиальный вирус, а среди ретровирусов – вирус иммунодефицита человека.
Стадии жизненного цикла вируса гриппа и соответствующие ингибиторы репродукции в известной степени могут быть экстраполированы на многие другие вирусы, за исключением тех, жизненный цикл которых включает интеграцию в клеточный геном. В процессе репликации вирусов обычно происходит селективная блокада трансляции клеточных мРНК и активация экспресси клеточных генов, кодирующих провоспапительные лимфокины. Многократные раунды репликации вирусного генома приводят к истощению энер гетических ресурсов клеток и пула предшественников азотистых оснований. Повышенное содержание провоспалительных лимфокинов приводит к развитию воспалительной реакции и локально му генерированию свободных радикалов, оказывающих, в свою очередь, повреждающее действие на клетки и ткани через перекисное окисление липидов клеточных мембран, инактивацию жизненно важных ферментов. Поэтому одним из важнейших факторов патогенности вирусов является их репликативный потенциал: чем активнее происходит репликация, тем сильнее цитопатическое действие вирусов на клетки и пораженную ткань (орган).
Значительный вклад в цитопатическое действие вирусов вносит репродукция вирусов в митохондриях, что сопровождается нарушением функций этих органоидов, падением продукции АТФ и индукцией опосредованного митохондриями пути апоптоза.
Впервые возможность репродукции вирусов в митохондриях была доказана выдающимся отечественным вирусологом В.М. Ждановым. Узкий тропизм вирусов, в известной степени, спасителен для организма, так как инфекционный процесс ограничен одним органом.
Это обстоятельство позволяет, проводит рациональную симптоматическую терапию, направленную на защиту данной ткани или органа и ориентировать противовирусные средства в данный орган, например, легкие.
Возбудители гриппа относятся к семейству ортомиксовирусов (Orthomyxo-viridae) и являются пневмотропными вирусами. Схематическое строение вируса гриппа представлено на рис. 2.1. Геном вируса складывается из 8-ми фрагментов однонитчатой РНК, которые кодируют
10 вирусных белков. Фрагменты РНК имеют общую белковую оболочку, соединяющую их, образуя антигенно-стабильный рибонуклеопротеид (S-антиген), который определяет принадлежность вируса к серотипу А, В или С. Снаружи вирус покрыт двойным липидным слоем с внутренней стороны которого находится слой мембранного белка.
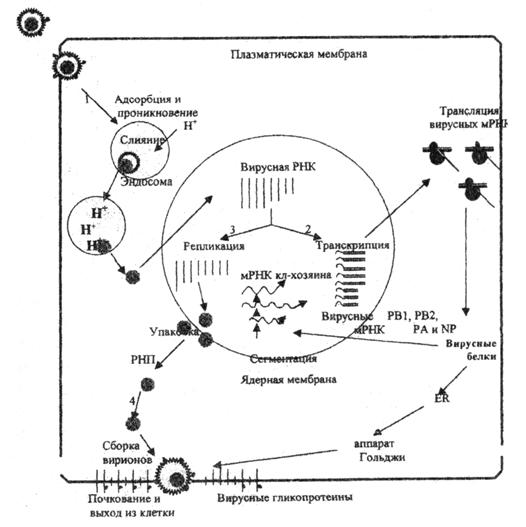
Рис. 1. Репликативный цикл вируса гриппа (В.И.Покровский, О.И.Киселев, 2002)
Представлены 4 основные фазы репликативного цикла вируса гриппа: 1 – адсорбция и проникновение вируса в клетку хозяина; 2 – транскрипция вирусной РНК и трансляция вирусных белков; 3 – репликация вирусной РНК и 4 – самосборка вирионов и последующий выход их из клетки.
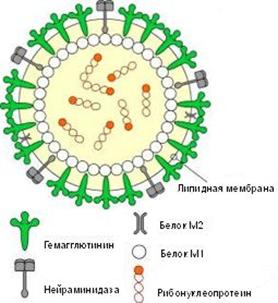
Над оболочкой вируса поднимаются два типа «шипов» (гликопротеины) – гемаглютинин (Н) и нейраминидаза (N) – поверхностные антигены вируса гриппа. Гемаглютинин – полипептид, назван так благодаря способности гемолизировать эритроциты. Он имеет высокую изменчивость и иммуногенность, обеспечивая прикрепление вируса к клетке. Нейраминидаза – этогликопротеидный комплекс, который определяет ферментативную активность, отвечает за способность вирусной частицы проникать в клетку хозяина и выходить из нее после размножения.
Рис. 2. Схематическое строение вируса гриппа
Гемаглютинин и нейраминидаза являются факторами агрессии вируса гриппа. Интенсивность интоксикации при гриппе определяется свойствами гемаглютинина, а нейраминидаза обладает выраженным иммунодепресивным действием. Оба поверхностных антигена характеризуются выраженной способностью к изменчивости, в результате чего появляются новые антигенные варианты вируса. Гемаглютинины 1, 2, 3 типов и нейраминидазы 1, 2 типов содержат вирусы, которые поражают человека. Другие антигены характерные для вирусов гриппа животных (свиней, собак, лошадей, многих видов птиц и др.).
Вирусы гриппа А. Эти возбудители более вирулентны и контагиозны, чем вирусы гриппа В и С. Это обусловлено тем, что вирус А содержит 2 типа нейраминидазы (N1, N2) и 4 –гемаглютинина (H0, H1, H2, H3); вирус В – 1 и 1 соответственно, поэтому он имеет лишь антигенные варианты внутри одного серотипа; вирус С содержит только гемаглютинин и не содержитнейраминидазу, но он имеет рецептор, который разрушает энзим. Вирусу С не свойственная изменчивость.
Одновременно циркулируют и имеют эпидемическое распространение 2 подтипа вируса гриппа А H3N2 и H1N1. На сегодняшний день во всем мире доминирует вариант А/Сидней/05/97, А/Берн/07/95 и А/Пекин/262/95. Характерной чертой современных вирусов гриппа А (H3N2) является изменение ряда их биологических свойств: тяжело размножаются в куриных эмбрионах, не агглютинируют эритроциты кур, взаимодействуют только с эритроцитами человека или морской свинки, имеют низкую иммуногенную активность.
Вирусы гриппа В выделяются только от людей. По вирулентности и эпидемиологической значимости они уступают вирусам гриппа А. По антигенным свойствам гемаглютинин инейраминидазу вируса В можно разделить на 5 подтипов. Их изменчивость носит более постепенный и медленный характер, что объясняет эпидемиологические особенности вируса гриппа В (эпидемии возникали 1 раз в 3-4 года до 1988 г.). В мире сейчас циркулируют 2 варианта вируса гриппа В: В/Пекин/184/93 (Европа, Америка, Африка, Австралия) и В/Виктория/2/87 (Юго-Восточная Азия). Характерной чертой современных вирусов гриппа А и В является их высокая чувствительность к ингибиторам гемаглютинирующей и инфекционной активности, которые содержатся в сыворотке крови нормальных животных.
Для вирусов гриппа С характерна значительно большая стабильность антигенных и биологических свойств. По ряду биологических характеристик эти возбудители отличаются от других представителей семейства ортомиксовирусов. Им присуща низкая репродуктивная активность в разных клеточных системах и наличие других, чем у вирусов гриппа А и В, рецепторов на поверхности эритроцитов. Рецептор-деструктирующая активность связана не с нейраминидазой, как у вирусов гриппа А и В, а с ферментом нейраминат-0-ацетилестеразою.
Сложность этиологии усиливают факты выделения от людей вирусов, которые не свойственные человеку. Гены вируса гриппа (H5N1), выделенные в 1997 году от человека в Гонконге, оказались подобными генам птичьего вируса, который преодолел межвидовой барьер. Оказалось, что человеческие и птичьи вирусы гриппа были реасортантами (рекомбинантные штаммы), которые получили внутренние гены РВ1 и РВ2 от перепелиного вируса гриппа А (H9N2) – штаммы А/перепел/Гонконг/61/97.
Вирус гриппа не растет на обычных питательных средах. Его можно выделить из материала, который получен от больного в первые дни болезни (смывы из носоглотки, мокроты), путем заражения культур или клеток куриных эмбрионов.
Традиционно считалось, что человеческий организм освобождается от возбудителя в ближайшие дни после выздоровления. Однако постепенно накапливались косвенные свидетельства, которые опровергают эту точку зрения. И в 1985 г. были получены прямые доказательства формирования длительной персистенции вируса гриппа. У одного человека удалось многократно выделять вирус гриппа в течение 9-ти месяцев и дольше. Возможность пожизненной персистенции вируса в организме человека продолжает изучаться.
1. Грипп и другие респираторные вирусные инфекции / под ред. О.И. Киселева, И.Г. Мариничева, А.А. Сомининой. – СПб. – 2003.
2. Дриневский В.П., Осидак Л.В., Цыбалова Л.М. Острые респираторные инфекции у детей и подростков // Практическое руководство под редакцией О.И. Киселева. – Санкт-Петербург. – 2003.
3. Железникова Г.Ф., Иванова В.В., Монахова Н.Е. Варианты иммунопатогенеза острых инфекций у детей. – Санкт-Петербург. – 2007. – 254 с.
4. Ершов Ф.И. Грипп и другие ОРВИ // Антивирусные препараты. Справочник. – М., 2006. –С. 226-247.
5. Ершов Ф.И., Романцов М.Г. Антивирусные средства в педиатрии. – М., 2005. – С.159-175.
6. Ершов Ф.И., Киселев О.И. Интерфероны и их индукторы (от молекул до лекарств). – М., 2005. – С. 287-292.
7. Иванова В.В. Острые респираторно-вирусные заболевания // Инфекционные болезни у детей. – М., 2002.
8. Онищенко Г.Г., Киселев О.И., Соминина А.А. Усиление надзора и контроля за гриппом как важнейший элемент подготовки к сезонным эпидемиям и очередной пандемии. – М., – 2004. – С.5-9.
9. Об утверждении стандарта медицинской помощи больным гриппом, вызванным идентифицированным вирусом гриппа (грипп птиц) // Приказ Минздравсоцразвития №460 от 07.06.2006 г.
10. Романцов М.Г., Ершов Ф.И. Часто болеющие дети: Современная фармакотерапия. – М., 2006. – 192 с.
11. Стандартизированные принципы диагностики, лечения и экстренной профилактики гриппа и других острых респираторных инфекций у детей / под ред. О.И. Киселева. – СПб. – 2004. – С. 82-95.
12. Лекарственные средства в фармакотерапии патологии клетки / под редакцией Т.Г. Кожока.-М., 2007.
Вирусы и человек. Противостояние длиной в тысячелетия
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Каждый год, с завидной регулярностью, человечество сталкивается с большой и малоизученной опасностью. Непонятно откуда и по каким причинам вдруг появляются новые, неизвестные ранее виды вирусов, которые угрожают всем нам эпидемиями и гибелью большого количества людей. Так, появившийся весной 2015 года в Южной Корее ближневосточный респираторный коронавирусный синдром (коронавирус MERS) застал врасплох южнокорейские власти и заставил их принимать срочные эпидемиологические меры. Смертность от MERS составила более 35%, и, как сказано в бюллетене ВОЗ, «в настоящее время не существует ни конкретного лечения, ни вакцины от этой болезни». Поэтому интерес исследователей к вирусам вполне объясним и имеет жизненно важное значение.
Обратите внимание!
Эта работа опубликована в номинации «Лучшая статья по иммунологии» конкурса «био/мол/текст»-2015.
Спонсором номинации «Лучшая статья о механизмах старения и долголетия» является фонд «Наука за продление жизни». Спонсором приза зрительских симпатий выступила фирма Helicon.
Спонсоры конкурса: Лаборатория биотехнологических исследований 3D Bioprinting Solutions и Студия научной графики, анимации и моделирования Visual Science.
Эволюция и происхождение вирусов
Как теперь известно ученым, вирусы окружают нас повсюду в живой природе. И каждая клетка каждого живого организма несет в себе следы прошлых встреч с ними. Генетическое разнообразие вирусов, их умение меняться и приспосабливаться, а также их огромное количество в природе — поражают. Предполагается, что общее число вирусных частиц на порядок выше количества всех клеток всех организмов на Земле [1]. Миллионы лет назад ретроэлементы и ретровирусы участвовали в эволюции, выступая в качестве генетического резервуара для создания новых генов и усложнения видов. Этот вопрос подробно исследовали и нашли массу подтверждающих фактов российские генетики из Института биоорганической химии РАН (академик Е.Д. Свердлов, А.А. Буздин и их коллеги) [2, 3]. И сейчас вирусы могут выступать одним из «орудий» эволюции, регулируя численность и жизнеспособность популяций*.
* — О том, как вирусы могли участвовать в эволюции живых организмов, рассказывают статьи «Вирусные геномы в системе эволюции» и «Гигантские вирусы: 4-й домен жизни?» [4, 5].
Когда именно на Земле появились первые вирусы, наука точно сказать не может. Сегодня существует несколько гипотез происхождения вирусов. Один из самых авторитетных ученых-вирусологов, академик РАМН В.М. Жданов, особо выделяет три из них. Согласно первой, вирусы могут быть потомками бактерий или других одноклеточных организмов, претерпевших дегенеративную эволюцию. То есть бактерии или одноклеточные по каким-то причинам вместо обычного развития в сторону усложнения, потеряли часть структур и «упростились» до вирусов. Согласно второй гипотезе, вирусы появились еще до образования первых живых клеток и являются потомками древних доклеточных форм жизни. Возможно, поначалу они обладали автономностью, но затем перешли к паразитическому способу жизни, используя для своего размножения другие формы. Согласно третьей гипотезе, вирусы произошли от клеточных генетических структур — ретротранспозонов, — способных передвигаться в геномах [6].
В 2007 году сотрудники биологического факультета МГУ Л. Нефедова и А. Ким описали, как мог появиться один из видов вирусов — ретровирусы. Они провели сравнительный анализ геномов дрозофилы D. melanogaster и ее эндосимбионта (микроорганизма, живущего внутри дрозофилы) — бактерии Wolbachia pipientis. Полученные данные показали, что эндогенные ретровирусы группы gypsy могли произойти от мобильных элементов генома — ретротранспозонов. Причиной этому стало появление у ретротранспозонов одного нового гена — env, — который и превратил их в вирусы. Этот ген позволяет вирусам передаваться горизонтально, от клетки к клетке и от носителя к носителю, чего ретротранспозоны делать не могли. Именно так, как показал анализ, ретровирус gypsy передался из генома дрозофилы ее симбионту — вольбахии [7]. Это открытие упомянуто здесь не случайно. Оно нам понадобится для того, чтобы понять, чем вызваны трудности борьбы с вирусами.
Из давних письменных источников, оставленных историком Фукидидом и знахарем Галеном, нам известно о первых вирусных эпидемиях, возникших в Древней Греции в 430 году до н.э. и в Риме в 166 году. Часть вирусологов предполагает, что в Риме могла произойти первая зафиксированная в источниках эпидемия оспы. Тогда от неизвестного смертоносного вируса по всей Римской империи погибло несколько миллионов человек [8]. И с того времени европейский континент уже регулярно подвергался опустошающим нашествиям всевозможных эпидемий — в первую очередь, чумы, холеры и натуральной оспы. Эпидемии внезапно приходили одна за другой вместе с перемещавшимися на дальние расстояния людьми и опустошали целые города. И так же внезапно прекращались, ничем не проявляя себя сотни лет.
Вирус натуральной оспы стал первым инфекционным носителем, который представлял действительную угрозу для человечества и от которого погибало большое количество людей. Свирепствовавшая в средние века оспа буквально выкашивала целые города, оставляя после себя огромные кладбища погибших. В 2007 году в журнале Национальной академии наук США (PNAS) вышла работа группы американских ученых — И. Дэймона и его коллег, — которым на основе геномного анализа удалось установить предположительное время возникновения вируса натуральной оспы: более 16 тысяч лет назад. Интересно, что в этой же статье ученые недоумевают по поводу своего открытия: как так случилось, что, несмотря на древний возраст вируса, эпидемии оспы не упоминаются в Библии, а также в книгах древних римлян и греков [9]?
Новосибирские микробиологи Игорь Бабкин и Ирина Бабкина из Института химической биологии и фундаментальной медицины РАН (ИХБФМ СО РАН), исходя из результатов геномного анализа называют более близкую к нам дату возникновения вируса натуральной оспы — 3000–4000 лет назад [8]. Место возникновения — восточная Африка. Но, так или иначе, вырвавшись с африканского континента около двух тысяч лет назад, вирус оспы начал свое «черное» шествие по миру, уложив в могилу огромное количество людей на всех континентах, и просуществовал до 1980 года, когда человечество объединенными усилиями его победило. Сегодня вирус натуральной оспы под строгим контролем сохраняется в двух лабораториях: в Центре по контролю заболеваний (CDC, Атланта, США) и в Научном центре вирусологии и биотехнологии «Вектор» (Кольцово, Россия) *.
* — Это официальные хранилища, а по поводу неофициальных спекулируют и обыватели, и авторитетные вирусологи, работающие под шефством ФБР. Так нужно ли уничтожать «легальные» образцы вирусов оспы? Почему ответ на этот вопрос неоднозначен, пытается разобраться американский журналист Ричард Престон в своей документальной книге «Демон в морозильной камере» [10]. Делает он это частично через призму событий, сопутствующих знаменитой рассылке писем со спорами сибиреязвенных бактерий в 2001 году («биомолекула» в одной из врезок затрагивала эту тему). Как реагировали всевозможные государственные структуры, как шаг за шагом продвигалось расследование ФБР, что творилось в недрах главного защитника населения США от биотеррористов — USAMRIID (Форт Детрик). Автор описывает вирусы оспы и случаи, связанные с их «оживлением» и экспериментальным заражением животных, шпионские скандалы, последние вспышки натуральной оспы и историю глобальной победы над ней в конце 70-х. Однако Престон (как и некоторые компетентные герои его расследования) не страдает избытком оптимизма, небезосновательно считая, что мечта о тотальном избавлении от оспы не сбылась: хотя нам удалось истребить инфекцию в природе, «мы не смогли вырвать вирус из человеческого сердца». Основанием для этой мысли, помимо прочего, послужили сведения, подкрепляющие потенциальную возможность искусственного создания супервирусов оспы, а также. детская рука с типичными оспенными поражениями, найденная в 1999 году.
Страхи-страхами, а престонские демоны волей-неволей и на благо науки работают — по крайней мере, у нас. В конце 90-х в микробиологических кулуарах ходила байка о том, что кое-какие — не известные широкой общественности — биологические институты выжили благодаря содержимому своих холодильников: чиновников удалось «разжалобить» только страшилкой об апокалиптических последствиях отключения электроэнергии в институте. Ведь из размороженных холодильников всенепременно выскочат бациллы сибирской язвы! — Ред.
Строение вирусов и иммунный ответ организма
В поле зрения ученых вирусы попали в начале XVIII века. Тогда европейские врачи заинтересовались феноменом непроизвольной вакцинации: люди, зараженные легкой формой оспы — коровьей, — были не подвержены оспе натуральной, то есть человеческой. Прорыв в этом вопросе произошел в 1796 году, когда английский врач и ученый Эдвард Дженнер (рис. 1, справа) публично произвел первое «цивилизованное» и безопасное оспопрививание [11]. После этого прошло без малого двести лет, когда в 1892 году впервые был описан вирус. Звание первооткрывателя вирусов по праву принадлежит российскому микробиологу Дмитрию Иосифовичу Ивановскому (рис. 1, слева), который в конце XIX века сумел описать вирус, вызывающий мозаичную болезнь растения табака. И вслед за этим открытием началось лавинообразное изучение вирусов, которые не перестают нас удивлять и преподносить неожиданные сюрпризы.
Рисунок 1. Первооткрыватель вирусов Д.И. Ивановский (1864–1920) (слева) и английский врач Эдвард Дженнер (справа).
После детального изучения вирусов, которые получили свое название от латинского слова virus (яд), стало известно, как именно они устроены. Полноценная вирусная частица — вирион — состоит из белковой оболочки (капсида) и внутреннего содержимого: нуклеиновой кислоты, «хранящей» вирусные гены (рис. 2, 3). У некоторых вирусов капсид покрыт дополнительными слоями из белков и липидов. По тому, какая именно нуклеиновая кислота содержится в вирусе, их делят на два больших вида: ДНК- и РНК-вирусы*.
Рисунок 2. Строение вируса иммунодефицита человека (ВИЧ). Диаметр частицы ВИЧ составляет примерно 100–120 нм. gp120 — поверхностный белок, молекулы которого формируют «шляпку гриба». Именно этот белок взаимодействует с антителами и рецептором клетки-мишени (gp — гликопротеин, 120 — масса белка в дальтонах). gp41 — белок, формирующий «ножку гриба», встроенную в липидную мембрану вируса. р24 — внутренний белок, две тысячи молекул которого составляют капсид вируса (кор), имеющий форму усеченного конуса. р17 — матриксный белок, образующий слой толщиной 5–7 нм между внешней оболочкой и капсидом. Интеграза, ревертаза и протеаза — ферменты, необходимые для жизненного цикла вируса. РНК (2 копии) — хранилище генетической информации (ВИЧ — ретровирус). Генетический аппарат ВИЧ-1, связанный с нуклеокапсидным белком p7, имеет длину около 10 тыс. нуклеотидов и содержит девять генов. Рисунок с сайтов visual-science.com и «Википедии».
Почти все известные науке вирусы имеют свою специфическую мишень в живом организме — определенный рецептор на поверхности клетки, к которому и прикрепляется вирус. Этот вирусный механизм и предопределяет, какие именно клетки пострадают от инфекции. К примеру, вирус полиомиелита может прикрепляться лишь к нейронам и потому поражает именно их, в то время как вирусы гепатита поражают только клетки печени. Некоторые вирусы — например, вирус гриппа А-типа и риновирус — прикрепляются к рецепторам гликофорин А и ICAM-1, которые характерны для нескольких видов клеток. Вирус иммунодефицита избирает в качестве мишеней целый ряд клеток: в первую очередь, клетки иммунной системы (Т-хелперы, макрофаги), а также эозинофилы, тимоциты, дендритные клетки, астроциты и другие, несущие на своей мембране специфический рецептор СD-4 и CXCR4-корецептор [13–15].
Рисунок 3. Генетическая организация вируса ВИЧ-1. (+)РНК-геном вируса содержит гены, ответственные за синтез белков, выполняющих структурные, ферментативные и регуляторные функции. Это гены gag, env и pol, имеющиеся у всех известных ретровирусов и кодирующие структурные белки оболочки вируса (gag, env), а также ферменты: ревертазу, интегразу и протеазу (ген pol). Оставшиеся шесть генов — vpr, vpu, vif, tat, rev, nef — так или иначе участвуют в жизненном цикле ВИЧ-1, кодируя регуляторные белки и подавляя активность иммунных клеток. Два вида вируса иммунодефицита человека (ВИЧ-1 и ВИЧ-2) различны по составу генов: у ВИЧ-2 нет гена vpu, зато есть ген vpx. Рисунок с сайта www.zdrav.kz.
Что происходит после того, как вирус попадает внутрь организма? Уже в слизистой оболочке иммунные клетки (макрофаги) поглощают часть вирионов. Вслед за этим, когда вирус проникает в кровь, другие иммунные клетки — Т-хелперы — дают стимулирующий сигнал «убийцам» вирусов: B-лимфоцитам и Т-киллерам. Операция по уничтожению вируса переходит в следующую фазу. Активированные B-лимфоциты образуют антитела, которые находят свободные антигены вирусов и связываются с ними. Такой тандем (вирусный антиген — антитело) захватывается и уничтожается макрофагами. Те вирусы, которые сумели ускользнуть от антител и макрофагов и внедриться в клетки, уничтожаются вместе с пораженными клетками Т-киллерами. И завершающий этап иммунной реакции: клетки Т-супрессоры гасят активность иммунного ответа, прекращая агрессивные действия Т-киллеров и B-лимфоцитов, чтобы те, разбушевавшись, не уничтожили и здоровые клетки.
Одновременно с этим в организме реализуется еще один, молекулярный, защитный механизм: пораженные вирусом клетки начинают производить специальные белки — интерфероны, — о которых многие слышали в связи с гриппозной инфекцией. Существует три основных вида интерферонов. Синтез интерферона-альфа (ИФ-α) стимулируют лейкоциты. Он участвует в борьбе с вирусами и обладает противоопухолевым действием. Интерферон-бета (ИФ-β) производят клетки соединительной ткани, фибробласты. Он обладает таким же действием, как и ИФ-α, только с уклоном в противоопухолевый эффект. Интерферон-гамма (ИФ-γ) синтезируют Т-клетки (Т-хелперы и (СD8+) Т-лимфоциты), что придает ему свойства иммуномодулятора, усиливающего или ослабляющего иммунитет. Как именно интерфероны борются с вирусами? Они могут, в частности, блокировать работу чужеродных нуклеиновых кислот, не давая вирусу возможности реплицироваться (размножаться).
В 2008 году американские исследователи из Университета Рокфеллера открыли еще один интерферон-зависимый антивирусный механизм. Выяснилось, что интерферон стимулирует синтез белка BST-2 (тетерина), блокирующего выход вирионов из клетки [16]. Но некоторые вирусы научились обходить действие интерферона. Так, вирус Эбола (рис. 4) с помощью своего белка eVP24 не дает ядерному фактору PY-STAT1 проникнуть в ядро и запустить действие интерферона [17]. У этого вируса есть еще несколько механизмов, делающих его неуязвимым для иммунитета. Так, внутреннее содержимое вируса окружено «чехлом» из полисахаридов, благодаря чему вирус плохо распознается иммунной системой*.
* — О борьбе с вирусом Эбола с помощью моноклональных антител рассказывает статья «Вирус Эбола и макак-резус: получено новое эффективное лекарство» [18].
Рисунок 4. Схема строения, 3D-модель и фото вируса Эбола. Рисунки с сайтов www.visual-science.com и ebolaviruspictures.blogspot.com.
Как мы видим, в идеале у здорового организма существует довольно надежная многоуровневая система защиты от проникновения всевозможных «чужаков». И действительно, все мы знаем, что встречаются люди, в силу своего крепкого здоровья устойчивые ко всяким сезонным инфекциям вроде ОРВИ или гриппа. Такой опасный агент, как вирус натуральной оспы, не убивал всех без исключения заразившихся, и большая часть заболевших выздоравливала своими силами. Среди них был и будущий глава СССР, И. Сталин, переболевший в детстве оспой. Даже лихорадка Эбола, наводящая сегодня ужас в Африке, оставляет в живых десятую часть заразившихся. И лишь по отношению к одной единственной инфекции эта система защиты оказывается бессильной в 100% случаев заражения. Ни один человек из 36,9 миллионов, инфицированных ВИЧ (данные ВОЗ на начало 2015 г.), не сможет избавиться от вируса, а заболевший СПИДом — полностью выздороветь [19].
Причины поражений в борьбе с ВИЧ
Тем не менее нельзя сказать, что ничего не делается в борьбе с ВИЧ и нет никаких подвижек в этом вопросе. Сегодня уже определены перспективные направления в исследованиях, главные из которых: использование антисмысловых молекул (антисмысловых РНК), РНК-интерференция, аптамерная и химерная технологии [12]. Но пока эти антивирусные методы — дело научных институтов, а не широкой клинической практики*. И потому более миллиона человек, по официальным данным ВОЗ, погибают ежегодно от причин, связанных с ВИЧ и СПИДом.
Почему же человечество со всем своим огромным научным и техническим потенциалом ничего не может противопоставить этой смертоносной инфекции? Проблема борьбы с ВИЧ многоуровневая и включает в себя несколько факторов. Так, неизвестно почему, но иммунная система человека вместо того, чтобы бороться с вирусом, иногда помогает ему. Этот феномен, получивший название антителозависимое усиление инфекции (ADE), был описан применительно к ВИЧ в конце 80-х годов американскими биологами из университетов Калифорнии и Вандербильта — В. Робинсоном и его коллегами [22]. Было обнаружено, что антитела, которые вырабатываются в организме в ответ на вирусную атаку, облегчают проникновение вируса в клетку (рис. 5, 6). Посредством специфического участка — Fc-области — они присоединяются к клеткам-фагоцитам и «проводят» вирус в них. Это похоже на то, как поводырь проводит плохо видящего человека в нужное место: антитело «берет за руку» вирус и заводит его в макрофаг.
Рисунок 5. Схема развития феномена ADE при вирусных инфекциях. а — Взаимодействие между антителом и рецептором FcR на поверхности макрофага. б — Фрагмент С3 комплемента (компонент комплемента, после присоединения которого весь этот комплекс приобретает способность прилипать к различным частицам и клеткам) и рецептор комплемента (complement receptor, CR) способствуют присоединению вируса к клетке. в — Белки комплемента С1q и С1qR способствуют присоединению вируса к клетке (в составе молекулы C1q имеется рецептор для связывания с Fc-фрагментом молекулы антитела). г — Антитела взаимодействуют с рецептор-связывающим сайтом вирусного белка и индуцируют его конформационные изменения, облегчающие слияние вируса с мембраной. д — Вирусы, получившие возможность реплицироваться в данной клетке посредством ADE, супрессируют противовирусные ответы со стороны антивирусных генов клетки. Рисунок с сайта supotnitskiy.ru.
Подобный вирусный механизм характерен не только для ВИЧ. Он описан и при инфицировании некоторыми другими опасными вирусами: такими, как вирусы Денге и Эбола. Но при ВИЧ антителозависимое усиление инфекции сопровождается еще несколькими факторами, делая его опасным и почти неуязвимым. Так, в 1991 году американские клеточные биологи из Мэриленда (Дж. Гудсмит с коллегами), изучая иммунный ответ на ВИЧ-вакцину, обнаружили так называемый феномен антигенного импринтинга [23]. Он был описан еще в далеком 1953 году при изучении вируса гриппа. Оказалось, что иммунная система запоминает самый первый вариант вируса ВИЧ и вырабатывает к нему специфические антитела. Когда вирус видоизменяется в результате точечных мутаций, а это происходит часто и быстро, иммунная система почему-то не реагирует на эти изменения, продолжая производить антитела к самому первому варианту вируса. Именно этот феномен, как считает ряд ученых, стоит препятствием перед созданием эффективной вакцины против ВИЧ.
Рисунок 6. Электронно-микроскопическая фотография макрофага, инфицированного ВИЧ-1. Две темные области — многочисленные вирусные частицы, которыми «нашпигована» клетка. Рисунок из [13].
Но и это еще не все уловки в арсенале смертоносной инфекции. В нашем организме существуют специальные антиретровирусные системы, которые должны противостоять ВИЧ. Сегодня известны три таких системы: упоминавшийся выше (в связи с интерфероном) BST-2/ тетерин, а также AID/APOBEC и TRIM5-α [24]. Но, как выяснилось, все они оказываются бессильны в борьбе против ВИЧ. Вот как об этом говорит М.Р. Бобкова из Института вирусологии им. Д.И. Ивановского: «Антивирусные системы клетки, получившие название „внутреннего иммунитета“ (intrinsic immunity), пытаются бороться с вирусом, но у них это плохо получается. APOBEC модифицирует вирусную ДНК таким образом, что это приводит к ее разрушению либо неполноценности. В ответ на это вирус ВИЧ приобрел белок Vif, блокирующий функцию APOBEC. TRIM5-α у обезьян хорошо справляется с функцией преждевременного „раздевания“ РНК вируса, но только не „своего“ вида, а всех других. У человека этот белок есть, но функция его снижена, и ее недостаточно для ограничения репликации (копирования) ВИЧ. Тетерин связывает отпочковывающиеся вирусные частицы и не дает им покинуть поверхность клетки. В противодействие этому у ВИЧ есть белок Vpu, который путем связывания тетерина „освобождает“ новые частицы. Представить себе, что эти механизмы защиты от внутреннего иммунитета вирус выработал за те несколько десятилетий, что он общается с человеком, невозможно, поэтому должно быть какое-то другое объяснение».
«Другое» объяснение приводит в своей работе известный специалист по ВИЧ, микробиолог Михаил Супотницкий. По его мнению, причина того, что антивирусные системы человека бессильны против ВИЧ, носит эволюционный характер: «Почему так работают антиретровирусные системы человека? Причина, скорее всего та же, что заставляет иммунную систему человека участвовать в размножении и распространении ВИЧ — эти системы созданы самими ретровирусами» [25]. Когда-то, несколько сотен миллионов лет назад, древние ретроэлементы, от которых произошли все ретровирусы, участвовали в процессе эволюции в формировании иммунной системы позвоночных, передав для ее генов некоторые свои элементы. И потому наша иммунная система, созданная ретроэлементами, иногда может по старой памяти воспринимать вирусы как «своих».
Открытие биологов из МГУ — Нефёдовой и Кима, — о котором упоминалось в самом начале, также говорит в пользу этой, эволюционной, версии.
Также известно, что ВИЧ в своем жизненном цикле задействует множество белков организма хозяина (рис. 7). В 2008 году ученые из Гарвардской медицинской школы и Института Говарда Хьюза посредством механизма РНК-интерференции провели исследование генома человека на предмет обнаружения белков-«коллаборационистов», сотрудничающих с ВИЧ [20]. В ходе работы ими были обнаружены 273 белка, так или иначе связанных с циклом ВИЧ [26]. Но и это еще не всё. Оказалось, что наши внутренние, эндогенные ретровирусы, тихо сидящие в нашей ДНК, могут в случае надобности предоставлять «чужим» ретровирусам (в том числе и ВИЧ) свои ферменты, необходимые для вирусного жизненного цикла. То есть внутренние и внешние вирусы взаимодействуют между собой: американскими исследователями был зафиксирован феномен, когда в ответ на прием ингибиторов протеаз протеаза эндогенного ретровируса человека HERV-К компенсировала своим действием отсутствие этого фермента у ВИЧ-1 [27]. Получается такая «дружеская взаимопомощь» между вирусами. Hе случайно авторитетный вирусолог, академик РАН Е.Д. Свердлов назвал наши эндогенные ретровирусы «пятой колонной» ВИЧ [2]. В свою очередь, ВИЧ может активизировать «дремавшие» эндогенные ретровирусы: наблюдали усиление экспрессии генов ретровируса HERV-K10 у ВИЧ-инфицированных и появление в сыворотке крови таких людей вирусных частиц HERV-K [28, 29].
Существует одна схожая особенность многих опасных вирусов, затрудняющая вакцинацию и лечение: они чрезвычайно быстро меняются. У ВИЧ это обусловлено тем, что фермент обратная транскриптаза делает массу ошибок при копировании вируса в организме — такая у этого фермента особенность. И потому вирусные копии отличаются одна от другой, и вирус становится неуловимым. Это похоже на то, как если бы полиция искала преступника по фотороботу и отпечаткам, а он каждый день менял свой облик, да еще и делал себе двойников. У других вирусов есть свои механизмы изменчивости. К примеру, два знаменитых филовируса — Эбола и Марбурга — с момента открытия изменились по составу аминокислот в некоторых белках более чем на 20%! Вирус гриппа постоянно меняется благодаря двум своим специфическим особенностям: «антигенному дрейфу» и «антигенному шифту» — мутации антигенов вируса и полной замене одного из генов* [31].
* — Разным аспектам, связанным с вирусом гриппа, биомолекула посвятила целую серию статей, первая из которых — «Гонки с вирусом: эпидемиология и экология вируса гриппа» [32].
Эпидемии «медленных» вирусов и вирусная эволюция
Сегодня не только ВИЧ представляет опасность для человечества, хотя он, конечно, самый главный наш вирусный враг. Так сложилось, что СМИ уделяют внимание, в основном, молниеносным инфекциям, вроде атипичной пневмонии или МЕRS, которыми быстро заражается сравнительно большое количество людей (и немало гибнет). Из-за этого в тени остаются медленно текущие инфекции, которые сегодня гораздо опаснее и коварнее коронавирусов* и даже вируса Эбола. К примеру, мало кто знает о мировой эпидемии гепатита С, вирус которого был открыт в 1989 году**. А ведь по всему миру сейчас насчитывается 150 млн человек — носителей вируса гепатита С! И, по данным ВОЗ, каждый год от этой инфекции умирает 350-500 тысяч человек [33]. Для сравнения — от лихорадки Эбола в 2014-2015 гг. (на состояние по июнь 2015 г.) погибли 11 184 человека [34].
* — Коронавирусы — РНК-содержащие вирусы, поверхность которых покрыта булавовидными отростками, придающими им форму короны. Коронавирусы поражают альвеолярный эпителий (выстилку легочных альвеол), повышая проницаемость клеток, что приводит к нарушению водно-электролитного баланса и развитию пневмонии.
** — О строении и свойствах другого вируса, вируса гепатита А, читайте в статье «Вирус гепатита А: новое — это хорошо забытое старое» [35].
Конечно, атипичная пневмония, «птичий» грипп, коронавирус MERS и другие, неизвестные пока инфекции при определенных обстоятельствах могут вызвать эпидемии с большими человеческими жертвами. Природный резервуар «запасных» частей для вирусов огромен, и они могут складываться в опасные формы. Этот процесс носит название рекомбинация вирусов — вирусы обмениваются своими «запасными» частями (генами) друг с другом и с носителями, создавая новые виды. И именно после этого появляются новые опасные формы вирусов, о которых мы регулярно узнаем из новостных лент СМИ.
Причем больших изменений для возникновения опасной формы вируса не требуется. Так, «испанский» грипп, от которого в 1918-1920 гг. погибло более 20 млн человек, был вызван вирусом типа H1N1 (рис. 8), доставшимся человеку от птиц. В конце 90-х гг. американские ученые из Armed Forces Institute of Pathology исследовали этот вирус, выделив его из тел, похороненных на Аляске, и нашли всего лишь одно существенное изменение, сделавшее его смертельным: изменение в гене поверхностного белка — нейраминидазы [36]. В 2008 году ученые из Массачусетского технологического института — Т. Тампи и его коллеги — дополнили эти исследования, обнаружив еще две возможные мутации, которые могли сделать этот вирус «массовым убийцей»: мутации в структуре второго поверхностного белка вируса гриппа — гемагглютинина, — которые позволили ему связываться со специфическими гликанами человеческих эпителиальных клеток (рецепторами α2—6)* [37].
Рисунок 8. Электронная микрофотография воссозданного вируса H1N1, вызвавшего эпидемию в 1918 г. Рисунок с сайта phil.cdc.gov.
Почему же вдруг сложилась такая ситуация, что буквально каждый год появляются новые, всё более опасные формы вирусов? По мнению ученых, главные причины — это сомкнутость популяции, когда происходит тесный контакт людей при их большом количестве, и снижение иммунитета вследствие загрязнения среды обитания и стрессов. Научный и технический прогресс создал такие возможности и средства передвижения, что носитель опасной инфекции уже через несколько суток может добраться с одного континента на другой, преодолев тысячи километров.
Всё тот же научный прогресс стал причиной односторонней миграции населения из сёл и малых городов в крупные города, что привело к возникновению компактных многомиллионных поселений. Чего не было за всю длинную эволюцию человека. И такая скученность населения в крупных городах создает все условия для возникновения и распространения новых форм вирусов: ослабление иммунитета как следствие загрязненной среды обитания и стрессов и возможность скорейшего инфицирования всё новых и новых хозяев. Академик В.А. Кордюм (Институт молекулярной биологии и генетики, Киев) приводит пример с вирусом герпеса человека 7-го типа (ВГЧ-7) и цитомегаловирусом. Эти два инфекционных агента распространены повсеместно: ими инфицировано большинство населения Земли. И пока человек живет в нормальных условиях, они никак себя не проявляют. Но стоит лишь иммунитету ослабеть — вследствие стресса или других факторов — ВГЧ-7 и цитомегаловирус активизируются, еще более угнетая иммунную систему и «открывая ворота» для других, более опасных вирусов [39].
Ясно, что мы пока не до конца понимаем причины стремительной эволюции вирусов и те природные механизмы, которые способствуют этому. Очевидно, что наш современный «урбанистический» образ жизни играет в этих процессах не последнюю роль. Человек, устраивая свою жизнь с комфортом и переделывая всё вокруг на свой вкус и под свои нужды, вдруг забыл, что он обычный биологический вид и перестал жить по законам природы. А вирусы напоминают нам об этом.
Первоначальный вариант статьи был опубликован в журнале «Популярная механика» [40].