Что выделяет уголь при горении
В условиях роста цен на нефть и газ наиболее выгодным топливом для производства электроэнергии становится уголь. Современные энергоблоки теплоэлектростанций достигают мощности 1 000 МВт, а сами процессы сжигания угля в котлах настолько сложны, что учесть все детали на стадии проектирования практически невозможно. Точно рассчитать необходимые параметры топочных процессов и найти способы повысить эффективность работы энергоблоков позволяют компьютерные модели
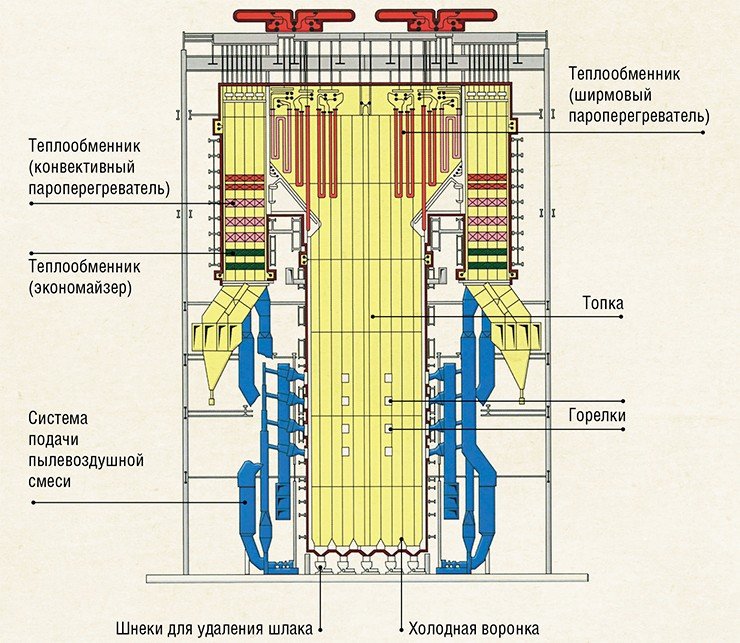
На современных энергостанциях уголь сжигается в факеле в виде пыли тонкого помола, которая вдувается в топку потоком воздуха через специальные горелки. Сама топка представляет собой высокую, несколько десятков метров, башню, внутри которой установлены специальные теплообменники для нагревания («перегрева») пара, подогрева воды или воздуха. Такой способ сжигания угля весьма перспективен, поскольку позволяет сравнительно легко управлять процессом горения.
В советское время основным научным подходом при создании энергетических котлов служило сжигание топлива в экспериментальных условиях. Но таким способом нельзя выявить всех особенностей процессов горения угля, которые проявятся во время штатной, длительной эксплуатации топочных котлов. В том числе определить, как скажется качество топлива на процессах шлакования, т. е. образования связанных отложений на поверхностях нагрева котельной топки.
Слишком горячо
В проектировании и технологической доводке котлов П-67 на Березовской ГРЭС, самых больших и мощных в России, принимали участие многие научно-исследовательские институты и машиностроительные заводы, в частности, Подольский машиностроительный завод им. С. Орджоникидзе.
Первый блок ГРЭС был запущен в 1988 г., второй – через три года. Уже через несколько лет работы котлов выяснилось, что, несмотря на все усилия проектировщиков, эксплуатационные характеристики топочных котлов оказались ниже проектных. Причина заключалась в том, что на топочных экранах происходил рост прочных шлаковых отложений.
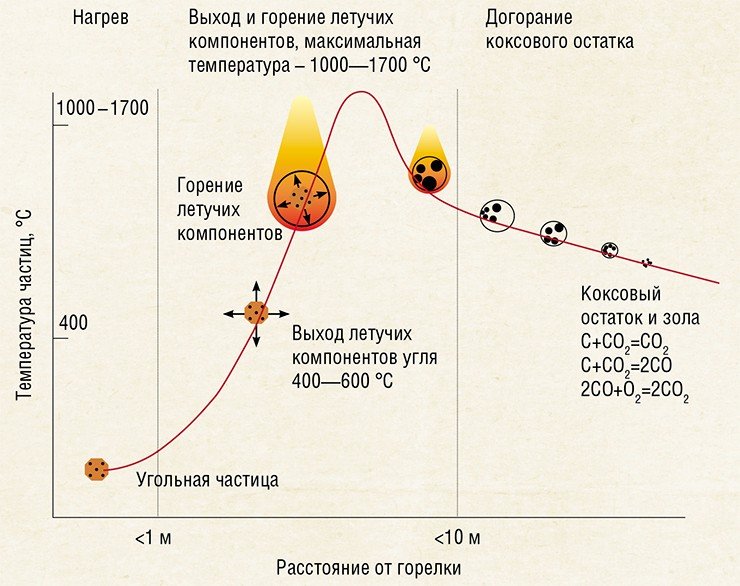
Дело в том, что при сгорании углей получается большое количество золы, способной образовывать шлаковые отложения. Если температура частиц золы будет выше температуры плавления золы, то расплавленный шлак осядет на стенках топки и поверхностях теплообменников, затвердеет и будет мешать работе котла. Однако если создать температурные условия, при которых зола останется твердой, то основная ее масса попадет в холодную воронку и золу можно будет удалить механически. Например, при помощи шнеков или транспортеров, как это и было задумано для котла П-67.
Однако выяснилось, что при достижении номинальной мощности во время эксплуатации котлов показатели интенсивности теплообмена в топке были ниже проектных, наблюдалось прогрессирующее шлакование топочной камеры, сопровождающееся ростом максимальной температуры газов на выходе, которая превышала проектные 1032°С более чем на 100° С. Образовавшиеся глыбы шлака при падении повреждали детали конструкции холодной воронки – нижней части топки под горелками, предназначенной для сбора и удаления твердых частиц шлака, а локальное шлакование ее скатов приводило к вынужденным остановкам котлов.
Поэтому на основании данных балансовых испытаний было предложено понизить рабочую мощность котлов, в результате чего в 2000 г. энергоблоки были перемаркированы с мощности 800 МВт на 700 МВт. Стало ясно, что необходимо искать новые методы, которые помогут устранить недоработки проекта и выйти на проектную мощность.
Компьютер в помощь
Только через десять лет после ввода в действие Березовской ГРЭС появился новый мощный инструмент для изучения процессов, происходящих в топочной камере. Речь идет о математическом моделировании, позволяющем изучить аэродинамику топки, теплообмен, процессы образования оксидов азота и шлакования для различных режимов эксплуатации и вариантов реконструкции топочно-горелочного устройства. Разработкой такой компьютерной модели занялись специалисты Института теплофизики СО РАН (Новосибирск) и Сибирского федерального университета (Красноярск).
В конечном итоге на свет появился программный продукт «SigmaFlow», который позволил с высокой точностью провести численные исследования и определить наконец причины образования шлаковых отложений в топке котла П-67.
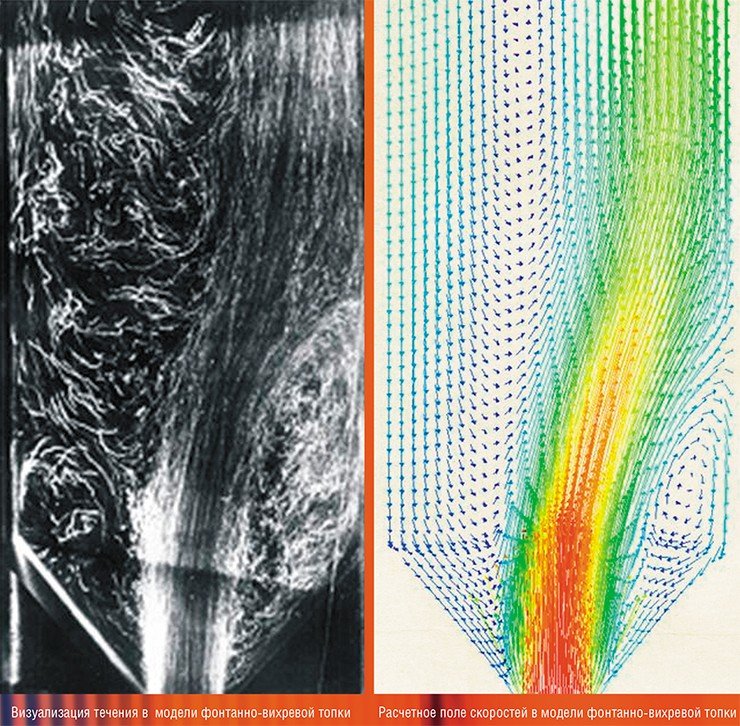
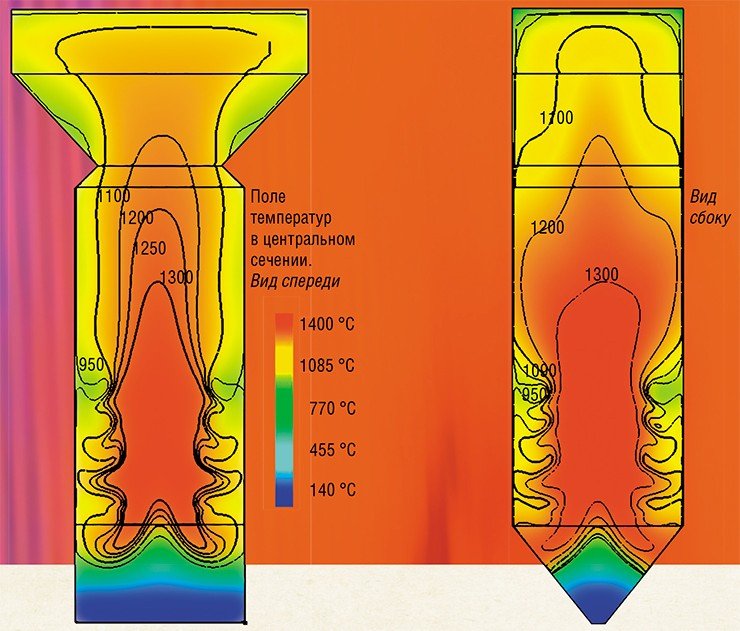
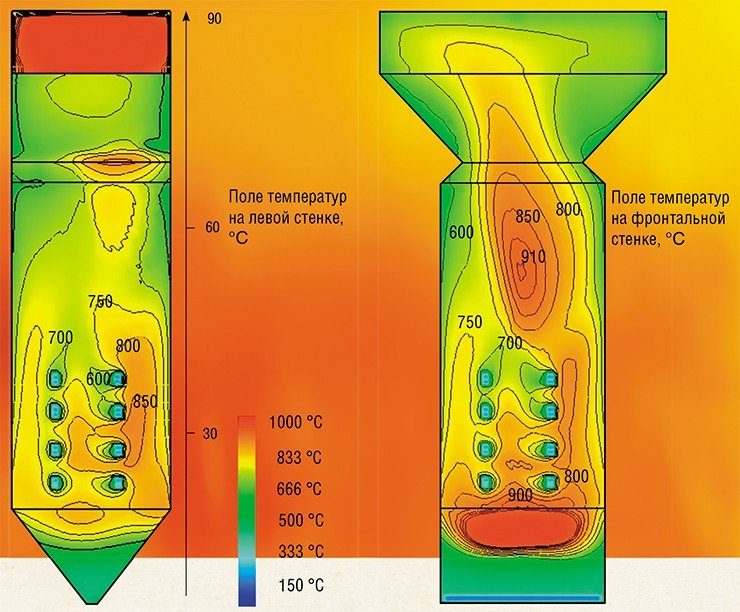
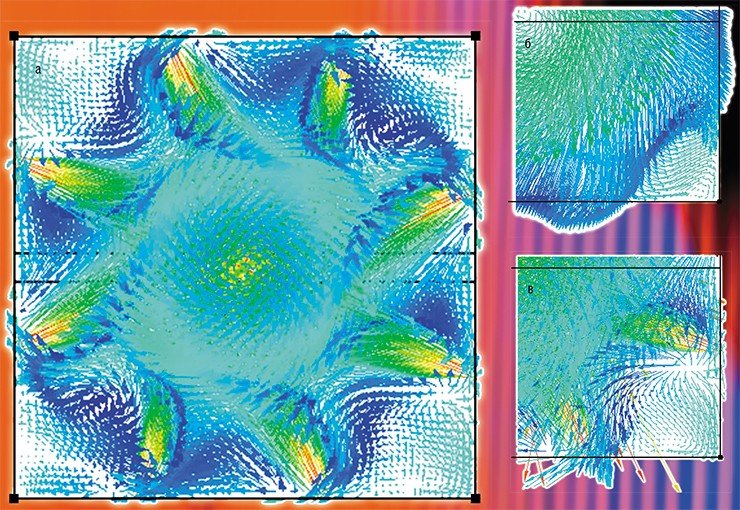
Было установлено, что аэродинамическая структура газовых потоков в топочной камере обладает высокой неравномерностью: крупномасштабный центральный вихрь инициирует вторичные вихри в углах топочной камеры, которые приводят к набросу потока на стенку топки, температура которой начинает повышаться. На этой перегретой поверхности образуются шлаковые отложения.
Отложение шлака происходит также около горелок, особенно по нечетным вертикальным рядам. Основная причина этого явления – осаждение мелкой фракции золы, частицы которой вовлекаются в движение вторичными вихрями в углах топочной камеры. Обладая достаточно высокой температурой, они достигают экрана, где и образуют шлаковые отложения.
Еще одно место интенсивного шлакования находится на фронтальной и задней стенках котла выше зоны активного горения – на высоте 45—65 м. На этом уровне центральный вихрь, раскручиваясь, быстро теряет осевую симметрию и приобретает овальную форму, вытянутую к фронтальной и задней стенкам. В результате там образуются области с высокой температурой, и расплавленные частицы золы «набрасываются» на стенки газовым потоком.
Шлаку – нет!
На основе численного моделирования и результатов ряда других исследовательских работ было предложено несколько способов решения проблемы шлакования. Было рассмотрено несколько вариантов топки: с организацией нижнего дутья с подводом воздуха в холодную воронку; с концентрической ориентацией горелок; с комбинацией нижнего дутья и концентрического сжигания; организацией воздушного дутья выше зоны активного горения и т. д.
Результаты численных исследований показали, что максимальный эффект по снижению шлакования поверхностей нагрева относительно «базового» варианта достигается при использовании блоков воздушных завес и нижнего дутья; а максимальный эффект по снижению выбросов NОх – двух ярусов сопел дутья, расположенных на высотах 45 и 65 м.
В результате для реконструкции котла был выбран вариант топки с нижним воздушным дутьем. Расчетным путем были также проанализированы разные способы подвода воздуха в холодную воронку, и из них выбран оптимальный, способствующий равномерной подаче воздуха в топочную камеру.
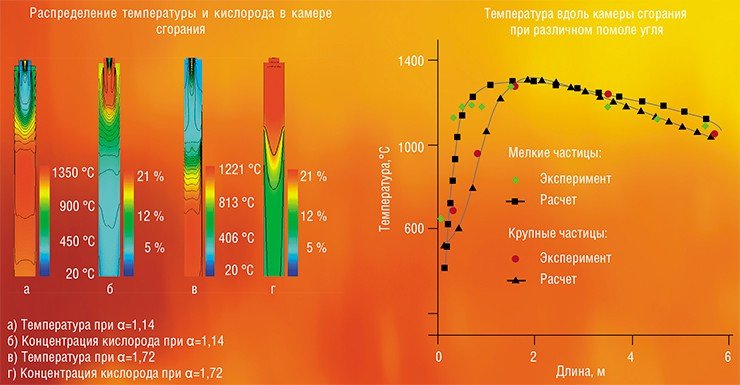
Кроме того, с помощью численного моделирования было исследовано влияние степени помола угольной пыли на эффективность топочного процесса. Согласно расчетам, загрузка нижних ярусов горелок более грубой пылью снижала содержание золы в верхней части котла. При этом повышался провал частиц угля в холодную воронку, однако этому при нижнем дутье препятствовал поток воздуха, идущий снизу вверх. А за счет подвода дополнительного кислорода оказалось возможным снизить содержание несгоревшего углерода в частицах.
Один из энергетических блоков Березовской ГРЭС был реконструирован в 2010 г. Его дальнейшая эксплуатация показала, что он может длительное время нести максимальную нагрузку на уровне проектной, т. е. 800 МВт.
На примере Березовской ГРЭС мы видим ту огромную бесспорную пользу, которую может принести применение современных методов математического моделирования при проектировании крупных технологических объектов. И дело здесь не только в оптимизации эксплуатационных параметров, но и в значительной экономии средств на разработку: ведь гораздо дешевле просчитать интересующие процессы, чем проводить натурные эксперименты.
Дело за малым – важно, что бы этими возможностями воспользовались производители энергетических котлов, гидротурбин, атомных станций и других крупных, высокотехнологичных и нередко представляющих экологическую угрозу объектов нашего промышленно-энергетического комплекса.
Белый В. В и др. Исследование теплообмена и модернизация топочной камеры котла П-67 блока 800 МВт газа // Теплофизика и аэромеханика, 2007. Т. 14. № 2. С. 299—312.
Backreedy R. I. et al. Modelling pulverised coal combustion using a detailed coal combustion model, Combustion Science and Technology. 2006. № 178(4). P. 763—787.
Работа выполнена при финансовой поддержке Министерства образования и науки РФ (гос. контракт № 16.516.11.6036)
Продукты горения (сгорания)
Продукты горения – это вещества (газообразные, жидкие или твердые вещества) и соединения, образующиеся в результате сложного физико-химического процесса горения веществ (материалов).
Под продуктами горения чаще всего понимают дым, токсичные продукты горения, сажу и другие.
Продукты горения сухой травы
Состав
Состав их зависит от состава горящего вещества и условий его горения. В условиях пожара чаще всего горят органические вещества (древесина, ткани, бензин, керосин, резина и др.), в состав которых входят главным образом углерод, водород, кислород и азот. При горении их в достаточном количестве воздуха и при высокой температуре образуются продукты полного сгорания: СО2, Н2О, N2. При горении в недостаточном количестве воздуха или при низкой температуре кроме продуктов полного сгорания образуются продукты неполного сгорания: СО, С (сажа).
Продукты сгорания называют влажными, если при расчете их состава учитывают содержание паров воды, и сухими, если содержание паров воды не входит в расчетные формулы.
Реже во время пожара горят неорганические вещества, такие как сера, фосфор, натрий, калий, кальций, алюминий, титан, магний и др. Продуктами сгорания их в большинстве случаев являются твердые вещества, например Р2О5, Na2O2, CaO, MgO. Образуются они в дисперсном состоянии, поэтому поднимаются в воздух в виде плотного дыма. Продукты сгорания алюминия, титана и других металлов в процессе горения находятся в расплавленном состоянии.
При неполном сгорании органических веществ в условиях низких температур и недостатка воздуха образуются более разнообразные продукты – окись углерода, спирты, кетоны, альдегиды, кислоты и другие сложные химические соединения. Они получаются при частичном окислении как самого горючего, так и продуктов его сухой перегонки (пиролиза). Эти продукты образуют едкий и ядовитый дым. Кроме того, продукты неполного горения сами способны гореть и образовывать с воздухом взрывчатые смеси. Такие взрывы бывают при тушении пожаров в подвалах, сушилках и в закрытых помещениях с большим количеством горючего материала. Рассмотрим кратко свойства основных продуктов горения.
Углекислый газ
Углекислый газ или двуокись углерода (СО2) – продукт полного горения углерода. Не имеет запаха и цвета. Плотность его по отношению к воздуху равна 1,52. Плотность углекислого газа при температуре Т = 0 ° С и при нормальном давлении р = 760 миллиметров ртутного столба (мм Hg) равна 1,96 кг/м 3 (плотность воздуха при этих же условиях равна ρ = 1,29 кг/м 3 ). Углекислый газ хорошо растворим в воде (при Т = 15 °С в одном литре воды растворяется один литр газа). Углекислый газ не поддерживает горение веществ, за исключением щелочных и щелочно-земельных металлов. Горение магния, например, происходит в атмосфере углекислого газа по уравнению:
Токсичность углекислого газа незначительна. Концентрация углекислого газа в воздухе 1,5 % безвредна для человека длительное время. При концентрации углекислого газа в воздухе, превышающей 3-4,5 %, нахождение в помещении и вдыхание газа в течение получаса опасно для жизни. При температуре Т = 0 °С и давлении р = 3,6 МПа углекислый газ переходит в жидкое состояние. Температура кипения жидкой углекислоты составляет Т = –78 °С. При быстром испарении жидкой углекислоты газ охлаждается и переходит в твердое состояние. Как в жидком, так и твердом состоянии, капли и порошки углекислоты применяются для тушения пожаров.
Оксид углерода
Всем известная вода – Н2О – также выделяется во время горения виде газа – как пар. Вода является продуктом горения газа метана – СН4. Вообще, вода и углекислота в основном выделяются при полном сгорании всех органических веществ.
Цианистый водород
Акролеин
Пропеналь, акролеин, акрилальдегид – все это названия одного вещества, ненасыщенного альдегида акриловой кислоты: СН2=СН-СНО. Этот альдегид тоже является сильно летучей жидкостью. Акролеин бесцветен, с резким запахом, очень ядовит. При попадании жидкости или ее паров на слизистые, особенно в глаза, вызывает сильное раздражение. Пропеналь является высокореакционным соединением, и это объясняет его высокую токсичность.
Формальдегид
Подобно акролеину, формальдегид принадлежит к классу альдегидов и является альдегидом муравьиной кислоты. Также это соединение известно как метаналь. Это токсичный, бесцветный газ с резким запахом.
Азотсодержащие вещества
Чаще всего во время горения веществ, содержащих азот, выделяется чистый азот – N2. Этот газ и так содержится в атмосфере в большом количестве. Азот может быть примером продукта горения аминов. Но при термическом разложении, к примеру, солей аммония, а в некоторых случаях и при самом горении, в атмосферу выбрасываются и его оксиды, со степенью окисления азота в них плюс один, два, три, четыре, пять. Оксиды – газы, имеют бурый цвет и чрезвычайно токсичны.
Сернистый газ
При горении многих веществ, кроме рассмотренных выше продуктов сгорания выделяется дым – дисперсная система, состоящая из мельчайших твердых частиц, находящихся во взвешенном состоянии в каком-либо газе. Диаметр частиц дыма составляет от 10 −4 до 10 −6 см (от 1 до 0,01 мкм). Отметим, что 1 мкм (микрон) равен 10 −6 м или 10 −4 см. Более крупные твердые частицы, образующиеся при горении, быстро оседают в виде копоти и сажи. При горении органических веществ дым содержит твердые частицы сажи, взвешенные в CO2, CO, N2, SO2 и других газах. В зависимости от состава и условий горения вещества получаются различные по составу и по цвету дымы. При горении дерева, например, образуется серовато-черный дым, ткани – бурый дым, нефтепродуктов – черный дым, фосфора – белый дым, бумаги, соломы – беловато-желтый дым.
В составе дыма, образующегося на пожарах при горении органических веществ, кроме продуктов полного и неполного сгорания, содержатся продукты термоокислительного разложения горючих веществ. Образуются они при нагреве еще негорящих горючих веществ, находящихся в среде воздуха или дыма, содержащего кислород. Обычно это происходит перед факелом пламени или в верхних частях помещений, где находятся нагретые продукты сгорания.
Состав продуктов термоокислительного разложения зависит от природы горючих веществ, температуры и условий контакта с окислителем. Так, исследования показывают, что при термоокислительном разложении горючих веществ, в молекулах которых содержатся гидроксильные группы, всегда образуется вода. Если в составе горючих веществ находятся углерод, водород и кислород, продуктами термоокислительного разложения чаще всего являются углеводороды, спирты, альдегиды, кетоны и органические кислоты. Если в составе горючих веществ, кроме перечисленных элементов, есть хлор или азот, то в дыме находятся также хлористый и цианистый водород, оксиды азота и другие соединения. Так, в дыме при горении капрона содержится цианистый водород, при горении линолеума «Релин» – сероводород, диоксид серы, при горении органического стекла – оксиды азота. Продукты неполного сгорания и термоокислительного разложения в большинстве случаев являются токсичными веществами, поэтому тушение пожаров в помещениях производят только в кислородных изолирующих противогазах.
Пепел, зола, копоть, сажа, уголь
Копоть, или сажа – остатки углерода, который не вступил в реакцию, по разным причинам. Сажу называют также амфотерным углеродом. Зола, или пепел – мелкие частицы неорганических солей, не сгоревших или не разложившихся при температуре горения. При выгорании топлива эти микросоединения переходят во взвешенное состояние или скапливаются внизу. А уголь – это продукт неполного сгорания дерева, то есть не сгоревшие его остатки, но при этом еще способные гореть. Конечно, это далеко не все соединения, которые выделятся при сгорании тех или иных веществ. Перечислить их всех нереально, да и не нужно, потому что другие вещества выделяются в ничтожно малых количествах, и только при окислении определенных соединений.
Классификация
Большинство продуктов горения являются отравляющими веществами. Поэтому, говоря об их классификации, будет правильным ознакомить вас со следующим термином:
Классификация опасности веществ по степени воздействия на организм – это установление (ранжирование) уровней опасности веществ по их поражающему и повреждающему воздействию на организм человека и (или) животного. Более подробно о данной классификации читайте в материале по ссылке >>
Также ознакомьтесь с познавательным материалом по теме:
Формулы для расчета объема
Вид формулы для расчета объема продуктов полного сгорания при теоретически необходимом количестве воздуха зависит от состава горючего вещества.
Индивидуальное химическое соединение
В этом случае расчет ведут, исходя из уравнения реакции горения. Объем влажных продуктов сгорания единицы массы (кг) горючего вещества при нормальных условиях рассчитывают по формуле:
Vп.с. – объем влажных продуктов сгорания, м 3 /кг; 
Например, чтобы определить объем сухих продуктов сгорания 1 кг ацетона при нормальных условиях, составляем уравнение реакции горения ацетона в воздухе:
Определяем объем сухих продуктов сгорания ацетона:
Объем влажных продуктов сгорания 1 м 3 горючего вещества (газа) можно рассчитать по формуле:
Vп.с. – объем влажных продуктов сгорания 1 м 3 горючего газа, м 3 /м 3 ; 
Сложная смесь химических соединений
Если известен элементный состав сложного горючего вещества, то состав и количество продуктов сгорания 1 кг вещества можно определить по уравнению реакции горения отдельных элементов. Для этого составляют уравнения реакции горения углерода, водорода, серы и определяют объем продуктов сгорания, приходящийся на 1 кг горючего вещества. Уравнение реакции горения имеет вид:
С + О 2 + 3,76N 2 = СО 2 + 3,76N 2
При сгорании 1 кг углерода получается 22,4 / 12 = 1,86 м 3 СО 2 и 22,4 × 3,76/12 = 7,0 м 3 N 2.
Аналогично определяют объем (в м 3 ) продуктов сгорания 1 кг серы и водорода. Полученные данные приведены ниже:
| СО2 | N2 | Н2О | SO2 | |
| Углерод | 1,86 | 7,00 | – | – |
| Водород | – | 21,00 | 11,2 | – |
| Сера | – | 2,63 | – | 0,7 |
При горении углерода, водорода и серы кислород поступает из воздуха. Однако в состав горючего вещества может входить кислород, который также принимает участие в горении. В этом случае воздуха на горение вещества расходуется соответственно меньше.
В составе горючего вещества могут находиться азот и влага, которые в процессе горения переходят в продукты сгорания. Для их учета необходимо знать объем 1 кг азота и паров воды при нормальных условиях.
На основании приведенных данных определяют состав и объем продуктов сгорания 1 кг горючего вещества.
Например, чтобы определить объем и состав влажных продуктов сгорания 1 кг каменного угля, состоящего из 75,8 % С, 3,8 % Н, 2,8 % О, 1,1 % N, 2,5 % S, W = 3,8 %, A = 11,0 %.
Объем продуктов сгорания будет следующий, м 3 :
| Состав продуктов сгорания | СО2 | Н2О | N2 | SO2 |
| Углерод | 1,86 × 0,758 = 1,4 | – | 7 × 0,758 = 5,306 | – |
| Водород | – | 11,2 × 0,038 = 0,425 | 21 × 0,038 = 0,798 | – |
| Сера | – | – | 2,63 × 0,025 = 0,658 | 0,7 × 0,025 = 0,017 |
| Азот в горючем веществе | – | – | 0,8 × 0,011 = 0,0088 | – |
| Влага в горючем веществе | – | 1,24 × 0,03 = 0,037 | – | – |
| Сумма | 1,4 | 0,462 | 6,7708 – 0,0736 = 6,6972 | 0,017 |
Vп.с. = 1,4 + 0,462 + 6,6972 + 0,017 = 8,576 м 3 /кг.
Смесь газов
Количество и состав продуктов сгорания для смеси газов определяют по уравнению реакции горения компонентов, составляющих смесь. Например, горение метана протекает по следующему уравнению:
СН 4 + 2О 2 + 2 × 3,76N 2 = СО 2 + 2Н 2О + 7,52N 2
Согласно этому уравнению, при сгорании 1 м 3 метана получается 1 м 3 диоксида углерода, 2 м 3 паров воды и 7,52 м 3 азота. Аналогично определяют объем (в м 3 ) продуктов сгорания 1 м 3 различных газов:
| СО2 | Н2О | N2 | SO2 | |
| Водород | – | 1,0 | 1,88 | – |
| Окись углерода | 1,0 | – | 1,88 | – |
| Сероводород | – | 1,0 | 5,64 | 1,0 |
| Метан | 1,0 | 2,0 | 7,52 | – |
| Ацетилен | 2,0 | 1,0 | 9,54 | – |
| Этилен | 2,0 | 2,0 | 11,28 | – |
На основании приведенных цифр определяют состав и количество продуктов сгорания смеси газов.
Анализ продуктов сгорания, взятых на пожарах в различных помещениях, показывает, что в них всегда содержится значительное количество кислорода. Если пожар возникает в помещении с закрытыми оконными и дверными проемами, то пожар при наличии горючего может продолжаться до тех пор, пока содержание кислорода в смеси воздуха с продуктами сгорания в помещении не снизится до 14-16 % (об.). Следовательно, на пожарах в закрытых помещениях содержание кислорода в продуктах сгорания может быть в пределах от 21 до 14 % (об.). Состав продуктов сгорания во время пожаров в помещениях с открытыми проемами (подвал, чердак) показывает, что содержание в них кислорода может быть ниже 14 % (об.):
| СО | СО2 | О2 | |
| В подвалах | 0,15-0,5 | 0,8-8,5 | 10,6-19 |
| На чердаках | 0,1-0,6 | 0,3-4,0 | 16,0-20,2 |
По содержанию кислорода в продуктах сгорания на пожарах можно судить о коэффициенте избытка воздуха, при котором происходило горение.
Действие на организм человека
Степень токсичности веществ связана с их физической и химической природой. Взаимодействуя с организмом, продукты горения вызывают патологические синдромы.
Международная классификация болезней десятого пересмотра МКБ-10 определяет отравление продуктами горения кодом Т59 – «Токсическое действие других газов, дымов и паров».
По механизму действия на человека отравляющие компоненты в составе дыма делятся на пять групп.
Многие токсины, образующие в продуктах горения «универсальны», так как вызывают поражение сразу нескольких систем организма.
Первая помощь при отравлении
Симптомы интоксикации разными веществами могут отличаться, но принципы оказания первой помощи всегда одинаковые.
Большинство ядов поступает через дыхательные пути. Первое, что необходимо сделать при отравлении – прекратить поступление продуктов горения в организм. Для этого необходимо:
Острая интоксикация требуют оказания экстренной помощи. Действия при отравлении продуктами горения, следующие:
Некоторые ингаляционные отравления продуктами горения имеют период мнимого благополучия. Даже при отсутствии патологических симптомов, стоит внимательно следить за состоянием тех, кто может быть отравлен. При первых же признаках неблагополучия необходимо вызывать соответствующих специалистов.
Отравление продуктами горения у детей развивается быстрее, чем у взрослых. Это объясняется более высоким уровнем кислородного обмена. У малышей появляются жалобы на головную боль, сонливость, слезотечение, тошноту. При осмотре заметны изменения цвета кожи, учащение и затруднение дыхания, нарушения координации. Принципы оказания первой помощи для детей те же, что и для взрослых. При отсутствии специализированной медицинской помощи, пострадавшему ребенку угрожают необратимые изменения центральной нервной системы.
Источник: Пожаровзрывобезопасность веществ и материалов и средства их тушения: Справочник. Баратов А.Н., Корольченко А.Я. –М., 1990.