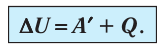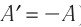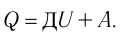Таблица «Применение изопроцессов в жизни»

Двигатели смешанного типа
V =const, А =0,

Нагрев воды в чайнике; нагрев воздуха в комнате; получение планетой Земля энергии от Солнца (видеофильм «Астрономия»); выделение энергии (образование ледяного покрова – без учёта изменения объёма)

Двигатели смешанного типа
V =const, А =0,

Нагрев воды в чайнике; нагрев воздуха в комнате; получение планетой Земля энергии от Солнца (видеофильм «Астрономия»); выделение энергии (образование ледяного покрова – без учёта изменения объёма)
Курс повышения квалификации
Дистанционное обучение как современный формат преподавания
Курс профессиональной переподготовки
Физика: теория и методика преподавания в образовательной организации
Курс повышения квалификации
Современные педтехнологии в деятельности учителя
Номер материала: ДБ-053425
Международная дистанционная олимпиада Осень 2021
Не нашли то что искали?
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
Рособрнадзор оставил за регионами решение о дополнительных школьных каникулах
Время чтения: 1 минута
Названы лучшие по качеству проведения ЕГЭ регионы России
Время чтения: 1 минута
В России объявлены нерабочие дни с 30 октября по 7 ноября
Время чтения: 2 минуты
В школе в Пермском крае произошла стрельба
Время чтения: 1 минута
Основы православной культуры чаще всего преподают учителя начальных классов
Время чтения: 2 минуты
Минобрнауки предложило вузам перевести студентов на удаленку
Время чтения: 1 минута
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
Что такое изотермический процесс? (Примеры, упражнения)
Содержание:
Эти изменения представляют собой фазовые переходы, когда вещество переходит из твердого состояния в жидкое, из жидкого в газообразное или наоборот. В таких случаях молекулы вещества меняют свое положение, добавляя или извлекая тепловую энергию.
Тепловая энергия, необходимая для возникновения фазового перехода в веществе, называется скрытой теплотой или теплотой превращения.
Этот тип процесса часто встречается в природе. Например, у людей, когда температура тела повышается или понижается, мы чувствуем себя больными, потому что в нашем теле многие химические реакции, поддерживающие жизнь, происходят при постоянной температуре. Это справедливо для теплокровных животных в целом.
Примеры изотермических процессов
— Обмен веществ у теплокровных животных осуществляется при постоянной температуре.
— Когда вода закипает, происходит фазовый переход от жидкости к газу, а температура остается постоянной примерно на уровне 100 º C, поскольку на значение могут влиять другие факторы.
-Автомобильные двигатели, холодильники, а также многие другие виды техники исправно работают в определенном температурном диапазоне. Для поддержания нужной температуры устройства называли термостаты. В его конструкции использованы различные принципы работы.
Цикл Карно
Двигатель автомобиля работает по аналогичным принципам. Движение поршня внутри цилиндра передается другим частям автомобиля и вызывает движение. Он не имеет поведения идеальной системы, такой как двигатель Карно, но термодинамические принципы являются общими.
Расчет работы, проделанной в изотермическом процессе
Чтобы рассчитать работу, совершаемую системой при постоянной температуре, мы должны использовать первый закон термодинамики, который гласит:
Это еще один способ выражения сохранения энергии в системе, представленный через ΔU или изменение энергии, Q по мере поступления тепла и, наконец, W, что и есть работа, проделанная указанной системой.
Предположим, что рассматриваемая система представляет собой идеальный газ, содержащийся в цилиндре подвижного поршня площадью К, который работает, когда его объем V смена V1 к V2.
Итак, проделанная работа рассчитывается путем интегрирования небольшой дифференциальной работы, в которой сила F производит небольшое смещение dx:
Как Adx это именно изменение объема dV, так:
Чтобы получить полную работу в изотермическом процессе, проинтегрируем выражение для dW:
Давление п и объем V изображены на диаграмме P-V как показано на рисунке, а проделанная работа равна площади под кривой:
Как ΔU = 0 поскольку температура остается постоянной, в изотермическом процессе необходимо:
— Упражнение 1
Цилиндр с подвижным поршнем содержит идеальный газ при 127ºC. Если поршень движется, чтобы уменьшить начальный объем в 10 раз, сохраняя постоянную температуру, найдите количество молей газа, содержащегося в цилиндре, если работа, проделанная с газом, равна 38 180 Дж.
Факт: R = 8,3 Дж / моль. K
Решение
В заявлении говорится, что температура остается постоянной, поэтому мы находимся в наличии изотермического процесса. Для работы, проделанной с газом, мы имеем ранее выведенное уравнение:
127 º C = 127 + 273 K = 400 K
Решите относительно n количество родинок:
Работе предшествовал отрицательный знак. Внимательный читатель заметит в предыдущем разделе, что W было определено как «работа, выполняемая системой» и имеет знак +. Так что «проделанная работа над системой» имеет отрицательный знак.
— Упражнение 2.
У вас есть воздух в цилиндре с поршнем. Изначально есть 0,4 м 3 газа под давлением 100 кПа и температурой 80ºC. Воздух сжимается до 0,1 м 3 обеспечение постоянной температуры внутри цилиндра во время процесса.
Определите, сколько работы было сделано во время этого процесса.
Решение
Мы используем ранее полученное уравнение для работы, но количество молей неизвестно, которое можно рассчитать с помощью уравнения идеального газа:
80 º C = 80 + 273 K = 353 K.
п1V1 = n.R.T → n = P1V1 / RT = 100000 Па x 0,4 м 3 /8,3 Дж / моль. K x 353 K = 13,65 моль
Опять же отрицательный знак указывает на то, что в системе были выполнены работы, что всегда происходит при сжатии газа.
Ссылки
Научная революция: что это такое и какие исторические изменения она принесла?
Типы и примеры термодинамических процессов
термодинамические процессы это физические или химические явления, которые включают поток тепла (энергии) или работу между системой и ее окружением. Говоря о тепле, рационально приходит на ум образ огня, который является явным проявлением процесса, который выделяет много тепловой энергии..
Система может быть как макроскопической (поезд, ракета, вулкан), так и микроскопической (атомы, бактерии, молекулы, квантовые точки и т. Д.). Это отделено от остальной части вселенной, чтобы рассмотреть тепло или работу, которая входит или покидает это.
Однако существует не только тепловой поток, но системы также могут генерировать изменения в некоторой переменной их среды в ответ на рассматриваемое явление. Согласно термодинамическим законам, между реакцией и теплом должна быть компенсация, чтобы вещество и энергия всегда сохранялись..
Тем не менее, термодинамические модели стремятся соединить оба мира, контролируя такие переменные, как давление, объем и температуру систем, сохраняя некоторые из этих констант для изучения влияния других..
Затем, выражая изменения между системным окружением в зависимости от этих переменных, другие могут быть определены как работа (PV = W), необходимая для машин и производственных процессов..
С другой стороны, другой тип термодинамической переменной представляет больший интерес для химических явлений. Они напрямую связаны с выделением или поглощением энергии и зависят от внутренней природы молекул: образования и типов связей..
Системы и явления в термодинамических процессах
На изображении выше представлены три типа систем: закрытые, открытые и адиабатические..
В замкнутой системе нет переноса вещества между ним и его окружением, так что материя не может ни войти, ни выйти; однако энергия может пересекать границы коробки. Другими словами: феномен F может выделять или поглощать энергию, изменяя тем самым то, что находится за пределами коробки..
С другой стороны, в открытой системе горизонты системы имеют свои пунктирные линии, что означает, что и энергия, и материя могут приходить и уходить между этим и окружающим миром..
Физико-химические явления
Какая разница? Вкратце: первое не разрывает и не создает новые ссылки, а второе делает.
Таким образом, термодинамический процесс может рассматриваться в зависимости от того, является ли это явление физическим или химическим. Тем не менее, оба имеют общее изменение в некоторых молекулярных или атомных свойствах.
Примеры физических явлений
Нагрев воды в горшке вызывает увеличение столкновений между его молекулами до точки, где давление ее паров равно атмосферному давлению, и затем происходит фазовое изменение от жидкости к газу. Другими словами: вода испаряется.
Здесь молекулы воды не разрушают ни одной из своих связей, но подвергаются энергетическим изменениям; или что то же самое, внутренняя энергия U воды модифицируется.
Каковы термодинамические переменные для этого случая? Атмосферное давление Рбывший, температура, образующаяся при сжигании кулинарного газа, и объем воды.
Что если вы положите воду с бобами в скороварку? В этом случае объем остается постоянным (пока давление не сбрасывается при варке зерна), но давление и температура изменяются.
Это связано с тем, что добываемый газ не может вырваться и вращается на стенках котла и поверхности жидкости. Мы говорим о другом физическом явлении, но в изохорном процессе.
Примеры химических явлений
Было упомянуто, что существуют термодинамические переменные, присущие микроскопическим факторам, таким как молекулярная или атомная структура. Каковы эти переменные? Энтальпия (H), энтропия (S), внутренняя энергия (U) и свободная энергия Гиббса (S).
Эти внутренние переменные вещества определены и выражены в терминах макроскопических термодинамических переменных (P, T и V) в соответствии с выбранной математической моделью (обычно модель идеального газа). Благодаря этому можно проводить термодинамические исследования химических явлений..
Например, мы хотим изучить химическую реакцию типа A + B => C, но реакция происходит только при температуре 70 ° C. Кроме того, при температуре выше 100 ° С вместо образования С образуется D.
В этих условиях реактор (сборка, в которой проводится реакция) должен гарантировать постоянную температуру около 70 ° C, поэтому процесс является изотермическим.
Типы и примеры термодинамических процессов
Адиабатические процессы
Это те, в которых нет чистой передачи между системой и ее окружением. Это в долгосрочной перспективе гарантируется изолированной системой (коробкой внутри пузыря).
примеров
Примером этого являются калориметры, которые определяют количество тепла, выделяемого или поглощаемого в результате химической реакции (сгорания, растворения, окисления и т. Д.)..
Внутри физических явлений происходит движение, которое генерирует горячий газ из-за давления на поршни. Аналогично, когда поток воздуха давит на земную поверхность, его температура увеличивается, так как он вынужден расширяться.
С другой стороны, если другая поверхность является газообразной и имеет более низкую плотность, ее температура будет уменьшаться, когда она чувствует более высокое давление, заставляя его частицы конденсироваться.
Адиабатические процессы идеальны для многих промышленных процессов, в которых меньшие потери тепла означают более низкую производительность, что отражается на затратах. Чтобы рассматривать это как таковой, тепловой поток должен быть нулевым, или количество тепла, которое входит, должно быть равным количеству, которое входит в систему..
Изотермические процессы
примеров
Примеры этого типа термодинамического процесса неисчислимы. По сути, большая клеточная активность происходит при постоянной температуре (обмен ионов и воды через клеточные мембраны). В пределах химических реакций все те, которые устанавливают тепловые равновесия, считаются изотермическими процессами..
Человеческому метаболизму удается поддерживать постоянную температуру тела (приблизительно 37 ° C) посредством широкого спектра химических реакций. Это достигается благодаря энергии, получаемой из пищи.
Фазовые изменения также являются изотермическими процессами. Например, когда жидкость замерзает, она выделяет тепло, предотвращая снижение температуры до тех пор, пока она полностью не окажется в твердой фазе. Как только это произойдет, температура может продолжать снижаться, потому что твердое вещество больше не выделяет энергию.
В тех системах, где используются идеальные газы, изменение внутренней энергии U равно нулю, поэтому все тепло используется для выполнения работы..
Изобарические процессы
В этих процессах давление в системе остается постоянным, варьируя ее объем и температуру. Как правило, они могут возникать в системах, открытых для атмосферы, или в закрытых системах, пределы которых могут быть деформированы увеличением объема, чтобы противодействовать увеличению давления..
примеров
В цилиндрах внутри двигателей, когда газ нагревается, он толкает поршень, который изменяет объем системы.
Если бы это было не так, давление увеличилось бы, так как система не имеет возможности уменьшить столкновения газообразных частиц на стенках цилиндра..
Изохорные процессы
В изохорных процессах объем остается постоянным. Его также можно рассматривать как те, в которых система не генерирует работу (W = 0).
По сути, это физические или химические явления, которые изучаются в любом контейнере, с возбуждением или без.
примеров
Примерами этих процессов являются приготовление пищи, приготовление кофе, охлаждение бутылки с мороженым, кристаллизация сахара, растворение мало растворимого осадка, ионообменная хроматография и другие..
Что такое изотермический процесс? (Примеры, упражнения)
Содержание:
Эти изменения представляют собой фазовые переходы, когда вещество переходит из твердого состояния в жидкое, из жидкого в газообразное или наоборот. В таких случаях молекулы вещества меняют свое положение, добавляя или извлекая тепловую энергию.
Тепловая энергия, необходимая для возникновения фазового перехода в веществе, называется скрытой теплотой или теплотой превращения.
Этот тип процесса часто встречается в природе. Например, у людей, когда температура тела повышается или понижается, мы чувствуем себя больными, потому что в нашем теле многие химические реакции, поддерживающие жизнь, происходят при постоянной температуре. Это справедливо для теплокровных животных в целом.
Примеры изотермических процессов
— Обмен веществ у теплокровных животных осуществляется при постоянной температуре.
— Когда вода закипает, происходит фазовый переход от жидкости к газу, а температура остается постоянной примерно на уровне 100 º C, поскольку на значение могут влиять другие факторы.
-Автомобильные двигатели, холодильники, а также многие другие виды техники исправно работают в определенном температурном диапазоне. Для поддержания нужной температуры устройства называли термостаты. В его конструкции использованы различные принципы работы.
Цикл Карно
Двигатель автомобиля работает по аналогичным принципам. Движение поршня внутри цилиндра передается другим частям автомобиля и вызывает движение. Он не имеет поведения идеальной системы, такой как двигатель Карно, но термодинамические принципы являются общими.
Расчет работы, проделанной в изотермическом процессе
Чтобы рассчитать работу, совершаемую системой при постоянной температуре, мы должны использовать первый закон термодинамики, который гласит:
Это еще один способ выражения сохранения энергии в системе, представленный через ΔU или изменение энергии, Q по мере поступления тепла и, наконец, W, что и есть работа, проделанная указанной системой.
Предположим, что рассматриваемая система представляет собой идеальный газ, содержащийся в цилиндре подвижного поршня площадью К, который работает, когда его объем V смена V1 к V2.
Итак, проделанная работа рассчитывается путем интегрирования небольшой дифференциальной работы, в которой сила F производит небольшое смещение dx:
Как Adx это именно изменение объема dV, так:
Чтобы получить полную работу в изотермическом процессе, проинтегрируем выражение для dW:
Давление п и объем V изображены на диаграмме P-V как показано на рисунке, а проделанная работа равна площади под кривой:
Как ΔU = 0 поскольку температура остается постоянной, в изотермическом процессе необходимо:
— Упражнение 1
Цилиндр с подвижным поршнем содержит идеальный газ при 127ºC. Если поршень движется, чтобы уменьшить начальный объем в 10 раз, сохраняя постоянную температуру, найдите количество молей газа, содержащегося в цилиндре, если работа, проделанная с газом, равна 38 180 Дж.
Факт: R = 8,3 Дж / моль. K
Решение
В заявлении говорится, что температура остается постоянной, поэтому мы находимся в наличии изотермического процесса. Для работы, проделанной с газом, мы имеем ранее выведенное уравнение:
127 º C = 127 + 273 K = 400 K
Решите относительно n количество родинок:
Работе предшествовал отрицательный знак. Внимательный читатель заметит в предыдущем разделе, что W было определено как «работа, выполняемая системой» и имеет знак +. Так что «проделанная работа над системой» имеет отрицательный знак.
— Упражнение 2.
У вас есть воздух в цилиндре с поршнем. Изначально есть 0,4 м 3 газа под давлением 100 кПа и температурой 80ºC. Воздух сжимается до 0,1 м 3 обеспечение постоянной температуры внутри цилиндра во время процесса.
Определите, сколько работы было сделано во время этого процесса.
Решение
Мы используем ранее полученное уравнение для работы, но количество молей неизвестно, которое можно рассчитать с помощью уравнения идеального газа:
80 º C = 80 + 273 K = 353 K.
п1V1 = n.R.T → n = P1V1 / RT = 100000 Па x 0,4 м 3 /8,3 Дж / моль. K x 353 K = 13,65 моль
Опять же отрицательный знак указывает на то, что в системе были выполнены работы, что всегда происходит при сжатии газа.
Ссылки
Научная революция: что это такое и какие исторические изменения она принесла?
Содержание:
Первый закон термодинамики:
При изучении физики в 9 классе вы узнали, что полная механическая энергия замкнутой системы тел сохраняется только при отсутствии трения, а при наличии трения она уменьшается. Куда девается механическая энергия? Если бутылку, заполненную до половины водой при комнатной температуре, встряхивать в течение нескольких минут, то окажется, что вода нагрелась на 1—2 °С. Каким образом нагрелась вода?
В середине XIX века известный английский физик Дж. Джоуль (1818— 1889), проведя многочисленные опыты, показал, что совершённая при перемешивании воды механическая работа практически равна увеличению её внутренней энергии. Опыты Джоуля, а также исследования немецкого врача и естествоиспытателя Р. Майера (1814—1878), немецкого профессора физиологии и одного из самых знаменитых физиков второй половины XIX века Г. Гельмгольца (1821 —1894) позволили сформулировать закон сохранения и превращения энергии, распространив его на все явления природы. Согласно этому закону при любых взаимодействиях материальных объектов энергия не исчезает и не возникает из ничего, она только передаётся от одних объектов к другим или превращается из одной формы в другую.
Для термодинамических систем (в термодинамике обычно рассматривают макроскопически неподвижные системы) закон сохранения и превращения энергии называют первым законом термодинамики. Согласно первому закону термодинамики, приращение внутренней энергии термодинамической системы при переходе из одного состояния в другое равно алгебраической сумме работы, совершённой внешними силами, и количества теплоты, полученного или отданного системой при взаимодействии с внешними телами:
Поскольку работа внешних сил равна работе, совершаемой термодинамической системой, взятой с противоположным знаком (
Если система представляет собой действующее устройство, периодически возвращающееся в исходное состояние, то при этом AU-0 и A-Q. Механизм, который мог бы совершать работу без изменения состояния составляющих его тел и без теплопередачи от внешних тел, называют «вечным двигателем первого рода». Поэтому первый закон термодинамики можно сформулировать и следующим образом: невозможен вечный двигатель первого рода, т. е. такой двигатель, который при неизменном значении собственной внутренней энергии совершал бы работу большую, чем энергия, получаемая им извне.
Применим первый закон термодинамики к различным изопроцессам, происходящим с идеальным одноатомным газом.
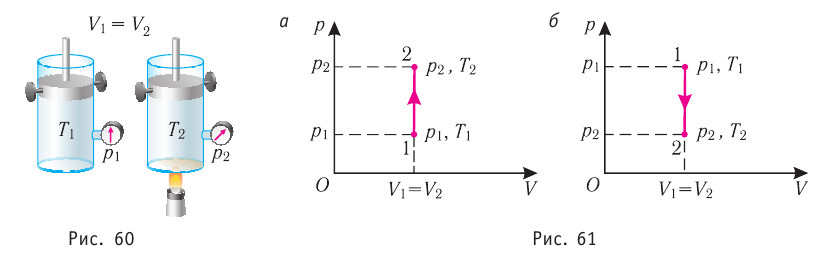
Изохорный процесс
Пусть идеальный одноатомный газ находится в цилиндрическом сосуде, закрытом неподвижным поршнем (V = const). Нагреем сосуд с газом. Объём газа остаётся практически постоянным (тепловым расширением сосуда пренебрегаем) (рис. 60), следовательно, работа силы давления газа А= 0. Тогда первый закон термодинамики примет вид 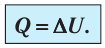
Это означает, что всё передаваемое газу количество теплоты идёт на увеличение его внутренней энергии. При этом приращение внутренней энергии газа 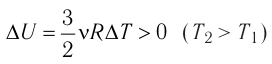
процессе отдаёт количество теплоты, то его внутренняя энергия убывает:
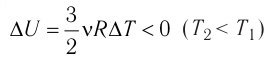
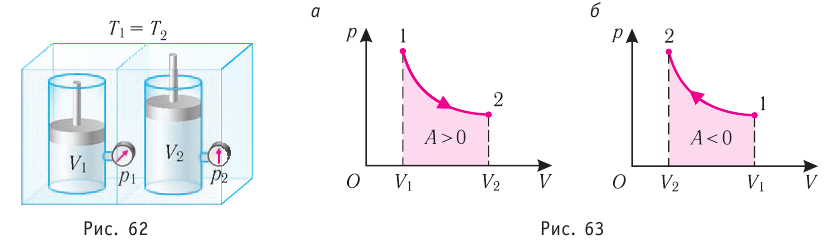
Изотермический процесс
Пусть цилиндрический сосуд с газом под поршнем находится в термостате — устройстве, в котором поддерживается постоянная температура. В этом случае внутренняя энергия идеального одноатомного газа 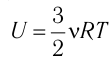
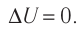
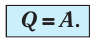
Какие выводы следуют из этого? Если с помощью внешнего устройства медленно перемещать поршень в сосуде так, чтобы объём газа увеличивался (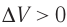
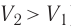
Если же внешнее устройство обеспечивает медленное уменьшение объёма газа в сосуде (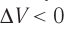
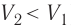
Изобарный процесс
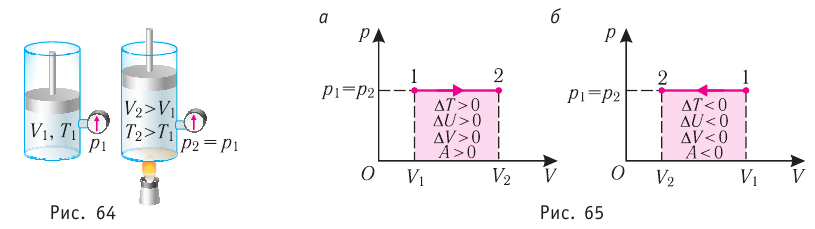
Пусть газ находится в цилиндрическом сосуде, закрытом поршнем, который может свободно или под постоянной нагрузкой перемещаться (рис. 64). Нагреем газ, передав ему некоторое количество теплоты (Q > 0). Согласно первому закону термодинамики (11.2) переданное газу количество теплоты частично расходуется на увеличение внутренней энергии 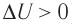
При изобарном процессе работа расширения (сжатия) газа 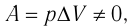
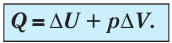
При изобарном сжатии газа внешние силы совершают работу А’ > 0. Чтобы давление газа при этом оставалось постоянным, газ необходимо охлаждать, т. е. он должен отдавать в окружающую среду некоторое количество теплоты (Q
При копировании любых материалов с сайта evkova.org обязательна активная ссылка на сайт www.evkova.org
Сайт создан коллективом преподавателей на некоммерческой основе для дополнительного образования молодежи
Сайт пишется, поддерживается и управляется коллективом преподавателей
Whatsapp и логотип whatsapp являются товарными знаками корпорации WhatsApp LLC.
Cайт носит информационный характер и ни при каких условиях не является публичной офертой, которая определяется положениями статьи 437 Гражданского кодекса РФ. Анна Евкова не оказывает никаких услуг.