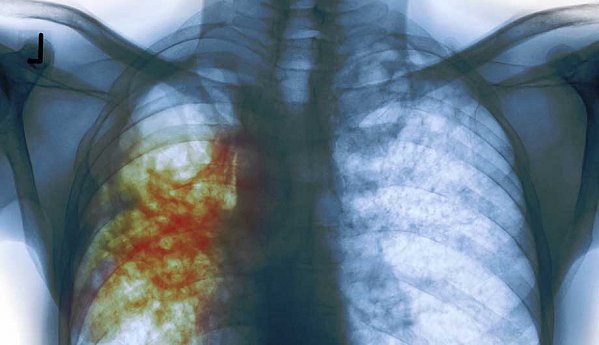
Туберкулез: формы, симптомы, диагностика, лечение
Туберкулез – это инфекционное заболевание, вызываемое палочкой Коха (Mycobacterium tuberculosis). Патоген чаще всего поражает легкие, но существуют и другие формы: туберкулез костей, суставов, почек, кожи и других органов.
Процент смертности от туберкулеза по всему миру высок, он входит в десятку заболеваний, приводящих к летальным исходам [1]. Это не только медицинская, но и социальная проблема, поскольку на заболеваемость, помимо состояния здоровья, также влияют социальные и экономические причины, качество питания и образ жизни. Ключевыми факторами риска считаются вредные привычки, ослабленная иммунная система и хронический стресс.
Как передается туберкулез
Возбудитель передается от человека к человеку воздушно-капельным путем при чихании и кашле и просто при разговоре, а также иногда контактно (через поврежденную кожу или внутриутробно). Бактерии туберкулеза долго сохраняются активными во внешней среде в плохо проветриваемом помещении и попадают в организм здорового человека через предметы быта и продукты питания.
Заражение туберкулезом еще не означает начало заболевания: оно развивается только у 5-15% инфицированных. До развития первых симптомов может пройти несколько недель или месяцев, и основным фактором риска считается ослабление иммунных сил организма [1].
Классификация туберкулеза
Симптомы туберкулеза
Признаки заражения различаются в зависимости от органа, пораженного микобактерией. Общие симптомы включают утомляемость, сниженную трудоспособность, плохой аппетит, повышенную температуру тела, потерю веса, появление румянца на щеках.
Клинические признаки туберкулеза у детей развиваются быстрее и более выражены. Риск заражения у этой группы пациентов выше. Это связано с возрастными особенностями строения органов и нестойкостью иммунитета ребенка к агрессивным инфекциям. Помимо «взрослых» симптомов у детей также отмечаются капризность, плаксивость, необоснованная беспокойность и нарушения сна.
Диагностика туберкулеза
Это заболевание, особенно закрытая форма, сложно диагностируется. Переход из латентной фазы в активную смазанный, а клинические симптомы не позволяют установить точный диагноз или отсутствуют. В связи с этим решающее значение имеет лабораторная диагностика.
Проба Манту (или туберкулиновая проба). Для проведения этого классического анализа на туберкулез пациенту подкожно в области предплечья вводят очищенный туберкулин – смесь белков, характерных для микобактерий. Оценку иммунологической реакции проводят через 48-72 часов на основании диаметра папулы (узелка над поверхностью кожи) или участка покраснения в месте введения туберкулина. У людей, неинфицированных бактерией, папулы не образуются или их размеры незначительны. К основным недостаткам метода относятся непереносимость туберкулина и ложноположительная реакция у людей, вакцинированных от туберкулеза вакциной БЦЖ.
Квантифероновый тест на туберкулез. Этот современный иммунологический метод позволяет выявить латентный туберкулез, а также туберкулезное поражение других органов. Введения туберкулина не требуется, поэтому этот тест подходит уязвимым группам пациентов (беременные и кормящие женщины, пожилые люди, ВИЧ-инфицированные, люди с непереносимостью туберкулина). Для диагностики используется венозная кровь. Наличие в организме активного туберкулеза обуславливает появление в крови особых белков, входящих в состав микобактерий. Т-лимфоциты реагируют на присутствие этих белков и в результате такой сенсибилизации начинают усиленно вырабатывать интерферон-гамма. Квантифероновый тест основан на измерении уровня интерферона-гамма, повышение которого указывает на наличие туберкулезной инфекции в пробе крови.
Метод T-SPOT.TB. Позволяет диагностировать латентную и активную формы легочного и внелегочного туберкулеза. Для исследования используют венозную кровь. В основе метода лежит оценка количества самих сенсибилизированных Т-лимфоцитов. Он также не дает ложноположительных результатов и подходит уязвимым группам пациентов.
Анализ мокроты. Для проведения теста необходимо собрать утреннюю мокроту, которая отделяется при кашле. Во взятом образце определяют наличие самих микобактерий. Анализ подходит только для диагностики туберкулеза легких.
Анализ мочи. Выявляют изменения параметров, характерные для туберкулеза: появление лейкоцитов, эритроцитов, бактерий, белка, гноя, сдвиг реакции мочи в кислую сторону.
Отрицательные лабораторные анализы не гарантируют отсутствие туберкулеза. Пациенты с подозрением на заболевание проходят флюорографию и/или рентгенографию легких. Для выявления внелегочных форм туберкулеза проводят МРТ, КТ и другие инструментальные исследования. Также применяют биопсию (взятие образца тканей) для микроскопических исследований и посевов на питательные среды.
Дифференциальную диагностику проводят с широким рядом заболеваний в тех случаях, когда ни одно исследование не подтвердило наличие микобактерий, присутствуют атипичные симптомы или отсутствует адекватный ответ на противотуберкулезное лечение.
Лечение туберкулеза
Полное выздоровление не гарантирует отсутствие рецидива заболевания в будущем.
Туберкулез
Туберкулез передается воздушно-капельным путем от человека к человеку. При кашле, чихании или отхаркивании люди больные легочной формой туберкулеза выделяют бактерии, для инфицирования достаточно вдохнуть лишь незначительное их количество. Инфекция может попасть в организм человека из-за нарушения правил гигиены: немытые руки после контакта с поручнями в общественном транспорте, употребление в пищу грязных овощей и фруктов, плохо обработанных продуктов животного происхождения могут стать причиной заражения.
Около одной четверти населения мира имеют латентную форму туберкулеза, то есть эти люди инфицированы бактериями туберкулеза, но (пока еще) не заболели этой болезнью и не являются источниками её распространения. Инкубационный период может продолжаться до 2 лет, заболевание часто протекает в бессимптомной или скрытой форме, однако при отсутствии должного лечения заканчивается переходом в активную.
Развитию туберкулеза способствуют факторы, снижающие защитные силы организма: хронические заболевания (сахарный диабет, язвенная болезнь, заболевания легких и почек), лечение гормонами и противоопухолевыми препаратами, ВИЧ в отсутствии противовирусной терапии, вредные привычки, стресс, некачественное питание, голодание, плохие бытовые условия жизни.
Классификация заболевания
Симптомы туберкулеза
Общими симптомами активного легочного туберкулеза являются кашель, иногда с мокротой и кровью, боль в груди, слабость, потеря веса, лихорадка и ночной пот. Больной может жаловаться на длительный кашель, который длится более трех недель, боли в грудной клетке, потерю аппетита и потерю массы тела, потоотделение в ночное время, общее недомогание и слабость, периодическое повышение температуры тела, появление крови в мокроте. У некоторых заразившихся палочкой Коха не проявляются симптомы заболевания и заболевание протекает в так называемой “закрытой” форме.
Для туберкулеза мозговых оболочек характерны нарушение кровоснабжения мозга, повышенное внутричерепное давление, отек мозга. Больной становится раздражительным, апатичным, быстро утомляется, страдает от головных болей. Если микобактерии внедрились в кишечник, то человеек может жаловаться на диарею, боли в животе, вздутие. В дальнейшем может развиться кишечная непроходимость или кишечное кровотечение.
Из всего опорно-двигательного аппарата чаще всего поражаются позвонки и кости таза. При распространении туберкулеза на сустав и окружающие его ткани возникают постоянные боли в суставе, ограничение его подвижности.
Симптомы туберкулеза почки, мочевыводящих путей и половых органов схожи с симптомами воспалительного процесса мочеполовой системы: тяжесть вниз живота, зуд, жжение, рези при мочеиспускании.
Туберкулез кожи проявляется изменением цвета и текстуры кожи, гнойными незаживающими ранами на коже, увеличением рядом расположенных к очагу инфекции лимфоузлов.
Диагностика туберкулеза
Как и при любом заболевании, диагностика начинается со сбора анамнеза и анализа жалоб пациента, изучения истории болезни. Для подтверждения или опровержения диагноза проводят ряд обследований:
С помощью рентгенографии и флюорографии определяют наличие очагов воспаления в тканях легких.
Лечение туберкулеза
Лечение длительное, комплексное, состоит из антибактериальных препаратов, противотуберкулезных средств, иммуномодуляторов, иммуностимуляторов, пробиотиков и витаминотерапии. Больному обязательно назначают специальное лечебное питание и рекомендуют занятия физкультурой, в частности кардиотренировки.
Препаратами выбора являются стрептомицин, изониазид, рифампицин (рифабутин), этамбутол и пиразинамид. Дозу лекарства и длительность лечения назначает врач. Как правило, в начале лечения применяются одновременно 4—5 указанных препаратов. Лечение активной стадии проводится в туберкулезном диспансере, так как пациент является заразным для окружающих. Длительность пребывания зависит от вида и стадии заболевания и может составлять от нескольких месяцев до нескольких лет. Самостоятельное прекращение лечения чаще всего приводит к рецидиву или дальнейшему развитию болезни, возникновению тяжелых осложнений, летальному исходу.
Роспотребнадзор (стенд)
Роспотребнадзор (стенд)
Туберкулез: опасность заболевания, меры профилактики, выявления и лечения
Туберкулез: опасность заболевания,
меры профилактики, выявления и лечения
Что такое туберкулез?
Туберкулез – инфекционное заболевание, вызываемое микобактериями туберкулеза, которые часто называют палочками Коха.
Заболевание развивается только в ответ на размножение в организме человека этих микробов.
Как можно заразиться туберкулезом?
Основным источником заражения туберкулезом является человек, который болеет туберкулезом легких.
Из дыхательных путей, особенно во время кашля, отделяется мокрота, содержащая микобактерии туберкулеза. Мелкие капли мокроты могут попадать в дыхательные пути здорового человека, находящегося рядом. Мокрота может оседать на поверхности пола или земли, на предметах и вещах.
Инфекция может попасть в организм человека вследствие нарушения правил гигиены – например, если не вымыть руки после контакта с поручнями в общественном транспорте или употреблять в пищу немытые овощи и фрукты, плохо обработанное мясо и некипяченое молоко.
Что же происходит при вдыхании туберкулезных палочек?
В большинстве случаев, если иммунная система человека находится в норме, вдыхание туберкулезных палочек не приводит к заболеванию в активной стадии.
К попавшим в дыхательные пути микобактериям устремляется целое войско клеток-защитников, которые поглощают и убивают большую часть болезнетворных микроорганизмов. Но некоторые микобактерии могут уцелеть и в течение долгого времени оставаться неактивными.
Таким образом, «нападение» болезнетворных организмов на организм остается без последствий. Однако спустя месяцы и даже годы, при ослаблении иммунитета в результате какой-либо другой болезни, недостаточного питания или стресса, бактерии туберкулеза начинают размножаться, уничтожая своей массой клетку-хозяина и полагая начало развитию активного туберкулеза.
В некоторых случаях при первом же попадании инфекции в организм бактерии могут размножаться, вызывая серьезные повреждения легочной ткани. Это случаи активного легочного туберкулеза, который может стать источником дальнейшего распространения инфекции.
В ряде случаев болезнетворные бактерии, попав в легкие, могут по лимфатическим сосудам или с током крови переноситься в другие части тела, попадая в почки, кости и суставы, мозг и т.д.
При хороших защитных силах организма микобактерии остаются в неактивном состоянии долгое время, но при ослаблении организма в этих частях тела также может развиться туберкулез.
Что может снизить защитные силы вашего организма?
Если в дыхательные пути попадёт слишком большое количество туберкулезных палочек-микобактерий, организм может не справиться с таким натиском.
Если Вы длительное время общаетесь с больным туберкулёзом, ваш организм подвергается постоянным атакам, и может настать момент, когда он больше не сможет эффективно сопротивляться инфекции.
Известны также другие факторы, содействующие развитию микобактерий в организме:
Дети, подростки, беременные женщины и пожилые люди более подвержены инфекции.
Как уберечься от заболевания?
Чтобы не заболеть туберкулезом, необходимо вести здоровый образ жизни. Для крепкого здоровья нужна здоровая нервная система, поэтому важно избегать стрессов.
Пища должна быть полноценной, обязательно должна содержать достаточное количество белков. Важным условием для поддержки здоровья должна быть ежедневная нормальная физическая нагрузка.
Пыльные непроветриваемые помещения благоприятствуют распространению туберкулезных бактерий. Для профилактики заболевания необходимо проветривать помещения.
Где можно пройти обследование?
Флюорографическое обследование грудной клетки можно сделать в поликлинике по месту жительства. При подозрении на туберкулез участковый врач или врач-специалист после клинического дообследования направит на консультацию к фтизиатру в противотуберкулезный диспансер или тубкабинет медицинского учреждения.
Кто должен чаще осматриваться на туберкулез?
Существует несколько уязвимых групп граждан и профессиональных категорий специалистов, которые в силу различных причин должны чаще обследоваться на туберкулез.
Два раза в год должны проходить осмотр:
Один раз в год должны проходить обязательный осмотр на туберкулез:
Кроме того, в индивидуальном (внеочередном) порядке осматриваются:
Как уберечь ребёнка от заболевания туберкулезом?
Снизить риск заболевания туберкулезом ребёнка можно проведением вакцинации БЦЖ, которая является обязательной и проводится бесплатно всем детям в роддоме с 3-х суток жизни (при отсутствии медицинских противопоказаний).
Дети, не привитые в роддоме, прививаются в отделениях патологии новорожденных или в условиях детской поликлиники, при этом в возрасте старше 2-х месяцев перед прививкой БЦЖ необходимо предварительно поставить пробу Манту с 2 ТЕ и прививка проводится в случае отрицательной пробы.
Повторные прививки – ревакцинация БЦЖ – проводится в 7 лет и 14 лет. Если у ребенка или подростка в декретированный возраст (7 и 14 лет) имелся медицинский отвод или проба Манту с 2 ТЕ была сомнительной (а это также является противопоказанием к проведению прививки), то ревакцинация против туберкулеза проводится в течение одного года после наступления указанного возраста.
Ревакцинация БЦЖ проводится неинфицированным микобактериями туберкулеза (МБТ) туберкулинотрицательным детям и подросткам.
Если у ребенка или подростка не сформировался постпрививочный знак (рубчик) или его размер менее 2-х мм, то при отрицательной пробе Манту с 2 ТЕ через 2 года после вакцинации и через 1 год после ревакцинации проводится повторная прививка против туберкулеза.
Для своевременного выявления инфицирования туберкулезом всем детям в РФ ежегодно проводится туберкулиновая проба Манту.
Часто болеющие дети или дети, имеющие хронические заболевания, составляют группу риска по туберкулезу.
Этой категории ребят уделяется особое внимание, проводятся дополнительные лечебно-профилактические мероприятия, которые определяет участковый врач, врач-специалист, медицинский работник детского учреждения.
При наличии медицинских показаний ребенок направляется на консультацию к фтизиатру по месту жительства. Для того чтобы оградить ребенка от заболевания, сами взрослые должны быть уверены, что они ЗДОРОВЫ, и своевременно проходить медицинские осмотры.
Как определить, что есть заболевание?
Основные симптомы, характерные для туберкулеза:
Если Вы обнаружили у себя эти симптомы, немедленно обращайтесь к врачу!
Могу ли я заразить окружающих?
Больной человек является источником инфекции, пока не приступит к интенсивному лечению.
Но как только лечение начато, опасность инфицировать окружающих быстро снижается. Это может подтвердить анализ мокроты на туберкулезные палочки. Если их не удается обнаружить при микроскопическом исследовании, то риск заражения для родных и близких в случае Вашего заболевания невелик.
Однако если Вы начали прием противотуберкулезных таблеток, очень важно завершить полный курс лечения, то есть принять все без исключения прописанные лекарства без перерыва даже в том случае, если Вы начнете чувствовать себя лучше.
В отличие от других заболеваний лечение туберкулеза требует приема нескольких специальных антибиотиков в течение длительного времени.
Причина этого – наличие трех разных по своей активности групп туберкулезных бактерий:
1) Активно размножающиеся бактерии в открытых полостях. Они выходят с мокротой, делая больного источником инфекции для окружающих.
2) Медленно размножающиеся бактерии в защитных клетках организма, окружающих открытые полости.
3) Бактерии в плотных очагах, которые большую часть времени «дремлют», но при отсутствии соответствующего лечения могут активизироваться и также наносить большой вред организму.
Также очень важно не пропускать прием таблеток и не прерывать лечение. Если курс лечения будет не завершен или прерван, погибнет только часть бактерий, а оставшиеся выработают устойчивость к препаратам и оденутся в непробиваемую для привычных лекарств броню.
Болезнь не будет излечена, а просто перейдет в форму, устойчивую к лекарственному воздействию, которая еще более опасна как для Вас, так и для окружающих Вас людей.
Если Вы пропустили прием таблеток, как можно скорее сообщите об этом Вашему лечащему врачу, он посоветует, как избежать неприятных последствий.
Также очень важно сообщить врачу о любых признаках побочных эффектов при приеме лекарств, таких как сыпь, желтуха, расстройство зрения или ухудшение слуха, желудочно-кишечные расстройства, покалывание в кончиках пальцев на руках и ногах. Врач даст Вам нужный совет.
В преодолении инфекции очень важно состояние общего здоровья, поэтому воздержитесь от алкоголя и курения (или, по крайней мере, уменьшите их прием).
Старайтесь больше отдыхать, правильно и полноценно питаться, дышите свежим воздухом. Никогда не сплевывайте на пол или на дорогу, используйте для этого вашу индивидуальную плевательницу. Проветривайте время от времени помещение, в котором находитесь. Кашляя, прикрывайте рот платком.
Будьте внимательны к родным и близким. Если Вы заметили у кого-либо симптомы туберкулеза, посоветуйте немедленно обратиться к врачу.
Излечим ли туберкулез?
В настоящее время имеется много противотуберкулезных препаратов, прием которых позволяет полностью излечить болезнь.
Главными условиями лечения туберкулеза являются своевременное выявление путем профилактических осмотров и раннее обращение больных за специализированной медицинской помощью к врачу-фтизиатру.
Больной туберкулезом должен своевременно принимать лечение в полном объеме, предписанном ему врачом.
Перерывы в лечении приводят к развитию устойчивой к лекарствам формы туберкулеза, вылечить которую намного сложнее.
Как долго больной туберкулезом должен лечиться?
Больной должен полноценно пролечиться не менее 6–8 месяцев: в течение 2–3 месяцев в туберкулезном стационаре, затем в условиях дневного стационара при туберкулезном кабинете и потом амбулаторно.
Противотуберкулезные препараты очень дорогие, но больному они предоставляются бесплатно. Если больной прекратит лечение досрочно или не будет принимать все прописанные ему лекарства, это приводит к возникновению лекарственной устойчивости и впоследствии микобактериями туберкулеза с лекарственной устойчивостью могут быть инфицированы члены семьи больного и окружающие.
Устойчивость к одному препарату поддается лечению другими противотуберкулезными препаратами.
А вот когда возникает резистентность к нескольким основным противотуберкулезным препаратам, это представляет значительную опасность и для больного, и для общества.
Лечить больных с множественной устойчивостью палочки Коха сложно и чрезвычайно дорого (курс лечения стоит в 100–150 раз дороже обычного курса лечения), длительность лечения может достигать нескольких лет и далеко не всегда оно оказывается успешным: можно потерять не только легкое (после оперативного вмешательства), но и жизнь.
Поэтому главное – соблюдение больными предписанных сроков и методов лечения и прием всех препаратов, которые прописал фтизиатр.
Что делать, если в семье есть больной туберкулезом?
Если в семье есть больной туберкулезом, то прежде всего он сам должен осознавать, что от его культуры и дисциплинированности очень многое зависит. Естественно, больной должен выполнять правила личной гигиены.
Но не меньшее значение имеет грамотность в вопросах гигиены всех членов семьи и близких, проживающих в очаге туберкулеза.
Больной должен иметь свою комнату, а если нет такой возможности, то свой угол. Кровать следует поставить поближе к окну, отгородить ее ширмой. Нельзя спать на диване, которым днем пользуются другие члены семьи, на котором играют дети. У больного должна быть своя посуда, все вещи следует хранить отдельно. Плевательницу должен обрабатывать сам больной.
Как помочь больному, как дезинфицировать его вещи, делать уборку в помещении, обрабатывать мокроту – об этом расскажут в туберкулезном диспансере. Вся семья больного должна наблюдаться в диспансере по контакту, вовремя обследоваться и проходить профилактические курсы лечения в соответствии с рекомендациями фтизиатра.
Нужно ли обрабатывать квартиру, если раньше там жил больной туберкулезом?
Микобактерии туберкулеза долго сохраняют свою жизнеспособность в окружающей среде, особенно во влажных и запыленных помещениях.
Губительными для микобактерий являются длительное ультрафиолетовое излучение и дезинфицирующие средства.
Лучше, чтобы обработку помещения по заказу провели специалисты дезинфекционной службы. Если в Вашем населенном пункте нет дезслужбы, то получить консультацию по правильной обработке помещения своими силами Вы сможете у фтизиатра.
Туберкулез и микобактериоз. Общая информация
Туберкулез у человека вызывают микобактерии туберкулеза (МБТ): M.tuberculosis, M.bovis, M.africanum, M.microti, M.canettii, M.caprae, M.pinnipedii, M. mungi, объединяемые в группу микобактерий, называемую Mycobacterium tuberculosis complex, к которой также относится вакцинный штамм M.bovis BCG. Преобладающим этиологическим агентом является M.tuberculosis. Кроме абсолютно-патогенных для человека микобактерий, к которым кроме МБТ относится микобактерия лепры, существуют еще нетуберкулезные микобактерии (НТМБ), около 30 видов которых являются условно-патогенными для человека, прочие являются сапрофитами. Все НТМБ являются убиквитарными – т. е. повсеместно распространенными в окружающей среде.
Микобактерии (МБ) отличаются высокой устойчивостью к воздействию физикохимических факторов. До полугода они могут сохраняться на объектах окружающей среды, в пыли, на страницах книг, в почве и воде, причем высушивание увеличивает их жизнеспособность. В высушенной мокроте МБТ сохраняют жизнеспособность в течение 10–12 месяцев и погибают при нагревании до 100. С только через 45 мин, а при 70. С – через 7 часов. Низкие температуры также способствуют сохранению жизнеспособных МБ – в масле и сыре при низких температурах они живут до 1 года.
Туберкулез (ТБ) – антропозоонозное инфекционное гранулематозное заболевание. Передается в большинстве случаев аэрогенным (воздушно-капельным или воздушно-пылевым), но встречаются также алиментарный, контактный и трансплацентарный пути заражения. Следует помнить о возможности перекрестного заражения ТБ человека и животных. Микобактериоз – заболевание, вызванное другими представителями рода Mycobacterium – НТМБ, которые могут передаваться от человека к человеку, но основным источником инфицирования служат сельскохозяйственные животные.
Оба заболевания характеризуются политропностью, т. е. в организме человека и животных при развитии патологического процесса могут поражаться различные органы. Более чем в 80% случаев развивается легочная форма заболеваний, в остальных случаях – внелегочная или сочетанные формы. Внелегочный ТБ, как правило, развивается вторично, в результате распространения туберкулезной инфекции из первичного очага, локализующегося обычно в органах дыхания. При этом первичный ТБ может быть отсроченным по времени с эпизодом проявления внелегочного ТБ и разрешиться ранее, либо вследствие проведения противотуберкулезной терапии, либо самостоятельно, без ее применения.
Заболеваемость туберкулезом в Российской Федерации в настоящее время высокая: 82,4–84,0 на 100 тыс. населения. Растет и число больных с резистентными к стандартной терапии штаммами МБТ. Особую угрозу туберкулез представляет для больных с иммунодефицитными состояниями, при которых он может протекать атипично, создавая трудности для клинико-лабораторной диагностики.
Среди контингента больных ВИЧ-инфекцией в РФ постоянно увеличивается число больных с поздними стадиями ВИЧ-инфекции. Это приводит к тому, что у все большего числа больных ВИЧ-инфекцией россиян, инфицированных МБТ, на фоне иммунодефицита развивается туберкулез. При этом туберкулез – главная причина смерти умерших от причин, связанных с ВИЧ-инфекцией (63,4% в 2010 г. по данным МЗ РФ). Европейское региональное бюро ВОЗ относит Россию к числу стран с наиболее неблагоприятной ситуацией по туберкулезу, сочетанному с ВИЧинфекцией.
Наиболее частыми этиологическими причинами микобактериозов у больных ВИЧ-инфекцией является Mycobacterium avium complex, M. xenopi, M. kansasii, M. fortuitum. Клинические формы этих поражений развиваются исключительно у лиц с выраженным иммунодефицитом. Диагностика легочного и внелегочного ТБ, а также микобактериоза, зависит от настороженности врачей, в первую очередь общей лечебной сети, а также доступности специальных методов исследования. Согласно приказу № 1224н от 29 декабря 2010 г. медицинские работники любых специальностей медицинских организаций РФ должны выявлять симптомы туберкулеза. При подозрении на туберкулез органов дыхания или внелегочной локализации в медицинских организациях проводится лабораторное исследование разных видов биологического материала, преимущественно – выявление возбудителя заболевания методом микроскопии.
Для защиты от ТБ применяется вакцинация, проведение которой регулируется федеральным законодательством. Вакцина представляет собой аттенуированный штамм M.bovis – M.bovis BCG. В ряде случаев вакцинация может вызывать осложнения, т.н. БЦЖ-иты.
ТБ в мире классифицируется в соответствии с МКБ-10, которая учитывает лишь метод подтверждения диагноза и локализацию процесса, и определяется кодами А15 – А19. В России существует собственная классификация, отражающая клинико- морфологические особенности патогенеза. В ее основу положены несколько принципов: клинико-рентгенологические особенности туберкулезного процесса (в т. ч. локализация и распространенность), его течение (т. е. фазы), а также наличие бактериовыделения. В приказе Минздрава РФ от 21.03.2003 № 109 «О совершенствовании противотуберкулезных мероприятий в Российской Федерации» сделана попытка совмещения обеих классификаций, когда к 4 знакам шифра МКБ-10 добавлено еще 6 знаков, в которых нашли отражение уточнения отечественной классификации.
Заболевания, вызванные НТМБ, а также другими представителями порядка Actinomycetales, имеющими близкое генетическое, иммунологическое, хемотаксономическое родство с МБ, микроорганизмами родов Nocardia, Rhodococcus, Corynebacterium и др., имеют сходную с ТБ локализацию патологического процесса, а также клиническую, в ряде случаев микробиологическую, и на определенных этапах патогенеза – морфологическую картины. Такие заболевания могут протекать под маской ТБ, что затрудняет его дифференциальную диагностику. Увеличивающееся в последнее время количество случаев заболеваний, вызванных подобными возбудителями, обусловлено увеличением количества иммунокомпрометированных лиц, а также развитием бактериологических и молекулярно-биологических методов исследования. Вопросы диагностики и лечения таких больных на законодательном уровне в РФ четко не обозначены.
Показания к обследованию
Дифференциальная диагностика. Первичная форма ТБ с поражением внутригрудных лимфатических узлов: саркоидоз I стадии, лимфогранулематоз, микобактериоз, лимфолейкоз, лимфосаркома, ретикулосаркома, центральный рак легкого, застойные изменения в легких на фоне сердечной недостаточности.
Диссеминированный ТБ: саркоидоз II стадии, бактериальная пневмония, профессиональные заболевания легких – пневмокониоз (силикоз и силикатоз, металлокониоз, карбокониоз, пневмокониоз, вызванные смешанной или органической пылью), микобактериоз, канцероматоз легких, фиброзирующий альвеолит, коллагенозы, гистиоцитоз Х, гемосидероз, криптококкоз, аспергиллез, гистоплазмоз, кокцидиоидоз, бластомикоз, гранулематоз Вегенера, хроническая интерстициальная пневмония, альвеолярный протеиноз, легочный васкулит.
Очаговый, инфильтративный ТБ и казеозная пневмония: внебольничная пневмония, периферический и центральный рак легкого, эозинофильный инфильтрат, актиномикоз легкого, нокардиоз, микобактериоз, ателектаз легкого, инфаркт легкого.
Кавернозный и фиброзно-кавернозный ТБ: абсцесс легкого, рак легкого с распадом, солитарные кисты легкого, бронхоэктазы, микобактериоз, нокардиоз.
Цирротический ТБ: саркоидоз III стадии и пневмофиброзы различной этиологии.
В случае округлых образований, наблюдаемых при рентгенологическом исследовании: периферический и метастатический рак, доброкачественные опухоли, эхинококкоз, аспергиллома, ретенционные кисты легкого, ограниченный осумкованный плеврит и артериовенозная аневризма легкого.
ТБ периферических лимфоузлов: саркоидоз, токсоплазмоз, микобактериоз, бруцеллез, болезнь Кикучи (гистиоцитарный некротизирующий лимфаденит), доброкачественный лимфоретикулез, лимфогранулематоз, неходжкинская лимфома.
У больных ВИЧ-инфекцией: вторичные заболевания, протекающие с поражением легких, генерализованные вторичные инфекции, онкологические поражения.
Материал для исследования
Мокрота, трахеальный смыв, материалы, полученные при проведении бронхоскопии – промывные воды бронхов, бронхоальвеолярный лаваж, а также материалы катетер- или щеточной биопсии, промывные воды желудка, экссудаты и транссудаты, гной, отделяемое ран, аспираты и пунктаты, спинномозговая и асцитическая жидкости, цельная кровь, моча, кал, секрет простаты, эякулят, менструальная кровь, ткани, в т.ч. фиксированные или в парафиновых блоках, смывы с предметов окружающей среды, а также культуры микроорганизмов, полученные при посеве этих видов материала для идентификации вида МБ.
Лабораторная диагностика туберкулеза и микобактериоза включает визуализацию кислото- и спиртоустойчивых бактерий при использовании микроскопии, получение первичной культуры или обнаружение ДНК/РНК МБ, их дальнейшее видовое дифференцирование и определение чувствительности возбудителя заболевания к противотуберкулезным препаратам культуральным методом или МАНК.
Сравнительная характеристика методов лабораторной диагностики и особенности интерпретации их результатов. По международным стандартам диагноз ТБ должен быть подтвержден бактериологически или гистологически.
Первоначальное исследование – микроскопия препарата мокроты или других жидкостей и тканей организма, взятых максимально близко к предполагаемой локализации патологического процесса. Микроскопия препарата с окраской по Цилю-Нильсену – быстрый, дешевый, но низко чувствительный метод (с его помощью можно обнаружить 105–106 микробных тел/мл), обладающий невысокой специфичностью, выявляющий все кислото- и спиртоустойчивые микроорганизмы. Метод не позволяет дифференцировать МБТ от НТМБ и, в ряде случаев, от других микроорганизмов порядка Actinomycetales. Диагностическая чувствительность метода составляет 20–65%.
Люминесцентная микроскопия препарата с окраской флуорохромными красителями – более чувствительный метод, т. к. позволяет проводить исследование при меньших увеличениях микроскопа и, следовательно, просматривать значительно больше полей зрения, чем при обычной микроскопии с иммерсионной системой при окраске по Цилю-Нильсену, что позволяет увеличить процент положительных находок на 10–17%.
Бактериологический посев на плотные питательные среды обладает большей чувствительностью и выявляет 100–1000 микробных тел/мл. Согласно стандартам микробиологической диагностики, обязательный посев проводится на 2 питательные среды, одной из которых является яичная среда Левенштейна-Йенсена (по рекомендации ВОЗ). В результате медленного роста, когда каждое деление микобактерий, в зависимости от вида, происходит через 2–24 ч, для получения результата требуется от 7 дней для быстрорастущих и до 2–12 недель для медленнорастущих, в число которых входит и МБТ.
Посев на жидкие питательные среды с помощью автоматических анализаторов BACTEC MGIT 960 (Becton Dickinson Microbiology Systems, Sparks, MD) и VersaTREK Myco (Trek Diagnostic Systems, Westlake, OH), позволяет получить результат через 4–42 дня.
В 2010 году в документах CDC, МАНК, наряду с культуральным методом, предложено использовать для подтверждения диагноза туберкулеза. В то же время, использование методов микроскопии ограничивается и предлагается для применения только в случаях невозможности проведения посева, при получении ложноотрицательного результата посева или его контаминации (пророста). Модификация программного обеспечения «Vercrit», используемого в противотуберкулезной службе США, выстраивает следующую иерархию доказательной диагностики ТБ:
Трехкратное взятие и исследование образцов биологического материала у пациента, например мокроты, увеличивает возможность обнаружения МБТ на 2–5%. Поэтому в отечественных и зарубежных руководствах по диагностике ТБ указана необходимость трехкратного, или, по меньшей мере, двукратного исследования образцов мокроты. Сбор первого образца мокроты проводится в присутствии среднего медицинского персонала для объяснения правильной последовательности действий пациента. Второй образец больной собирает вечером того же дня, а третий утром, после чего приносит их в лабораторию. В случае госпитализации больного образцы собираются последовательно в течение 3-х дней.
Вместе с тем, обнаружение МБТ в экскретируемых организмом жидкостях не всегда возможно даже при многократном сборе и исследовании материала методом ПЦР, что связано с преимущественно тканевой локализацией возбудителя ТБ. Поэтому в сложных диагностических случаях больным показано проведение гистологической диагностики ТБ. Образец ткани из очага патологического процесса, после проведения гистологической проводки и заключения его в парафин, можно исследовать как для верификации специфического туберкулезного воспаления, так и для подтверждения этиологической причины патологического процесса. Исследования проводят с помощью окраски бактерий по Цилю-Нильсену, иммуногистохимического исследования, позволяющего отнести обнаруженные микроорганизмы к роду Mycobacterium, а также МАНК, определяющих их видовую принадлежность.
С целью дифференцирования МБ до вида, необходимого для правильного определения этиологии заболевания, анализируют морфологические характеристики выросшей культуры, проводят ее микроскопическое исследование с окраской препаратов по Цилю-Нильсену, после чего осуществляют биохимические тесты и пересев на селективные питательные среды. Такая стратегия требует много времени как для получения достаточного для анализа роста культуры, так и для осуществления используемых методик. Однако даже применение всех методов позволяет дифференцировать МБ с точностью, не превышающей 95%, что связано с индивидуальными особенностями штаммов.
Дифференцирование до вида целесообразнее осуществлять с помощью молекулярно- биологических методов: ПЦР; гибридизация с ДНК-зондами, выявляющая наиболее распространенные МБ; высокоэффективная жидкостная хроматография, сравнивающая профиль жирных кислот клеточной стенки анализируемого микроорганизма с имеющимися в базе данных; секвенирование 16S rDNA и ITS-региона МБ, результаты которого анализируются с помощью интернет-ресурса RIDOM ( http://rdna.ridom.de ). Для дифференцирования некоторых НТМБ, особенно быстрорастущих (M.fortuitum, M.abscessus, M.chelonae), обязательно ориентируются на данные антибиотикочувствительности и результаты секвенирования. Практически для всех технологий, за исключением ПЦР, в качестве материала для исследования применимы только первичные культуры МБ, выросших на плотных или жидких питательных средах
Не менее важно дифференцирование до вида внутри группы Mycobacterium tuberculosis complex. Это связано с необходимостью определения источника заболевания, определения дальнейшей тактики противотуберкулезной терапии (при индикации М.bovis или ее вакцинного штамма М.bovis BCG, которые отличаются природной резистентностью к одному из основных ПТП – пиразинамиду, этот препарат не назначается), а также для подтверждения поствакцинальных осложнений у пациента. МР № 99/219 «Диагностика поствакцинальных осложнений после введения вакцины БЦЖ» предлагают с этой целью использовать диагностический комплекс, предусматривающий последовательное применение двух методов: культурального и ИФА для обнаружения АГ полученной культуры с помощью моноклональных АТ, специфически взаимодействующих с поверхностными АГ М.bovis, но не связывающимися с АГ М.tuberculosis. Исследование включает определение морфологических особенностей штамма, его тинкториальных свойств, спирто- и кислотоустойчивости, видовой принадлежности и изучение его лекарственной чувствительности к ПТП с обращением особого внимания на чувствительность к пиразинамиду. Несмотря на то, что в МР написано, что использование диагностического комплекса при морфологической верификации диагноза позволяет в 100% случаев верифицировать диагноз «БЦЖит», очевидно, что данные методы не позволяют дифференцировать М.bovis от ее вакцинного штамма М.bovis BCG. С этой задачей успешно справляется набор реагентов, основанный на использовании метода ПЦР, который выявляет виды M.tuberculosis complex: M.tuberculosis, M.bovis и ее вакцинный штамм M.bovis BCG и др. непосредственно в разных видах биологического материала.
Для определения лекарственной чувствительности (ЛЧ) МБ к противотуберкулезным препаратам с помощью культурального метода используют первичную культуру МБ. Существует 3 основных метода непрямого определения ЛЧ МБ: метод пропорций, метод коэффициента устойчивости и метод абсолютных концентраций на плотных и жидких средах. В России и большинстве стран мира наиболее распространенным и традиционно используемым методом определения ЛЧ МБ является непрямой метод абсолютных концентраций на плотной яичной питательной среде Левенштейна–Йенсена. Остальные методы определения ЛЧ МБТ являются альтернативными. Основным недостатком традиционных культуральных методов определения ЛЧ МБТ, является их чрезвычайная длительность. Результаты исследования ЛЧ первичной культуры МБ учитываются через 3–4 недели инкубации для плотных и 4-13 дней для жидких питательных сред, поэтому необходимая коррекция химиотерапии может быть проведена не ранее, чем через 10–60 дней или 40–120 дней, в зависимости от используемых питательных сред, от момента поступления в лабораторию диагностического материала.
Определение ЛЧ с помощью молекулярно-биологических методов основано на выявлении мутаций, ассоциированных с развитием лекарственной устойчивости к ПТП. Основное преимущество таких методов заключаются в скорости получения результатов анализа – 1–2 дня, что достигается вследствие возможности использования для тестирования непосредственно клинического материала, хотя возможно использование также и первичной культуры.
Необходимо учитывать, что наборы реагентов, основанные на применении разных методов, характеризуются разными показателями чувствительности и специфичности. Гибридизационные технологии, такие как ДНК-микрочипы, могут обнаруживать только конкретные мутации, внесенные в дизайн диагностических наборов и/или дикий тип МБТ. Их диагностическая чувствительность в значительной степени зависит от спектра генетических изменений штаммов МБТ, характерных для данного географического региона, в случае наличия других мутаций исследование будет давать ложноотрицательные результаты.
Метод секвенирования является «золотым стандартом» в молекулярной диагностике, он может определять любые изменения в нуклеотидной последовательности, в т. ч. протяженные инсерции и делеции. На сегодняшний день выпускаются наборы реагентов, а также специальное программное обеспечение, автоматизирующее процесс получения результатов.
Из вышеназванных исследований тестами лабораторной диагностики in vitro являются IGRA, в настоящее время представленные наборами QFT-IT и T-SPOT. TB. Исследование основано на стимуляции мононуклеарных клеток пациента антигенами, специфичными для M.tuberculosis complex, в ответ на которую высвобождается гамма-интерферон (IFN-.). АГ представлены секреторным белком 6-kDa early-secreted antigenic target (ESAT-6), его шапероном 10-kDa culture filtrate protein (CFP-10), а также дополнительным туберкулезным протеином TB 7.7 (p4) (только в наборе QFT-IT). Эти белки отсутствуют у всех вариантов вакцинного штамма M.bovis BCG и большинства НТМБ, за исключением M.kansasii, M.marinum, M.szulgai, M.flavescens и M.gastrii. Следовательно, оба теста всегда будут давать отрицательный результат при поствакцинальной аллергии или БЦЖ-ите, и ложноположительный результат при наличии в организме НТМБ: M.kansasii, M.marinum или M.szulgai, имеющих клиническое значение.
Тесты IGRA не могут дифференцировать у человека состояние инфицированности МБТ (латентный ТБ) и активный ТБ. Их результаты должны оцениваться совместно с клиническими и рентгенологическими данными, сведениями о контактах, микробиологическими исследованиями и т. д. Особое значение приобретает использование тестов IGRA в странах, где проводится вакцинация БЦЖ. В случае положительной пробы Манту и отрицательном результате теста IGRA у пациента достоверно подтверждается состояние поствакцинальной аллергии. При конверсии результатов теста IGRA, т. е. при изменении отрицательного результата на положительный, риск последующего развития активного туберкулезного процесса не увеличивается. У иммуносупрессивных пациентов IGRA-тесты, как и проба Манту, будут отрицательными, что не может исключить у них активного туберкулезного процесса.
Наиболее удобно применять тесты IGRA у пациентов, ранее вакцинированных против ТБ, у лиц, имеющих противопоказания к проведению кожного теста, у детей, а также у тех пациентов, которым сложно попасть на повторный прием к врачу через 72 часа для определения результатов пробы Манту. В зарубежной практике тесты IGRA используют вместо или вместе с пробой Манту, во многих странах такие исследования закреплены законодательно.
IGRA-тесты являются качественными, их результаты выдаются в категориях: положительный, отрицательный и неопределенный.
Положительный результат означает текущую инфекцию МБТ, но не позволяет дифференцировать недавнее инфицирование МБТ от ранее произошедшего, а также оценить степень активности туберкулезного процесса.
Отрицательный результат чаще означает отсутствие МБТ в организме человека, но может наблюдаться и при супрессии Т-клеточного звена иммунной системы, наступившей вследствие иммунодефицитного состояния, в т. ч. и при прогрессировании туберкулеза. В этом случае следует ориентироваться на результаты прямых методов исследования, подтверждающих специфическую природу заболевания.
В редких случаях результаты тестов не могут быть интерпретированы вследствие не прохождения положительного контроля теста и оцениваются как неопределенные. В этом случае нельзя ни подтвердить, ни исключить туберкулезную инфекцию.
Следует помнить, что у части больных не удается обнаружить МБТ традиционными микробиологическими методами и даже методом ПЦР (если не проводится биопсийный забора материала). В этих случаях диагноз ТБ будет основываться на клинических данных, результатах косвенных методов диагностики и терапии ex juvantibus, а принимаемые по этому поводу решения полностью зависят от квалификации и опыта врача-фтизиатра. Вследствие этого, учитывая биологические особенности микроорганизма, а также иммунного ответа организма человека, диагностика ТБ не может ограничиваться каким-либо одним методом и должна проводиться комплексно.
Показания к применению лабораторных исследований для диагностики туберкулеза у больных ВИЧ-инфекцией и особенности интерпретации их результатов. Основной принцип диагностики туберкулеза у больных ВИЧ-инфекцией такой же, как и у пациентов с ВИЧ-негативным статусом – выявление достоверных признаков специфического воспаления (детекция возбудителя либо морфологическая верификация).
Самым важным в диагностике туберкулеза у больных ВИЧ-инфекцией является выявление возбудителя. У этой категории больных частота выявления МБТ из мокроты уменьшается по мере снижения количества CD4+лимфоцитов (ввиду снижения регистрации деструктивных форм). Однако при глубоком иммунодефиците (менее 100 клеток/мкл), вероятность обнаружения МБТ повышается (за счет огромного количества возбудителя в легочной ткани). Важно отметить, что у больных полиорганным туберкулезом не менее ценным, чем исследование мокроты, является выявление возбудителя в другом диагностическом материале. Поэтому необходим обязательный поиск МБТ в любых биологических жидкостях и биопсийном материале. Также для детекции МБТ целесообразно применять молекулярно-биологические методы, чувствительность и специфичность которых значительно превосходит традиционные микробиологические методы.
Туберкулиновая чувствительность у больных с активным туберкулезом на фоне ВИЧ-инфекции снижается по мере прогрессирования иммунодефицита, и у пациентов с количеством CD4+лимфоцитов менее 100 клеток/мкл частота регистрации положительной пробы Манту с 2 ТЕ не превышает 10%, а при количестве CD4 клеток более 500/мкл она сопоставима с группой больных без ВИЧ-инфекции (до 95%). Проведенные клинические исследования показали, что при высокой специфичности Диаскинтеста (до 100%), чувствительность этого диагностического метода также снижается по мере уменьшения количества CD4+лимфоцитов и сопоставима с чувствительностью реакции Манту.
При неинформативности туберкулинодиагностики, Диаскин- и IGRA-тестов, снижении вероятности выявления МБТ в мокроте и расширении дифференциально- диагностического ряда за счет других вторичных заболеваний в диагностике специфического процесса важную роль приобретает малоинвазивная хирургия с целью морфологической верификации туберкулезного процесса. Морфология туберкулезного воспаления тесно связана с состоянием иммунной системы больного и в значительной степени зависит от него. Гистоморфологические проявления туберкулезного воспаления при ВИЧ-инфекции утрачивают свои специфические признаки по мере ее прогрессирования. У больных с количеством СD4+лимфоцитов более 350 клеток/мкл сохраняется способность к формированию типичной гранулематозной реакции. В биоптатах пациентов с более тяжелой степенью иммуносупрессии (число СD4+лимфоцитов 200–350 в мкл) преобладает несовершенная стертая гранулематозная реакция. Это свидетельствует о смене реакции гиперчувствительности замедленного типа, типичной для туберкулеза, реакцией гиперчувствительности немедленного типа. Состояние выраженного иммунодефицита (при количестве СD4+лимфоцитов менее 200 клеток/мкл), характеризуется в большинстве случаев некротическими изменениями с выраженным экссудативным компонентом воспаления. Однако при проведении микроскопии препаратов биопсии с окраской по Циль-Нильсену обнаруживаются кислотоустойчивые бактерии в большом количестве (20-50 и более в одном поле зрения). В связи с этим у больных ВИЧинфекцией, особенно на фоне выраженной иммуносупрессии, важно проведение комплексного поэтапного изучения биопсийного материала с проведением микроскопии препаратов с окраской по Цилю-Нильсену, микроскопических исследований с применением методов иммуногистохимии (использование моноклональных АТ к M. tuberculosis) и ПЦР для выявления ДНК МБТ в нативном материале и из парафиновых гистологических блоков. Обнаружение микобактерий в кале, мокроте или бронхоальвеолярном лаваже при отсутствии клинической симптоматики может свидетельствовать только о колонизации слизистых оболочек.